|
A pesar de los avances en el tratamiento de las cataratas infantiles, estas
continúan siendo la causa principal de visión disminuida y ceguera en los
niños, y la ambliopía irreversible, la causa más común de resultados
visuales pobres, después de la cirugía de la catarata.
Las encuestas sobre la prevalencia de las cataratas infantiles (1), varían
mucho de unos países a otros. En EE.UU., hay encuestas que dan una prevalencia
del 1,2 por cada 10.000 habitantes, y otras que dan 1,4 para la población
blanca y 1,7 para la no blanca. En el Reino Unido, en 1970 sería de 5, y en
1984 de 6, en Suiza es de un 4 y en Francia de 2,2 todos ellos por cada 10.000
habitantes. Bermejo y Martínez-Frías (2), analizando 1.124.654 nacimientos
consecutivos en España entre 1980 y 1995, encuentran cataratas congénitas en
6,31 niños de cada 100.000 nacidos. Estas diferencias, dependen en parte de la
forma de recoger los datos, que en unas ocasiones priman las cataratas
congénitas y en otras las adquiridas.
RECUERDO ANATÓMICO
En el recién nacido el cristalino se compone de núcleo (embrionario y
fetal) y corteza, ambos encerrados por la cápsula. El núcleo embrionario es la
parte central clara del cristalino, que se desarrolla en los tres primeros meses
del embarazo, a partir del epitelio posterior del mismo. Por fuera del núcleo
embrionario esta el núcleo fetal, formado por fibras que provienen del epitelio
ecuatorial anterior y que se juntan en ambas suturas en Y (la anterior derecha y
la posterior invertida). El material periférico a estas suturas es la corteza
del cristalino. Al nacimiento, los núcleos fetal y embrionario constituyen la
mayoría del volumen del cristalino, mientras que las fibras corticales son
escasas y continúan produciéndose durante toda la vida, a partir del epitelio
ecuatorial anterior, para formar el núcleo y la corteza del adulto. El
cristalino esta mantenido en posición por la zónula y alojado en la foseta
patelar del vítreo, al que está íntimamente unido a través del ligamento de
Wiegers. Tanto los núcleos como la escasa corteza infantil, están
perfectamente hidratados y, por lo tanto, son blandos y pueden reabsorberse o
aspirarse a través de un pequeño orificio.
CLASIFICACIÓN DE LAS CATARATAS INFANTILES
La situación y características de una catarata pueden proporcionar
información sobre su causa y evolución. El lenticono posterior, la catarata
zonulár y la sub-capsular anterior y posterior, son situaciones generalmente
progresivas, mientras que las cataratas polares y nucleares anteriores tienden a
ser más estáticas. De acuerdo con su localización las cataratas se pueden
clasificar en:
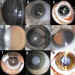
Figura 1. 1: Catarata polar anterior. 2: Catarata piramidal. 3, 4 y
5: Cataratas nucleares zonulares. 6: Catarata suturaria. 7: Catarata supcasular
superior. 8: Catarata completa. 9: Catarata traumática.
Cataratas anteriores
Catarata Polar Anterior (Beer 1817). Este tipo de catarata generalmente es
una opacidad pequeña, blanca, de menos de 3 mm de diámetro, localizada en el
centro de la cápsula anterior y a veces, conectada con restos de membrana
pupilar persistente. Un tercio de las cataratas polares anteriores son
bilaterales, la mayoría no son progresivas y afectan poco a la visión, por lo
que generalmente no requieren cirugía. La mayor parte de estas cataratas son
esporádicas y sólo unas pocas se transmiten de forma autosómica dominante.
Una variedad de estas cataratas polares anteriores, es la catarata piramidal
anterior que es una catarata blanca, de forma cónica que hace protusión en la
cámara anterior. La base del cono es de unos 2 a 2,5 mm de diámetro y puede
estar ro deada de opacidades corticales. La opacidad cónica no suele ser
suficiente para impedir el desarrollo de la visión, sin embargo, los cambios
corticales circundantes, pueden progresar hasta hacer necesaria la intervención
quirúrgica.
Catarata Sub-capsular Anterior. En ella las opacidades se localizan
inmediatamente por debajo de la cápsula anterior, apareciendo tiempo después
del nacimiento, y casi siempre su origen es idiopático.
Cataratas centrales
Catarata Nuclear (Doyne 1888, von Hippel 1895). Esta opacidad, generalmente
congénita, se localiza en los núcleos embrionario o fetal y suelen ser
estacionarias, aunque a veces progresan y se extienden a capas corticales
adyacentes. Las cataratas nucleares pueden ser unilaterales (esporádicas) o
bilaterales (autosómicas dominantes).
Catarata Suturaria (von Hasner 1865). Las cataratas suturarias, son un tipo
de catarata nu clear congénita, con la opacidad concentrada a lo largo de una o
las dos suturas en Y, en el área del núcleo fetal. Estas cataratas pueden ser
progresivas y extenderse a la corteza o al núcleo embrionario central. Las
formas bilaterales suelen ser autosómicas dominantes, pero también hay casos
recesivos ligados al sexo.
Catarata Zonular (Jaeger 1854). Ésta es una opacidad cortical blanquecina,
que rodea el núcleo del cristalino por fuera de las suturas en Y. La catarata
se desarrolla en capas como una cebolla, con zonas claras que alternan con
láminas corticales blancas. A menudo además de las opacidades
circunferenciales, hay otras radiales (los jinetes) también zonulares de
aspecto pulverulento. Estas cataratas aparecen en los primeros meses de la vida.
La mayoría de las cataratas zonulares son progresivas y en el futuro
requerirán cirugía, y puesto que el cristalino permanece relativamente
transparente durante el período crítico de desarrollo de la visión, el
pronóstico visual tras la cirugía es bueno, cuando se realiza precozmente. Las
cataratas zonulares casi siempre son bilaterales y se heredan de forma
autosómica dominante, pero también las hay secundarias a enfermedades
metabólicas, como la hipoglucemia neonatal o la galactosemia.
Cataratas posteriores
Catarata Capsular Posterior. Las causas más comunes, de catarata capsular
posterior unilateral en el niño son: el lenticono posterior y la persistencia
de vascularización fetal.
El Lenticono Posterior (Meyer 1888) es un adelgazamiento congénito de una
parte de la cápsula posterior que se sacula herniándose las fibras
cristalinianas en su interior. Al principio, la corteza herniada es
transparente, pero con el paso del tiempo, se opacifica y progresa a una
catarata subcapsular posterior. El lenticono posterior casi siempre es
unilateral, ocurre esporádicamente y a menudo requiere cirugía. Cuando es
transparente, el lenticono produce miopía y astigmatismo irregular y, por
tanto, puede originar ambliopía.
En la Persistencia de la Vascularización Fetal (Meissner 1855) el primitivo
sistema vascular hialoideo se mantiene en mayor o menor grado. En los casos más
completos, el tejido fibrovascular sale de la papila y llega hasta la cápsula
posterior del cristalino cubriéndola por detrás, y traccionando los procesos
ciliares, y en los casos mínimos, se aprecia una pequeña opacidad congénita
blanca, en la cápsula posterior, nasal al eje visual central, llamada huella de
Mittendorf, que no altera la agudeza visual.
Catarata Sub-Capsular Posterior. Esta, es una opacidad cortical situada justo
delante de la cápsula posterior. Estas cataratas casi siempre aparecen después
del nacimiento, pueden ser idiopáticas pero también pueden asociarse al
síndrome de Down, al uso continuado de esteroides, a traumatismos contusos, o a
un lenticono posterior. Debido a su situación posterior, cerca del punto nodal
óptico del ojo, las cataratas sub-capsulares posteriores tienden a afectar
bastante la visión, y a menudo requieren cirugía.
Catarata en Gota de Aceite. En ella hay una opacidad ligera, en el centro de
la corteza posterior del cristalino que en retro iluminación parece una gota de
aceite. Las cataratas en gota de aceite suelen asociarse con galactosemia y en
tal caso, si se diagnostican precozmente y se elimina la galactosa de la dieta,
la catarata puede desaparecer.
Catarata difusa
Catarata Cristalina (Gunn 1895). Una catarata formada por múltiples manchas
pequeñas que, cuando la luz se refleja, da el aspecto de cristales coloreados
en la corteza. Estas cataratas pueden asociarse con distrofia miotónica,
pseudo-hipoparatiroidismo e hipoparatiroidismo.
Catarata Cerúlea. Formada por pequeñas opacidades azuladas dispersas a lo
largo de la corteza. Pueden verse en el síndrome de Down, se desarrollan
durante la pubertad, y se localizan en la corteza cercana al núcleo. Son
bilaterales, normalmente no progresan, y causan una pérdida visual mínima.
Catarata Total. La catarata total, es una opacidad que afecta a la totalidad
del cristalino, y puede asociarse al síndrome de Down, a alteraciones
metabólicas, o ser traumática o hereditaria autosómica dominante.
Catarata Membranosa (Ammon 1833). En ella el material cristaliniano
desaparece y la cápsula anterior y posterior entran en oposición. Puede
asociarse con traumas, infecciones intrauterinas, o puede ser secundaria a un
desarrollo anómalo del cristalino.
ETIOLOGÍA DE LAS CATARATAS PEDIÁTRICAS
Cuando se considera la etiología de las cataratas congénitas o infantiles,
es útil hacer la distinción entre unilaterales y bilaterales.
Cataratas Congénitas Bilaterales
En contraste con las cataratas unilaterales, las bilaterales a menudo se
heredan, y pueden asociarse con enfermedades sistémicas. La lista de
enfermedades sistémicas asociadas es larga e incluye las alteraciones
metabólicas, las anoma lías craneo-faciales, enfermedades cromosómicas, e
infecciones intrauterinas. Las cataratas congénitas o infantiles bilaterales, o
tienen una causa identificable, o se heredan en aproximadamente el 60% de los
casos.
Cataratas Congénitas Unilaterales
Las cataratas congénitas unilaterales son causadas por disgenesia local; en
principio ni se asocian con enfermedades sistémicas ni se heredan, y suelen ser
de etiología desconocida. Las cataratas asociadas con disgenesias oculares son:
la secundaria a persistencia de la vascularización fetal, el lenticono
posterior, la catarata polar anterior, y el síndrome de disgenesia de la
cámara anterior. Las cataratas unilaterales a menudo se asocian con micro
córnea y microftalmos.
Cataratas bilaterales
1. Idiopáticas (60%)
2. Cataratas hereditarias (30%), sin enfermedad sistémica
a. Autosómica dominante (modelo de herencia más común)
b. Autosómica recesiva
c. Ligada al sexo
3. Enfermedades metabólicas
a. Galactosemia
b. Enfermedad de Fabry
c. Hipoglucemia
d. Hipoparatiroidismo
e. Pseudo-hipoparatiroidismo
f. Diabetes mellitus.
4. Enfermedades genéticas sistémicas
a. Síndrome oculo-cerebro-renal de Lowe
b. Trisomias
I) Síndrome de Down (trisomia 21)
II) Síndrome de Edward (trisomia 18)
III) Síndrome de Patau (trisomia 13)
c. Síndromes locomotores
I) Distrofia Miotónica
II) Condrodisplasia puntata
III) Osteogénesis imperfecta
IV) Síndrome de Majewski
d. Síndromes cerebrales centrales
I) Síndrome de Sjogren-Larson
II) Síndrome de Marinesco-Sjogren
e. Síndrome de Marfan
f. Síndrome de Conradi
g. Enfermedad de Wilson
h. Síndrome del grito del gato
i. Xantomatosis cerebrotendinosa
j. Síndromes Craneofaciales
I) Síndrome de Alport
II) Síndrome de Hallermann-Streiff
III) Síndrome de Pierre-Robin
IV) Síndrome de Smith-Lemli-Optiz
V) Síndrome de Albrigh
VI) Síndrome de Crouzon
k. Síndromes multisistémicos
I) Síndrome de Werner
II) Síndrome de Nooanan
l. Síndrome de Turner
m. Síndrome de Stickler
n. Síndrome de Zeliweger
ñ. Síndrome de Wilson
o. Síndrome de Hallgren
p. Síndrome de Laurence-Moon-Bardet- Biedl
q. Enfermedad de Refsum
r. Esclerodactilia
s. Síndrome de Rubinstein-Taybi
5. Infecciones puerperales
a. Rubeola
b. Citomegalovirus
c. Varicela
d. Sífilis
e. Toxoplasmosis
f. Herpes simple
6. Anomalías oculares
a. Aniridia
b. Disgenesia del segmento anterior
c. Microftalmía
Cataratas unilaterales
1. Idiopáticas (80%)
2. Anormalidades oculares
a. Lenticono posterior
b. Persistencia de la vascularización fetal
c. Disgenesia del segmento anterior
d. Tumores del polo posterior
3. Traumatismos del parto (raro)
4. Cataratas bilaterales enmascaradas
5. Infecciones intrauterinas (rubéola: raro)
Cataratas adquiridas
1. Idiopáticas
2. Cataratas hereditarias
a. Autosómica dominante
b. Autosómica recesiva
c. Ligada al sexo
3. Traumáticas
4. Metabólicas
a. Galactosemia
b. Enfermedad de Fabry
c. Hipoglucemia
d. Hipoparatiroidismo
e. Pseudo-hipoparatiroidismo
f. Diabetes mellitus.
g. Hiperalimentación
5. Dermatológicas
a. Síndrome de Rothmund-Thomsom
b. Síndrome de Cockayne
c. Incontinencia pigmenti
d. Ictiosis congénita
e. Dermatitis atópica
6. Enfermedades oculares
a. Retinosis Pigmentaria
b. Aniridia y otras disgenesias
c. Persistencia de vítreo primario hiperplásico
d. Amaurosis congénita de Leber
e. Retinopatía del prematuro (vacuolas)
7. Por radiaciones
8. Medicamentosas
a. Corticoides
b. Clorpromacina
c. Ergotamina (cornezuelo del centeno)
d. Naftaleno
e. Triparanol
9. Inflamatorias
a. Artritis reumatoide juvenil
b. Sarcoidosis
c. Parsplanitis
Exploración y sintomatología
Los signos, síntomas y razones por los que se diagnostica una catarata, de
mayor a menor índice de frecuencia son: 1.º disminución de visión que, o
notan los padres, o manifiesta el propio enfermo cuando alcanza cierta edad,
2.º exploración rutinaria o secundaria a cualquier otra enfermedad, 3.º
leucocoria, 4.º estrabismo, generalmente esotropía en los más pequeños y
exotropía en los mayores, 5.º nistagmos en las cataratas bilaterales, y 6.º
glaucoma doloroso, microftalmos o cualquier otro tipo de anormalidad ocular.
El examen ocular debe hacerse con la pupila dilatada y lámpara de hendidura
manual, abriendo el ojo con un blefarostato, y mejor bajo anestesia general que
se aprovechará para tomar la presión intra-ocular. Se verificará primero si
la catarata es uni o bilateral y cual es su morfología y posición. Hay que
medir y comparar los diámetros corneales. El iris también debe examinarse
cuidadosamente en busca de membranas persistentes, roturas del esfínter que
sugieran un posible traumatismo, o anomalías que indiquen la existencia de un
síndrome de clivaje. Un examen oftalmoscópico indirecto, despistará cualquier
patología del polo posterior y si este no puede visualizarse con claridad, se
realizará una ecografía. El oftalmoscopio directo, nos ayudará a juzgar el
grado de opacidad cristaliniana.
Mientras que en las cataratas unilaterales necesitaremos pocas pruebas
complementarias, las cataratas bilaterales nos harán sospechar un origen
hereditario o una enfermedad sistémica asociada, por lo que hay que hacer un
buen estudio genético, así como un examen pediátrico completo, análisis de
orina para despistar galactosemia, y títulos para TORCHS (Toxoplasmosis,
Rubeola, Citomegalovirus, Herpes y Sífilis).
TRATAMIENTO DE LAS CATARATAS EN EL NIÑO
La ambliopía es la causa mas frecuente de visión disminuida en las
cataratas congénitas e infantiles. Los primeros meses de vida representan el
período crítico de desarrollo visual, cuando las áreas visuales del cerebro
se están desarrollando rápidamente estimuladas por la impresión de imágenes
claras sobre la retina, de tal forma que una imagen deficiente unilateral o
bilateral incidiendo sobre la retina durante este período crítico, producirá
una ambliopía irreversible. Son ya clásicos los trabajos de Wiesel y Hubel (3)
con gatos, posteriormente confirmados por von Noorden (4) en monos, en los que
los ojos de estos animales se ocluían desde el nacimiento, hasta pasados tres
meses, comprobando que al destaparlos, todos ellos eran ciegos y sólo
conseguían una recuperación parcial. También sabemos, que si un paciente que
tiene una catarata completa desde el nacimiento, se opera a los 7 años de edad,
no hay recuperación alguna, permaneciendo definitivamente ciego. Por todo, ello
son muchos los autores que desde los años 70 plantean la cirugía precoz de las
cataratas congénitas (5-12), tanto uni como bilaterales. Rodgers (13) encontró
en una serie de cataratas congénitas bilaterales que afectaban al eje visual,
ambliopía irreversible y nistagmos, a menos que se operasen antes de los 2
meses de edad. La mayoría de los autores están de acuerdo en que, las
cataratas congénitas unilaterales o bilaterales visualmente significativas,
deben de quitarse y corregirse la afaquia lo más pronto posible, siempre antes
de los 2 meses y a ser posible durante la primera semana de vida. La
rehabilitación visual muy temprana puede conseguir una agudeza visual buena y
fusión con estereopsis, incluso en pacientes con cataratas congénitas
unilaterales.
Hay que tener en cuenta que:
1) Las cataratas congénitas parciales tienen mejor pronóstico que las
totales.
2) La capacidad ambliopigénica de una catarata depende del grado de
afectación del eje visual.
3) Incluso una catarata central puede ser poco ambliopigénica con la pupila
dilatada (fenilefrina 2 1/2%, tropicamida o ciclopléjico).
4) Las cataratas progresivas suelen tener mejor pronóstico que las que
afectan el eje visual desde el nacimiento.
5) Las cataratas bilaterales suelen tener mejor pronóstico que las
unilaterales.
6) Las cataratas bilaterales con nistagmos tienen mal pronóstico.
7) Las cataratas unilaterales en ortoforia tienen buen pronóstico.
8) Una opacidad central debe ser por lo menos de 3 mm para que sea
visualmente peligrosa.
9) Una buena visualización de los detalles de la retina y especialmente de
la mácula con el oftalmoscopio directo, es una indicación de que el eje visual
esta bastante transparente.
10) En una agudeza visual de 1/6 o peor (optotipos o visión preferencial),
el deslumbramiento, la fotofobia, el nistagmos, el estrabismo o el guiño del
ojo afectado son indicaciones de cirugía.
11) Eliminar completamente todo estímulo luminoso en ambos ojos mediante una
oclusión bilateral, es menos ambliopigénico que una mala imagen (tiempo
máximo probado de oclusión bilateral, 17 días) (14).
TRATAMIENTO QUIRÚRGICO
En contraste con las cataratas seniles que tienen un núcleo deshidratado y
duro, el núcleo en las cataratas de pacientes por debajo de los 30 años de
edad es blando y por lo tanto puede ser fácilmente aspirado a través de una
cánula.
Desde los inicios de la extracción intra-capsular de las cataratas, bien
fuera por compresión (Harp 1753) o por tracción (Terson 1870) esta se
consideró una técnica contraindicada en las cataratas infantiles, debido a la
fuerte unión entre el cristalino y el vítreo (ligamento de Wiegers) en el
niño, lo que originaba pérdidas muy importantes del mismo en el momento de la
extracción. La discisión de la cápsula anterior (Barbette 1672) fue durante
casi 3 siglos la técnica quirúrgica más comúnmente empleada en las cataratas
del infante, seguida de la extracción lineal (Daviel 1742) con o sin lavado,
que solía usarse en los casos peores. Con ambos métodos, aunque más con el
primero, la hipertensión, la inflamación o las reoperaciones eran la regla, y
casi todas terminaban en una discisión de la cápsula posterior. Por ello
muchos cirujanos preferían, si la catarata era parcial, hacer una iridectomía
óptica total, que tenia la ventaja de mantener la acomodación (15,16). La
técnica de Scheie (17) de aspiración de las cataratas blandas, y el uso
generalizado del microscopio quirúrgico, supuso una importante mejora en los
resultados finales, disminuyendo el número y la gravedad de las complicaciones
a corto y largo plazo. Scheie utilizaba una aguja de 19 G conectada a una
jeringa con 2 cc de suero, que introducía a través del limbo y una vez rota la
cápsula anterior, iba aspirando e inyectando alternativamente, hasta extraer la
totalidad de las masas; cuando la catarata era incompleta realizaba primero una
discisión, y días después la aspiración. El desarrollo de instrumentos de
infusión y aspiración para la retirada del córtex en las cataratas seniles ha
facilitado extraordinariamente la cirugía de las cataratas infantiles (18-21).
También el vitrectomo es de gran ayuda, tanto para la capsulotomía anterior,
como para la aspiración, como para la capsulotomía posterior, y como para
aquellos casos, la mayoría, en que se indica una vitrectomía anterior (22),
aunque ya apenas se utilizan las lensectomías vía pars-plicata, que tanto se
practicaron al principio de los años 80 (23,24).

Figura 2. Técnica de Gimbel: captura del cuerpo de la lente en la
capsulorrexis posterior.
La técnica quirúrgica incluye:
1) Incisión corneal que debe ser pequeña (2-3 mm) y muy valvulada para
evitar la salida del iris que en los niños es muy laxo y por ello se hernia con
facilidad.
2) Capsulorrexis que en la cápsula muy flexible de los cristalinos jóvenes
es difícil de controlar debiendo hacerse más por tracción desde el sitio
opuesto, que por desgarro continuo. Como en esta cirugía no hay ningún núcleo
que al exprimirlo, rompa la cápsula anterior hasta los fondos de saco, es
posible hacer una capsulotomía en abrelatas, o mordiendo con el vitrectomo, y
mantener luego la integridad sacular durante toda la cirugía, para finalmente,
soportar en su interior una lente, sin que se produzca su descentramiento
post-operatorio.
3) Aspiración de las masas cristalinianas en su totalidad mediante un
sistema de infusión-aspiración manual o automático. Muchos prefieren usar de
aspirador-infusor, un vitrectomo de cámara anterior, o uno posterior ayudado de
un mantenedor de cámara.
4) Realización, cuando se considere necesario, de una capsulorrexis
posterior, que puede ser sustituida por uno o dos mordiscos de vitrectomo, dada
la especial elasticidad de la cápsula posterior de los infantes, capaz de
transformar en redondo cualquier tipo de desgarro. Luego se vitrectomizará o se
rechazará el vítreo con un visco-elástico, dependiendo de lo que pretendamos
hacer.
5) Cuando esté indicado introducir una lente intra-ocular, se realizará una
apertura suficiente para permitir la colocación de una de ellas, rígida o
plegable en el saco capsular. Gimbel (25) preconiza el herniado del cuerpo de la
LIO a través de la capsulorrexis posterior, como un método para evitar la
aparición de membranas secundarias.
Todas las maniobras se realizarán con la ayuda de hialuronidato sódico,
preferiblemente de alta densidad.
Terminaremos suturando la herida y extrayendo el visco-elástico.
COMPLICACIONES DE LA CIRUGÍA DE LA CATARATA
Las complicaciones post-operatorias mas frecuentes son: el glaucoma crónico,
el desprendimiento de retina, el glaucoma agudo por bloqueo pupilar, la
formación de membranas secundarias, la inflamación y la endoftalmitis (26-28).
La cicatriz filtrante, la hernia o la incarceración del iris o del vítreo en
la herida, (7) son hoy en día mucho menos frecuentes que antaño, y casi
siempre consecuencia de una técnica deficiente. Si la incisión, la sutura y la
vitrectómía son cuidadosas no debe producirse ninguna de estas complicaciones.

Figura 3. 1 y 2: Fibrina. 3: Sinequia. 4: Perlas capsulares.
La inflamación post-operatoria dependerá en mucho de la edad del niño, del
tipo de catarata (las rubeólicas y las artríticas son especialmente
flogísticas) y de la técnica quirúrgica, y será responsable de la aparición
de otras complicaciones. Para Jameson (29) (que por el limbo tras la aspiración
hace una amplia capsulotomía con vitrectomía anterior) la inflamación
clínicamente significativa (fotofobia y dolor, con enrojecimiento, quemosis,
Tyndal y celularidad de cámara anterior) se presenta preferentemente después
de los 18 meses de edad, probablemente debido a la ausencia de respuesta
inmunológica en el niño recién nacido. Sin embargo, si no se hace
capsulotomía posterior, esta es pequeña, o se implanta una LIO, la
inflamación antes de esta edad, puede ser muy considerable y altamente
peligrosa, no sólo por sí misma, sino también por el retraso en el inicio del
tratamiento de la ambliopía (3 ó 4 semanas). Cuando la reacción fibrinoide es
abundante, lo que es muy frecuente tras la implantación de una lente
intra-ocular, sobre todo por debajo de los tres años, la inyección de
activador tisular del fibrinógeno suele dar magníficos resultados (30)
naturalmente acompañado de corticoides y atropina.
La formación de membrana secundaria dependerá en gran parte, de la
inflamación previa, pre o post-operatoria, pero sobre todo de la técnica
empleada (31), pues mientras sobrepasa el 60% si se deja intacta la cápsula
posterior, será de un 12%, si se practica una pequeña capsulotomía, y de casi
el 0% si la capsulotomía es grande, o la lensectomía-vitrectomía se hace vía
pars-plicata; por ello, cuando el niño tiene menos de 7 años de edad, mordemos
con el vitrectomo la cápsula posterior y hacemos una vitrectomía, se coloque o
no una LIO. En otras ocasiones preferimos luxar la parte óptica de la lente, a
través de una capsulorrexis posterior.
El glaucoma, muy frecuente en otros tiempos cuando se hacía una simple
discisión de la cápsula, oscila en este momento entre el 5% y el 12% (32,33)
siendo en su mayoría, alrededor del 80%, de ángulo abierto y sólo en un 10%
de ángulo cerrado (34). Suele presentarse después del 2.º año de la cirugía
y en su mayor parte después de los 10 años. Asrani y col. (35) en una serie de
377 cataratas con una edad media de 5,1 años, operados por diversos cirujanos
con implantación de una LIO de cámara posterior, encontraron sólo un caso de
glaucoma de ángulo abierto, llegando a la conclusión, de que esta técnica
evita la aparición de glaucoma tras la cirugía de cataratas infantiles. Sin
embargo Lambert (36), considera que si esta técnica se utiliza antes de las 16
semanas de vida, mas del 80% de los ojos necesitarán reoperarse por padecer
complicaciones graves, entre las que se encuentra el glaucoma de ángulo
abierto.
Podemos concluir que la presión ocular debe de ser explorada periódicamente
en todos los individuos que han sido operados de cataratas infantiles.
El desprendimiento de retina se presenta en el 1 ó 2% de los operados,
siendo más frecuente en los ojos que presentan alguna otra anomalía
congénita.
El edema macular quístico en general se considera poco frecuente en niños,
pero mientras Gilbard (37) lo encuentra en menos de un 4% tras
lensectomia/vitrectomía, para Hoyt es de un 37% con el mismo sistema y de sólo
un 3,7% en caso de simple discisión/aspiración (38). Lo cierto es que el E.M.Q
consecutivo a cirugía del globo ocular en los niños está poco estudiado como
consecuencia de las dificultades exploratorias en los más pequeños.
La captura de la lente (39), su desplazamiento o luxación, son
complicaciones menos frecuentes tras el uso de la capsulorrexis, mientras las
sinéquias posteriores (40) y el desplazamiento pupilar, son complicaciones
frecuentes.
TRATAMIENTO DE LA AFAQUIA
La corrección de la afaquia dependerá de la edad del niño, de que sea uni
o bilateral, del estado del ojo, del tipo de catarata y de la causa de esta.
Podremos corregir con gafas, con lentes de contacto o con lente intra-ocular.
Choyce fue el primero que introdujo una LIO de cámara anterior en un niño
con una catarata unilateral en 1955 (41). Binkhorst a partir de 1959 implanta
LIOs irido-capsulares en niños, primero en cataratas traumáticas (42) y luego
en congénitas (43) e Hiles (44,45) publica en 1984, una serie de 225 cataratas
operadas entre 1974 y 1983 con LIO, entre traumáticas (40%) y espontáneas
(60%), y todas ellas al igual que hacían sus predecesores, monoculares. En los
primeros casos utilizó lentes irido-capsulares, luego suturadas a iris y desde
1982 de cámara posterior. A lo largo de los años 80 se publicaron diversos
trabajos, todos ellos en cataratas unilaterales, y definiéndose
mayoritariamente por las LIOs de cámara posterior (46-48). Al mismo tiempo, se
va desarrollando la idea de mantener constantemente la zona central clara, por
lo que antes o después de colocada la lente, se realizará una capsulotomía
posterior y una vitrectomía anterior (49 a 52). Únicamente en los niños con
edad de colaborar se mantendrá la cápsula posterior íntegra, para romperla
con láser de neodimio- yag, cuando se opacifique. Cuando se disponga de este
láser en quirófano, se puede dejar siempre intacta la cápsula y escindirla
con el láser pocas semanas después, (53) recordando, que cualquier retraso en
la perfecta claridad del eje visual es peligroso pues engendra ambliopía.
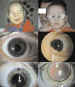
Figura 4. Corrección con gafas, lentes de contacto y lente
intraocular.
La capsulorrexis circular continua de Neu hann, (54,55) se incorporó
rápidamente a la cirugía infantil y se popularizó, mejorando la técnica y
los resultados, aunque es más difícil de ejecutar en la cápsula de un
cristalino joven. Con la capsulorrexis aseguramos el perfecto centrado de la
lente, disminuyendo la inflamación y la posibilidad de captura. La
capsulorrexis de la cápsula posterior permite obviar la vitrectomía (22,56);
para ello, con la cámara anterior y el saco capsular lleno de material
visco-elástico, se hace una pequeña punción en la cápsula posterior, se
rechaza el vítreo inyectando hialuronidato sódico a través de ella, y luego
se procede a realizar la capsulorrexis, para a continuación introducir la lente
en el saco.
Si bien durante muchos años las cataratas infantiles operadas con lente
intra-ocular fueron monoculares, desde finales de los 80 (57) estas se vienen
utilizando también en las bilaterales.
Nosotros en general, preferimos la LIO después de los 21/2 a 3 años de
edad, tanto para las cataratas de un ojo como para la de los dos, puesto que
después de esta edad, la inflamación es menor y a partir de entonces, el ojo
crecerá poco más de 2 mm y la córnea tendrá ya su curvatura, por tanto, al
llegar a la edad adulta será miope de unas 3 ó 4 dioptrías y estará enfocado
para cerca. Excluiremos de esta norma general las cataratas de origen
inflamatorio, tanto puerperal (rubeola) como post-natal (artritis reumatoide),
la persistencia de vascularización fetal (se puede implantar LIO secundaria) y
las disgenesias oculares (síndromes de clivaje de la cámara anterior).
Hay que tener en cuenta (58), que el mayor crecimiento del eje
antero-posterior del ojo va a ser en los 3 primeros años de la vida, en los que
crece aproximadamente 1 mm por año; en los 4 años siguientes aumentara 0,4 mm
cada uno de ellos, y a partir de los 7 solo 1 mm más hasta su tamaño
definitivo que se alcanza de los 10 a los 15 años. La queratometría, que es de
51-52 D en el momento del nacimiento, pasa a 45 D al final del primer año y a
44 D al final del tercero, siendo las variaciones a partir de entonces poco
significativas (ver tabla 2). Por lo tanto: si corregimos a la emetropía una
LIO pocos días después del nacimiento, (35 D) será miope de 10 u 11 D al
llegar a la edad adulta; si esto lo hacemos cuando tenga 1 año (29 D), será
miope, cuando el ojo deje de crecer, de unas 7 u 8 D y si lo hacemos a los 3
años (23 D) será miope de entre 3 y 4 D después de los 15. Cabe la
posibilidad de colocar una LIO en niños menores de 2 años, calculándola para
los 3 años o para el adulto, y suplir la hipermetropía restante hasta alcanzar
esta edad, con lentes de contacto, si bien es cierto que la inflamación puede
retrasar la adaptación de la lentilla, engendrando ambliopía. Otra opción, es
la de introducir dos lentes, una en saco, con la graduación de adulto, y otra
en surco que complementa esta, hasta alcanzar la refracción propia del niño y
que se extraerá posteriormente (59). Piñero Bustamante ha diseñado una nueva
lente intraocular, que todavía esta en período de fabricación por A.J.L.;
consta de una parte fija que se introduce en el saco, y que esta formada por las
patas de la lente unidas a un anillo donde se engarzará el óptico, y otra
parte intercambiable que corresponde a la zona óptica de la lente. La parte
fija se mete, a través de una incisión de 3 mm, en el saco capsular y luego
por la misma apertura, se introduce plegada la parte óptica, que es redonda y
de material acrílico, para una vez dentro de la cámara anterior, insertarla en
el anillo. El óptico por lo tanto puede extraerse y cambiarse por otro.

En las cataratas bilaterales por debajo de los 3 años de edad, en principio
podemos suplir la afaquia mediante gafas sobre-corregidas en +2,00 ó +3
dioptrías por debajo del año de edad, y de +1,00 a +1,50 D en niños de 1 a 2
años. Se pueden prescribir bifocales para afáquicos bilaterales entre los 3 y
4 años de edad.

Figura 5. Piggy-back.
Para las cataratas unilaterales por debajo de los 2 años de edad, lo mejor
es plantear la colocación de una lente de contacto, que debe ponerse lo antes
posible después de la cirugía incluso dentro de la primera semana del
postoperatorio, aunque algunos cirujanos las colocan ya en la sala de
operaciones. Durante el primer año de vida, es mejor usar una lente de uso
prolongado para asegurar una imagen clara todo el tiempo. Después de esto,
pueden usarse lentes del contacto durante todas las horas del día y quitarlas
por la noche. Con las lentes de contacto también será necesario sobre-corregir
hasta los 4 años y luego usar gafas bifocales que se aprovecharán para
compensar cualquier astigmatismo existente.
La decisión de colocar una lente de contacto o una lente intra-ocular,
dependerá en gran parte de la cultura, posición económica y concienciación
de los padres que deberán colaborar en el cuidado, reposición, limpieza y
colocación de la lentilla, así como en el tratamiento de la ambliopía. Por lo
tanto, si los padres son cultos y colaboradores se elegirá la lente de
contacto, y si los progenitores son inapropiados para seguir el tratamiento, nos
decantaremos por la LIO. De todas formas, en los casos en que el paciente se
haga intolerante a la lente de contacto o sus cuidadores se declaren inhábiles
en el manejo de la misma, podremos introducir una lente intra-ocular secundaria.
Para ello lo mejor es colocarla en surco, aprovechando los restos capsulares
debidamente preparados (60, 61), y en el caso de que estos no existan o sean
insuficientes, suturando una lente preferentemente con agujeros en las patas
(62-64).
Tratamiento de la ambliopía
El tratamiento de la ambliopía se basa en proporcionar una imagen clara a la
retina lo antes posible (idealmente en la primera semana de la vida), eliminando
la catarata y tapando a tiempo parcial el ojo mejor. En el caso de una catarata
congénita unilateral, la cantidad de oclusión necesaria para obtener un
desarrollo visual apropiado del ojo afáquico, dependerá de la edad en que la
retina recibió una imagen clara. Si una catarata congénita unilateral se opera
sin complicaciones en la primera semana de vida, la ambliopía inicial será
moderada y puede empezarse con una oclusión de unas 3 horas al día. Por el
contrario, un niño que se opera después de los 2 meses de edad, habrá tenido
una imagen retiniana turbia durante el período crítico de desarrollo visual, y
tendrá ambliopía importante requiriendo una oclusión, de por lo menos medio
día. Los pacientes con cataratas congénitas unilaterales, requerirán terapia
oclusiva a largo plazo, normalmente hasta los 8 ó 9 años de edad. Naturalmente
es fundamental la perfecta concienciación familiar, así como una vigilancia
estrecha de la agudeza visual del niño, que será la que marque el grado de
oclusión, mediante el test de visión preferencíal primero y con los optotipos
después, junto con una cuidadosa refracción. En las cataratas bilaterales, la
forma de ocluir irá marcada por la existencia o no de estrabismo y por lo que
nos indique la agudeza visual de cada ojo.
PRONÓSTICO
Cataratas infantiles monoculares
Los resultados visuales tras la cirugía de las cataratas monoculares, han
cambiado mucho en los últimos 20 años dependiendo sobre todo, de la
intervención precoz (antes de las 6-8 semanas) y del tratamiento y vigilancia
estrecha de la am bliopía, pero también del refinamiento tecnológico del
instrumental quirúrgico, y del desarrollo de nuevos materiales defensivos de la
integridad ocular, como es el hialuronidato sódico, o para la fabricación de
lentes de contacto y lentes intra-oculares, que han permitido mejorar
extraordinariamente las técnicas quirúrgicas y los resultados finales. Si la
catarata es congénita y completa en el momento del nacimiento y se opera antes
de la 6.ª semana, los resultados serán mejores que si se opera después de los
dos meses. Si la catarata congénita es parcial o se trata de una forma
adquirida los resultados serán mejores que si es completa. Si hay estrabismo,
lo que es frecuente, la catarata será muy ambliopigénica y los resultados
finales peores. En las cataratas traumáticas el pronostico dependerá, de que
otras estructuras se han lesionado.
Si la cirugía se realiza después del período crítico de desarrollo
visual, los pacientes con mejor pronóstico son: los que no tienen estrabismo y
los que padecen persistencia de vascularización fetal, lenticono posterior, o
catarata zonular (probablemente debidas al carácter progresivo de estas
opacidades).
Aunque nosotros somos partidarios de la cirugía con LIO, son muchos los que
siguen prefiriendo la lente de contacto. En una encuesta recogida por Wilson
(55) en 1994 entre 234 miembros del AAPOS (American association for pediatric
ophthalmology and strabimus) y 1039 miembros del ASCRS (American society of
cataract and refractive surgery), solo un 46% de los primeros y un 27% de los
segundos, ponen normalmente LIOs en niños, la mayor parte de ellos en mayores
de 6 años y nada más 16 de los AAPOS y 41 de los ASCRS, implantan LIOs en
niños menores de 2 años, y con esta edad son todavía menos los que lo hacen
en cataratas bilaterales. El 84% de los ASCRS emplean en la cápsula anterior
capsulorrexis, el 15% abre-latas y un 1% otros sistemas; el 50% de ellos hacen
capsulotomía posterior durante la cirugía, y dentro de estos el 38%
capsulorrexis. De los que hacen capsulotomía posterior intra-quirúrgica, el
38% la siguen haciendo después de los 5 años y el 8% después de los 12.
Francois en 1979, en 59 casos operados sin LIO, no consigue en ninguno de
ellos una visión superior a 0,1, mientras que Hiles en 1983 con LIO, consigue
más de 0,5 en el 17% de los casos. Sin embargo, si obtenemos una media entre un
conjunto de estadísticas con lente de contacto (66-70) y otras con LIO (71-74),
nos encontraremos con que se consigue una agudeza visual de 0,5 o mejor en el
21,4%, entre los primeros, y en el 4,5% entre los segundos, si bien es cierto
que la selección de aquéllas puede estar mediatizada por quien las elige.
Lo cierto es que cada día son más los autores que prefieren usar lentes
intraoculares en niños, en gran parte como resultado de la mejora en las
técnicas quirúrgicas, que han permitido disminuir el número y gravedad de las
complicaciones inherentes, a lo mal que tolera el ojo infantil estas lentes
(75-85).
Cataratas binoculares
Al igual que en las cataratas congénitas monoculares, en las bilaterales,
los mejores resultados se obtendrán cuando la cirugía y la rehabilitación
visual se instauran antes de los 2 meses de vida. Hay que tener en cuenta, que
una vez que se establece el nistagmos sensorial, el pronóstico visual será
pobre, y que la mayoría de los niños conseguirán visiones de 1/50 o peor,
mientras que en general, las cataratas bilaterales que se operan antes de los 2
meses de edad tienen un pronóstico visual bueno, logrando aproximadamente el
80% una visión de 1/2 o mejor. De todas formas, los niños con cataratas y
nistagmos también se deben operar, pues en muchos casos se consigue una
mejoría visual apreciable.
BIBLIOGRAFÍA
- Lambert SR, Drack AV. Infantile Cataracts. Surv Ophthalmol 1996; 40:
427-458.
- Bermejo E, Martínez-Frías M. Congenital eye malformations:
clinical-epidemiological analysis of 1,124,654 consecutive births in Spain. Am.
J. Med. Genet. 1998; 75: 497-504.
- Wiesel TN, Hubel PH. Effect of visual deprivation on morphology and
physiology of cells in the cats lateral geniculate body. Neurophisiol. 1963; 26:
978-978.
- von Noorden Comunicación personal 1978 (citado por François en:
François J. Late result of congenital cataracts surgery. Ophthalmology. 1979;
86: 1586-1598).
- von Noorden GK, Ryan SJ. Maumenee AE. Management of congenital cataracts.
Trans. Am. Acad. Ophthalmol. Otolaryngol. 1970; 74: 352-360.
- Davies PD, Tarbuck, DTH. Management of cataracts in infancy and childhood.
Trans. Ophthalmol. Soc. U.K. 1977; 97: 148-157.
- François J. Late result of congenital cataracts surgery. Ophthalmology.
1979; 86: 1586-1598.
- Hiles DA, Waller PH. visual results following infantile cataracts surgery.
Int. Ophthalmol.Clin 1977; 17: 265-282.
- Heveston EM, Saunders RA, Ellis FD. Unilateral cataracts in children.
Ophthalmic Surg. 1980; 11: 102-111.
- Enoch JM, Rabinowicz IM. Early surgery and visual correction of an infant
born with unilateral eye lens opacity. Doc. Ophthalmol. 1976; 41: 371-382.
- Pratt-Johnson JA, Tillson G. Visual result after removal of congenital
cataract before the age of one year. Can. J. Ophthalmol. 1981; 16: 19-20.
- Beller R, Hoyt CS, Marg E, Odom JV. Good visual function after neonatal
surgery for congenital cataracts. Am. J. Ophthalmol. 1981; 91: 559-565
- Rogers GL, Tishler CC, Tsous BH, and al. Visual acuity in infants with
congenital cataracts operated on prior to 6 months of age. Arch. Ophthalmol.
1981; 99: 999-1003.
- Wright KW, Wehrle MJ, Urrea PT. Bilateral total occlusion during the
critical period of visual development. Arch Ophthalmol. 1987; 105: 321-327.
- Chandler FC. Surgery of the lens in infancy and childhood Arch.
Ophthalmol 1951; 45: 125-138.
- Costenbader FD, Albert DG. Conservatism in the management of congenital
cataract Arch. Ophthalmol 1957; 58: 426-430.
- Scheie HG. Aspiration of congenital or soft cataracts. A new technique.
Am. J. Ophthalmol. 1960; 50: 1048-1056.
- McIntyre DJ. Coaxial cannula connector system. Cont and Intraoc. Lens.
Med. J. 1976; 2: 50.
- Gills JP, Loyd TL. Extracapsular cataract extraction with intraocular
lens insertion. J Am. Intraocul. Implant. Soc. 1979; 5: 9-12.
- Simcoe CW. Coaxial irrigating instruments J. Am. Intraocul. Implant. Soc.
1981; 7: 261-262.
- Simcoe CW. Double-barreled irrigation/aspiration unit. J. Am. Intraocul.
Implant. Soc. 1981; 7: 380.
- Parks MM. Management of posterior capsule in congenital cataract. J.
Pediatr. Ophthalmol. Strabismus. 1984; 21: 114-115.
- Peyman GA, Raichand M, Goldberg M F. Surgery of congenital and juvenile
cataract: a pars plicata approach with the vitrophage; British. J. Ophthalmol.
1978; 62: 780-783.
- Peyman GA, Raichand, M, Oesterle C, Goldberg MF. Pars plicata lensectomy
and vitrectomy in the management of congenital cataracts. Ophthalmology. 1981;
88: 437-439.
- Gimbel HV, DeBroff J. Posterior capsulorhexis with optic capture:
maintaining a clear visual axis after pediatric cataract surgery. Cataract.
Refract. Surg. 1994; 20: 658-64.
- Keech KV, Tongue AC, Scott WE. Complications after surgery for congenital
and infantile cataracts. Am J Ophthalmol. 1989; 108: 136-141.
- Phelps CD, Arafat NL. Open angle glaucoma following surgery for
congenital cataracts. Arch. Ophthalmol. 1977; 95: 1985-1987.
- Hing S, Speedwell L, Taylor D. Lens surgery in infancy and childhood. Br.
J. Ophthalmol. 1990; 74: 73-77.
- Jameson NA, Good WV, Hoyt CS. Inflammation after cataract surgery in
children Ophtlamic. Surg. 1992; 23: 99-102.
- Klais C M, Hattenbach LO, Steinkamp G W K, Zubcov AA, Kohnen T.
Intraocular recombinant tissue-plasminogen activator fibrinolysisf fibrin
formation after cataract surgery in children. J. Catarac. Refract. Surg. 1999
25: 357- 362.
- Chrousos GA, Parks MM, O’Neil JF. Incidence of chronic glaucoma,
retinal detachment, and secondary membrane surgery in pediatric aphakic
patients. Ophthalmology. 1984; 91: 1238-1241.
- Keech RV, Tongue AC, and Scott WE. Complications after surgery for
congenital and Infantile cataracts Am. J. Ophthalmol. 1989; 108:136-141.
- Egbert JE., Wright MM., Dahlhauser KF., Keithahn MZ., Letson RD, Summers
CG. A prospective study of ocular hypertension and glaucoma after pediatric
cataract surgery. Ophthalmology. 1995; 102: 1098-1101.
- Mills MD, and Robb R M., Glaucoma Following Childhood Cataract Surgery J.
Pediatr. Ophthalmol. Strabismus 1994; 31: 355-360.
- Asrani S, Freedman S, Hasselblad V, and all. Does primary intraoculár
lens implantation prevent «aphakic»glaucoma in children?. J. AAPOS, 2000; 4:
33-39.
- Lambert SR, Buckley EG, Plager DA, and all. Unilateral intraocular lens
implantation during the first six months of life. J. AAPOS, 2000; 3: 344-349.
- Gilbard SM, Peyman GA, Goldberg MF. Evaluation for cystoid maculopathy
after pars-plicata lensectomy- vitrectomy for congenital cataracts
Ophthalmology. 1983; 90:1201- 1206.
- Hoyt CS, NickeI B, Aphakie cystoid macular edema. Occurrence in Infants
and children after transpupillary lensectomy and Anterior Vitrectomy. Arch
Ophthalmol. 1982; 100: 746-749.
- Belmonte J, Taña P. Nuestra experiencia con implante de lentes
intraocularesde camara posterior en niños Arch. Soc. Españ. Oftalmol. 1993;
64: 343-358
- Peralta J, Abelairas J, Fonseca A. Pseudofaquia en niños complicaciones
en el postoperatorio precoz Arch. Soc. Esp. Oftalmol. 1996; 71: 583-590.
- Choyce DP. Correction of uni-ocular aphakia by means of anterior chamber
acrylic implants Trans. Ophthalmol.Soc.UK. 1958; 78: 459-470.
- Binkhorst CD, Gobin MH, Injuries to the eye with lens opacity in young
children. Ophthalmologica. 1964; 148: 169-183
- Binkhorst C D, Gobint MH. Treatrment o f congenital and juvenile cataract
with intraocular lens implants (pseudophakoi); Brit. J. Ophthal. 1970; 54:
759-765.
- Hiles DA. The need for lntraocular lens implantation in children,
Ophthalmic. Surgery. 1977; 8: 162-169.
- Hiles DA. Intraocular lens implantation in children with monocular
cataracts 1974-1983 Ophthamology. 1984; 91: 1231-1237.
- BenEzra D, And Paez JH. Congenital Cataract And Intraocular Lenses Am. J.
Ophthalmol. 1983; 96: 311-314.
- Hiles DA, Hered RW. Modern intraocular lens implants in children with new
age limitations. J Cataract Refract Surg. 1987; 13: 493-497.
- Sinskey RM, Karel F, Dal Ri E. Management of cataracts in children. J.
Cataract Refract. Surg. 1989; 15: 196-200.
- Dahan E,Brian D, Salmenson, Pseudophakia In Children: Precautions,
Technique, And Feasibility, J Cataract Refract Surg. 1990; 16: 75-82.
- Mackool RJ, Chhatiawala H. Pediatric cataract surgery and intraocular
lens Implantation: A new technique for preventing or excising postoperative
secondary membranes. J. Pediatr. Ophthalmol. Strabismus. J. Cataract Refract.
Surg. 1991; 17: 62-66.
- Gimbel HV, Ferensowiez M, Raanan M, DeLuca M. Implantation in Children;
J.Pediatr. Ophthalmol. Strabismus. 1993; 30: 69-79.
- Buckley EG, Klombers LA, Seaber J.H, Scalise-Gordy A, Minzter R.
Management of the posterior capsule during pediatric intraoular lens
implantation American Journal Of Ophthalmol. 1993; 115: 722-728.
- Atkinson CS, Hiles DA. Treatment of secondary posterior capsular
membranes with the ND:YAG laser in a pediatric population. Am. J. Ophtlamol.
1994; 118: 496-501.
- Neuhann T. Theorie und Operationstechnik der Kapsulorhexis. Clin.
Monastbl. Augenhildkd. 1987; 190:542-545.
- Gimbel HV, Neuhann T. Development, advantages, and methods of the
continuous circular capsulorhexis technique J. Cataract. Refract. Surg. 1990;
16: 31-37
- Zetterstróm C, Kugelberg U, Oscarson C. Cataract Surgery in children
with capsulorhexis of anterior and posterior capsules and heparin
surface-modified. J. Cataract. Refractive. Surg. 1994; 20: 599-601.
- Hing S, Speedwell L, Taylor D. Lens surgery in infancy and childhood.
Bri. J Ophthalmol. 1990; 74: 73-77.
- Gordon RA, Donzis PB. Refractive Development of the Human Eye Arch.
Ophthalmol. 1985; 103: 785-789.
- Wilson ME, Lall-Trail JK. Pseudophakia and polypseudophakia in three
first years of life. Communication personal. Symposium of ASCRS ACROS Boston may
2000.
- Awad AH, Mullaney PB, Al-Hamad A. David Wheeler, and all. Secondary
Posterior Chamber Intraocular Lens Implantation in Children. J. AAPOS 1998; 2:
269-274.
- Wilson ME, Englert JA, Greenwald MJ. In-the-bag secondary intraocular
lens Implantation in children. J: AAPOS: 1999; 3: 350-355.
- Zetterstróm C, Lundvall A, Weeber H, Jeeves M. Sulcus fixation without
capsular support in children. J. Cataract. Refract. Surg. 25: 1999; 777-781.
- Buckley EG. Scleral fixated (sutured) posterior chamber intraocular lens
implantation in children. J. AAPOS. 1999; 3: 289-294.
- Mittelviefhaus H, Mittelviefhaus K, Geriing J. Transscleral suture
fixation of posterior chamber intraocular lenses in children under 3 years.
Graefe`s Arch. Clin. Exp. Opgthalmo. l2000; 238: 143-148.
- Wilson ME, Bluestein EC. Wang X. Current trends in the use of intraocular
lenses in. children. Cataract Refract Surg. 1994; 20: 579-583.
- Birch EE, Stager, DR. Prevalence of good visual acuity following surgery
for congenital unilateral cataract. Arc. Ofhthalmol. 1988; 106:40-42.
- Birch EE, Swanson WH, Stager DR, and al. Outcome after very early
treatment of’ dense congenital unilateral cataract. Invest. Ophthalmol. Vis.
Sci. 1993; 34:3687-3698.
- Drummond CT, Scott WE, Keech RV: Management of monocular congenital
cataracts. Arch. Ophthalmol. 1989; 107: 5-51.
- Lorez B, Woj, Friedl N, Boergen KP. Monocular and binocular functional
result in cases of contact lens corrected infant aphakia, in Cotlier E, Lambert
SR Taylor D (eds): Congenital cataract. Boca Raton, Landers/CRC Press, FL 1994,
pp 151-162.
- Neumann D, Weissman BA, Isenberg SJ, and al: The effectiveness of daily
wear contact lenses for the correction of infantile aphakia. Arch. Ophthalmol.
1993; 111: 927-930.
- Burke JP, Willshaw HE, Young JDH. Intraocular lens implants for uniocular
cataract in childhood. Br.J.Ophthalmol. 1989; 73: 860-864.
- Dahan E, Salmenson BD. Pseudophakia in children: Precaution, thechnique,
and feasibility. J. Cataract. Refrac.Surg. 1990; 16: 75-82.
- Cheng KP, Hiles DA, Biglan AW, Pettapiece MC. Visual results after early
surgical treatment of unilateral congenital cataracts. Ophthalmology. 1991; 98:
903-910.
- Markham RHC, Bloom PA, Chandna A, Newcomb EH: Result of intraocular lens
implantation in pediatric aphakia. Eye 1992; 6: 493-498.
- Dahan E, Drusedau MUH. Choice of lens and dioptric power in peditatric
pseudophakia J. Cataract. Refract. Surg. 1997; 23: 618-623.
- Hamili MB, Koch DD. Pedíatric cataracts. Curr. Opin. Ophthalmol. 1999;
10: 4-9.
- Lambert SR, Management of monocular congenital cataracts. Eye. 1999; 13:
474-479.
- YoungTL, Bloom JM., Ruttum M, and all. The IOLAB, Inc Pediatric
Intraocular Lens Study. J.AAPOS 1999; 3: 295-302.
- Ahmadieh H, Javadi M, Ahmady M, and all. Primary capsulectomy, anterior
vitrectomy, lensectomy, and posterior chamber lens implantation in childrén:
Limbal versus pars plana J. Cataract. Refract. Surg. 1999; 25: 768-774.
- Pandey SK, Ram J, Werner L, Brar GS, and all. Result and postoperative
complication of capsular bag and sulcus fixation of posterior chamber
intraocular lenses in children with traumatic cataracts. J. Cataract. Refract.
Surg. 1999; 25: 1576-1584.
- Basti S, Aasuri MK, Reddy MK, Prectam P, and all.
Heparin-surface-modified intraocular lenses in pediatric cataract surgery:
prospective randoniized study.J. Cataract. Refract. Surg. 1999; 25: 782-787.
- Griener D, Dahan E, Lambert SR. Effect of age at time of cataract surgery
on axial length growth in infant eyes. J. Cateract. Refract. Surg. 1999; 25:
1209-1213.
- Pavlovic S, Jacobi FK, Graef M, Jacobi KW. Silicone intraocular lens
implantation in children: Preliminary results. J. Cataract. Refract. Surg. 1999;
26: 88-94.
- Dahán E. Intraocular lens ímplantation in children. Curr. Opin.
Ophthalmol. 2000; 11: 51-55.
- Onol M, Ozdek SC, Koksal M, Hasanreisoglu B. Pars plana lensectomy with
double-capsule-supported intraocular lens implantation in children. J. Cataract.
Refract. Surg. 2000; 26: 486-490.
|