|
INTRODUCCIÓN
El glaucoma pediátrico puede ser clasificado de muy diversos modos,
atendiendo a multitud de criterios. Con fines didácticos, nosotros preferimos
dividirlo en dos grandes grupos:
1. Glaucoma primario: Es el que aparece clínicamente aislado, constituyendo
una entidad por sí misma, sin unirse a otros síndromes ni a otras alteraciones
oculares, salvo la malformación trabecular que origina el cuadro y las
producidas como consecuencia de la hipertensión ocular. Este glaucoma se ha
denominado tradicionalmente «congénito» (1), aunque en determinados países
tiende a manifestarse en los primeros meses de vida, y está caracterizado por
una trabeculodisgenesia aislada en la clasificación etiopatogénica más
difundida actualmente, la de Hoskins (2).
2. Glaucoma secundario: Acompaña a otras malformaciones o alteraciones
oculares, entre las que destacan:
- Determinados síndromes con afectación multiorgánica como la aniridia,
el síndrome de Axenfeld-Rieger, la anomalía de Peters tipo I y II, el
síndrome de Lowe, el de Nance-Horan, el de Sturge-Weber, las neurofibromatosis.
- Glaucomas que complican la evolución de determinados cuadros
vitreorretinianos como la retinopatía del prematuro (RP), las displasias
vitreorretinianas (Norrie) o la Persistencia de la Vasculatura Fetal (PVF),
conduciendo al bloqueo angular por desplazamiento del diafragma
irido-cristaliniano.
- Glaucomas neovasculares como estadío final del desprendimiento retiniano
de larga evolución, bien postraumático, bien secundario a alteraciones tales
como la Vitreorretinopatía Exudativa Familiar (VREF), la enfermedad de Coats, o
ciertos tumores como los hemangiomas capilares retinianos, el retinoblastoma y
el meduloepitelioma.
- Glaucomas secundarios a uveítis, por ángulo cerrado (sinequias
iridianas posteriores y anteriores periféricas) o abierto (cortisónico,
trabeculitis), que se ven principalmente en la Iridociclitis Crónica Juvenil y
en la uveítis intermedia.
- Glaucomas secundarios a la cirugía, particularmente a la de la catarata
congénita, pudiendo tratarse bien de ángulos abiertos (cataratas nucleares en
ojos microftálmicos), o bien cerrados (sinequias iridianas
posteriores/anteriores periféricas).
- Glaucomas por malposición cristaliniana, generalmente producidos por
bloqueo pupilar y asociados a síndrome de Weill-Marchesani, Marfan u
homocistinuria.
- Glaucomas asociados a tumores iridianos, como el xantogranuloma juvenil y
la leucemia.
- Glaucomas postraumáticos complicando hifemas y generalmente asociados a
una recesión angular.
Debe recordarse que ciertos glaucomas pediátricos secundarios pueden hacerse
patentes al nacimiento, por lo que son, stricto sensu, «congénitos».
Para intentar reducir el confusionismo existente, denominaremos al primer
grupo como glaucoma congénito primario (GCP). Este tipo de glaucoma merece un
comentario aparte.
APROXIMACIÓN AL GLAUCOMA
CONGÉNITO PRIMARIO
Es el glaucoma pediátrico más prevalente (3), y aunque en ciertos lugares
tiende a aparecer en los primeros meses de vida (4), en España tiende a
presentarse al nacimiento, según experiencia propia. Esto parece tener una
importancia terapéutica fundamental, como se discutirá posteriormente.
Las contribuciones principales al conocimiento de la etiopatogenia del GCP se
deben a los avances quirúrgicos. A finales del siglo XIX Tailor (5) y De
Vicentiis (6) introdujeron una novedosa técnica quirúrgica para tratar el
glaucoma del adulto: La goniotomía. El procedimiento no ofreció buenos
resultados pero, modificada posteriormente por Barkan (7), supuso un cambio
radical en el tratamiento y pronóstico del GCP. La eficacia de la goniotomía
en el tratamiento del GCP ha quedado avalada (8-10), atribuyendo Barkan (11) y
Worst (12) su mecanismo de acción a la sección de una delgada membrana
(«membrana de Barkan») que tapizaba la superficie trabecular. No ha podido
demostrarse en ningún caso la existencia de dicha membrana. Anderson, en
estudios anatomopatológicos, llegó a la conclusión de que el trabeculum del
GCP es similar al de un feto de 7-8 meses de gestación, encontrándose las
láminas trabeculares comprimidas por esta detención en el desarrollo (13). La
sección del trabeculum en la goniotomía permitiría su expansión y
permeabilización (figura 1).
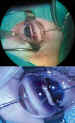
Figura 1a. Goniotomía clásica con lente de Worst.
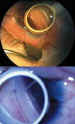
Figura 1b. Goniotomía clásica con lente de Swan-Jacob.
Smith (14) y Burian (15,16) descubrieron que la resistencia trabecular
también podía vencerse mediante la trabeculotomía ab externo, con un acceso a
través de la esclera al canal de Schlemm, que era seccionado junto al
trabeculum. Esta técnica pronto ganaría numerosos adeptos (17-19).
Se considera que las dos técnicas son igualmente efectivas (20), si bien
cada una tiene sus propios defensores (10,21). La goniotomía es un abordaje ab
interno que requiere una córnea transparente y un entrenamiento especializado
por parte del cirujano y sus ayudantes. Quizá por ello gana cierta preferencia
la trabeculotomía en la actualidad como tratamiento inicial del GCP (22-23),
bien como procedimiento exclusivo, bien unida a la trabeculectomía (24-26).
No obstante, Shaffer, estudiando durante varios años 287 ojos sometidos a
goniotomía (27), concluyó que los resultados finales vienen condicionados por
el momento del inicio de la clínica. Si el glaucoma pediátrico primario debuta
entre el mes y los 24 meses de vida, el éxito del procedimiento alcanza el 90%
—glaucoma «infantil» (25)—. Si debuta antes del mes —«congénito»— o
después de los 24 meses —«juvenil»—, el éxito sólo llega al 30%. Estos
resultados llevaron a Hoskins a proponer una clasificación anatómica del GCP
(2) que pudiera explicar la disparidad de resultados de la goniotomía según el
grado de malformación existente. Distingue entre:
- Trabeculodisgenesia aislada, según el concepto de trabeculum fetal de
Anderson, que responde a la goniotomía y trabeculotomía con elevado porcentaje
de éxitos.
- Iridotrabeculodisgenesia: Se asocian hipoplasia del estroma iridiano
anterior y generalmente vasos iridianos anómalos. Son ojos con córneas opacas
presentes al nacimiento y con PIOs muy elevadas. La respuesta a gonio y
trabeculotomía es pobre.
- Corneotrabeculodisgenesia: Agrupa a alteraciones concomitantes de la
córnea periférica (síndrome de Axenfeld-Rieger) o central (anomalía de
Peters). La respuesta a gonio y trabeculotomía es pobre.
Luntz (28) cree que el procedimiento indicado en estos dos últimos grupos es
la cirugía filtrante, pudiendo también recomendarse las válvulas de
derivación para el glaucoma. Parece, entonces, que la indicación quirúrgica
en el GCP puede venir determinada por ciertos hallazgos clínicos e
intraoperatorios.
INDICACIONES DE LOS DIFERENTES
PROCEDIMIENTOS QUIRÚRGICOS
A continuación se ofrece un algoritmo aproximativo al tratamiento del
glaucoma pediátrico en sus variantes más prevalentes. Glaucoma hace referencia
aquí a una hipertensión intraocular mantenida, independientemente del daño
papilar asociado. Este algoritmo está basado en la práctica clínica diaria y
pretende reflejar nuestra experiencia quirúrgica en el Hospital La Paz de
Madrid.
1. Glaucoma congénito primario (GCP) (figura 2): El tratamiento
inicial viene condicionado por la transparencia corneal y los hallazgos
gonioscópicos, como ha quedado expuesto previamente. SI LA OPACIDAD CORNEAL
IMPIDE VISUALIZAR LOS DETALLES DEL TRABECULUM, INCLUSO TRAS
DESEPITELIZACIÓN, NO ESTÁ INDICADA LA GONIOTOMÍA, que puede suponer un
daño yatrogénico severo. Si la gonioscopia revela malformaciones iridianas
asociadas, generalmente unidas a un «ángulo cicatricial» (28), puede ser más
recomendable la cirugía combinada ab externo (trabeculectomía más
trabeculotomía). En raras ocasiones practicamos trabeculotomía aislada. El
fracaso del procedimiento empleado dictará una nueva indicación quirúrgica.
La goniotomía pierde eficacia en las repeticiones (1); la trabeculectomía
repetida compromete decisivamente nuevas trabeculectomías al producirse una
cicatrización de los tejidos epiesclerales. La solución puede estar en el
empleo de antimitóticos o, como método más seguro y eficaz, un dispositivo de
derivación para el glaucoma. Nosotros empleamos la Válvula de Ahmed para el
Glaucoma (VAG).

Figura 2. Algoritmo para el tratamiento del GCP.
GCP: Glaucoma Congénito Primario; Trabeculod: Trabeculodisgenesia;
Iridotrabeculod: Iridotrabeculodisgenesia; TE: Trabeculectomía; TT:
Trabeculotomía: GT: Goniotomía; VAG: Válvula de Ahmed para el Glaucoma.
2. Glaucoma asociado con la aniridia (figura 3): El mecanismo de
glaucoma parece ser la aposición de primordios iridianos al trabeculum (29). Se
considera que el glaucoma en la aniridia es difícil de controlar, por lo que
Walton aboga por una profilaxis mediante goniotomía (29,30). Si se desarrolla
el glaucoma, se trata médicamente y, si debe intervenirse, el tratamiento que
parece más eficaz es la trabeculotomía (31,32). Tanto en la gonio como en la
trabeculotomía el riesgo de lesionar el cristalino es elevado, por lo que se
puede valorar una trabeculectomía inicialmente o VAG (33).
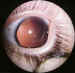
Figura 3. Aniridia congénita.
3. Glaucoma asociado con el síndrome de Axenfeld-Rieger (figura 4):
Se atribuye a una detención del desarrollo angular con mantenimiento del
endotelio primordial (34,35), asociándose en los casos más severos una
hipoplasia del canal de Schlemm (36). Estos ojos pueden manifestar un glaucoma
connatal, y el tratamiento preferible es la trabeculectomía o VAG. Si el debut
se produce en la infancia o adolescencia, se comienza por el tratamiento
médico. Si no se controla adecuadamente, se procede a trabeculectomía,
preferiblemente asociada a antimetabolitos (37) o VAG.
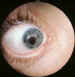
Figura 4. Síndrome de Axenfeld-Rieger.
4. Glaucoma asociado con la anomalía de Peters (figura 5):
Parece que la alteración subyacente es un prematuro envejecimiento trabecular
(38). El glaucoma puede presentarse al nacimiento o más adelante (1), y
frecuentemente se relaciona con la queratoplastia penetrante (39,40). El
glaucoma connatal se tratará quirúrgicamente, principalmente mediante
trabeculectomía (41) o una válvula (28). Si aparece en los primeros años de
vida o tras queratoplastia, puede intentarse el tratamiento médico primero,
aunque con gran probabilidad requiera cirugía en algún momento, aplicándose
las indicaciones previas.
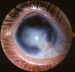
Figura 5. Anomalía de Peters.
5. Glaucoma asociado con el síndrome de Sturge-Weber (figura 6) —y
anomalías relacionadas, como el síndrome de Klippel-Trenaunay-Weber (41) y el
«cutis marmorata telangiectatica congenita» (1)—. Parece que el glaucoma
connatal se relaciona con una trabeculodisgenesia (41). El desarrollado más
tardíamente se debería a una presión epiescleral elevada (42). Es conocida la
frecuencia de complicaciones secundarias a la cirugía filtrante en el
Sturge-Weber, particularmente la hemorragia coroidea expulsiva y el
desprendimiento coroideo (43), atribuibles ambos a una presión epiescleral
elevada (41,42). Si existe un glaucoma connatal, frecuentemente con ojo
buftálmico, es recomendable practicar una gonioscopia intraoperatoria y
realizar goniotomía si existen indicios de trabeculodisgenesia. Varios autores
consideran de elección combinar trabeculotomía con trabeculectomía en la
cirugía de este síndrome (44,45), preferentemente en el glaucoma neonatal
(46). Si el glaucoma aparece más tardíamente, se puede plantear inicialmente
el tratamiento médico. Si no es suficiente, se valorará la trabeculectomía,
generalmente unida a esclerotomías posteriores profilácticas con el fin de
minimizar las complicaciones asociadas a desprendimientos coroideos (47), aunque
recomendamos la VAG por su notable eficacia en la prevención de dichas
complicaciones y facilidad de manejo (48).
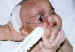
Figura 6. Síndrome de Sturge-Weber.
6. Glaucoma asociado con la neurofibromatosis: Presenta también dos
tipos de glaucoma. En el connatal parece existir una detención del desarrollo
trabecular (1). En el glaucoma tardío se produce una compresión trabecular por
tejido uveal hamartomatoso (41). Por tanto, en el glaucoma precoz se pueden
aplicar las mismas técnicas que en el GCP tras realizar gonioscopia y comprobar
la presencia de trabeculodisgenesia. En el tardío se comienza por el
tratamiento médico y, si es insuficiente, se plantea trabeculectomía o VAG.
7. Glaucoma asociado con síndrome de Lowe (figura 7): El
síndrome oculocerebrorrenal de Lowe, de herencia ligada al sexo, se caracteriza
oftalmológicamente por cataratas (100% de los casos) y un glaucoma
aproximadamente en el 70% de los niños, de etiología idiopática y de difícil
control (49). Pueden plantearse todas las técnicas quirúrgicas pero, al ser
frecuentemente afáquicos, es muy recomendable la VAG.

Figura 7. Síndrome de Lowe.
8. Glaucomas de ángulo cerrado secundarios. Se pueden agrupar
principalmente en:
A. Secundarios a alteraciones vitreorretinianas como la Retinopatía
del Prematuro (RP) avanzada, la Persistencia de la Vasculatura Fetal (PVF) y las
displasias vitreorretinianas. La intervención precoz puede impedir estas
complicaciones en la RP (50-52) y en la PVF (53), llegando a establecer
resultados funcionales en las dos entidades (50-53). En los casos avanzados el
glaucoma se produce por desplazamiento del diafragma iridocristaliniano, bien
por el desprendimiento retiniano completo de los grados 5 de RP o bien por la
tracción ejercida por la PVF asociada o no a catarata intumescente (49). Si no
existe posibilidad visual se procede a lensectomía más iridectomía. Es
conveniente practicar gonioscopia: Si se evidencian sinequias anteriores
periféricas (SAP) se puede asociar una goniosinequialisis (cuando se cree que
la evolución del proceso es corta), e incluso pensar en trabeculectomía o VAG
cuando existe algún resto visual. Muchos de estos ojos están abocados a la
atrofia dada su grave desestructuración (figura 8).
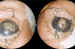
Figura 8. Grado 5 de RP con glaucoma de ángulo cerrado.
B. Secundarios a uveítis (principalmente la Iridociclitis Crónica
Juvenil): Son raros y se producen por sinequias iridianas posteriores. Se puede
proceder a iridectomía, aunque por lo general desarrollarán otros problemas
como cataratas y glaucomas crónicos de ángulo abierto.
C. Secundarios a cirugía intraocular previa (generalmente de la
catarata): Pueden complicar todas las técnicas, pero es más frecuente verlos
tras extracciones extracapsulares de las cataratas con/sin capsulotomía
posterior y de deben a sinequias iridianas a restos capsulares o a hialoides.
Cuando se diagnostica el problema generalmente no es efectiva la iridectomía
aislada, por presencia de sinequias anteriores. Recomendamos practicar
iridectomía periférica, sinequiotomías posteriores, vitrectomía si existe
vítreo en cámara anterior y gonioscopia intraoperatoria: Si se confirman
sinequias anteriores periféricas en más de 180° de circunferencia,
recomendamos intento de goniosinequialisis, que puede ser efectiva si la
evolución del proceso es inferior al año (54). Si existen dudas acerca de la
necesidad de cirugía filtrante, recomendamos VAG.
El glaucoma en la queratoplastia penetrante pediátrica se asocia a
anomalías angulares congénitas y/o a SAP. Se previene y trata principalmente
mediante VAG. Temporalmente puede emplearse tratamiento médico.
D. Glaucomas neovasculares evolucionados: Complican los procesos
isquémicos y/o desprendimientos retinianos de larga evolución —p.e. la
Vitreorretinopatía Exudativa Familiar (VREF) (55)— y también a ciertos
tumores, particularmente el retinoblastoma y el meduloepitelioma (56,57). En el
caso de las retinopatías se puede intentar un tratamiento precoz como la
panfotocoagulación en una retinopatía con isquemia periférica asociada a
Incontinentia Pigmenti o una VREF, o bien proceder a un vitrectomía si existe
ya un desprendimiento retiniano. En los tumores infantiles se considera que la
presencia de un glaucoma es sinónimo de enucleación (56).
E. Secundarios a dislocación cristaliniana: Puede ser de origen
traumático o bien asociada a síndromes típicos como el Weill-Marchesani o el
Marfan (58). El glaucoma se produce por bloqueo pupilar ocasionado por el
cristalino en su desplazamiento, pudiendo estar indicada la iridectomía (59).
Sin embargo, parece más lógico actualmente prevenir otras posibles
complicaciones mediante la lensectomía y vitrectomía (no se puede conservar la
cápsula cristaliniana), asociando generalmente iridectomía.
9. Glaucomas de ángulo abierto secundarios: Se pueden agrupar
principalmente en:
A. Secundarios a uveítis: El origen de una hipertensión intraocular
crónica frecuentemente es especulativo, pero parece relacionarse con un daño
trabecular producido por células y mediadores inflamatorios, así como por los
corticoides utilizados en la terapia de estas patologías. Este tipo de
glaucomas se ven principalmente en la Iridociclitis Crónica Juvenil, asociada o
no a artritis, y en la uveítis intermedia (pars planitis). Si la hipertensión
no se controla adecuadamente con tratamiento médico se puede intentar la
trabeculodiálisis, técnica derivada de la goniotomía (60), aunque
recomendamos vivamente el uso de la VAG (61).
B. Secundarios a cirugía intraocular previa: Suele ser más frecuente
tras cirugía de cataratas nucleares en ojos microftálmicos, sin que se haya
dilucidado el mecanismo último (62). Se presenta generalmente en la
adolescencia o juventud. Si no se controla adecuadamente con tratamiento médico
se puede intentar trabeculectomía, aunque recomendamos VAG.
C. Glaucomas asociados a tumores iridianos. Se dan principalmente en
dos entidades:
• Xantogranuloma juvenil (figura 9) (63): Tumor de células
histiocitarias de tipo no-Langerhans, cuando se localiza en el iris se
caracteriza por originar hifemas espontáneos con hipertensión intraocular. Se
trata mediante corticoterapia tópica-periocular-sistémica, asociando
medicación antiglaucomatosa. En raras ocasiones debe recurrirse a la
radioterapia externa, a dosis bajas.

Figura 9. Xantogranuloma juvenil.
• Leucemias, típicamente en una recurrencia (64): Tiende a
presentarse como una masa iridiana asociada a signos inflamatorios, hipopión
gris e hipertensión intraocular. El tratamiento consiste en corticoterapia
tópica-periocular y medicación antiglaucomatosa, si bien debe reinducirse la
quimioterapia y se asocia radioterapia externa en el ojo afecto, a razón de
unos 3.000 cGy.
D. Glaucomas asociados a traumatismos oculares: Es muy frecuente y
conocida la hipertensión intraocular asociada a hifemas, generalmente de gran
tamaño y/o resangrados, pudiendo requerir el lavado de cámara anterior por
este motivo. El glaucoma crónico postraumático parece íntimamente
correlacionado con la extensión de la recesión angular (65) y es especialmente
resistente al tratamiento médico. Recomendamos el empleo de VAG.
BIBLIOGRAFÍA
- Russell-Eggitt. Childhood glaucoma. In Taylor D ed: Paediatric
Ophthalmology. London: Blackwell Science; 1997; 477-497.
- Hoskins HD Jr, Shaffer RN, Hetherington J. Anatomical classification of
developmental glaucomas. Arch Ophthalmol 1984; 102: 1.331-1.334.
- Miller SJH. Genetic aspects of glaucoma. Trans Ophthalmol Soc UK 1962; 81:
425-434.
- Morin JD, Merin S, Sheppard RW. Primary congenital glaucoma; a survey.
Canad J Ophthalmol 1974; 9: 17-22.
- Tailor U. Sulla incisione dell´angolo irideo (contribuzione alla cura del
glaucoma). Ann Ottalmol 1891; 20: 117-127.
- De Vicentiis C. Sulla cosidetta «sclerotomia» interna. In: Lavori della
Clinica Oculistica dell´Università di Napoli. Napoli: Pasquale V, 1894-1896;
227-235.
- Barkan O. Technic of goniotomy. Arch Ophthalmol 1938; 19: 217-223.
- Rice NSC. The surgical management of the congenital glaucomas. Aust J
Ophthalmol 1977; 5: 174-179.
- Draeger J, Wirt H, Ahrens V. Long-term results following goniotomy in
congenital glaucoma. Klin Monatsbl Augenheilkd 1984; 185: 481-489.
- Russell-Eggitt MI, Rice NS, Jay B, Wyse RK. Relapse following goniotomy
for congenital glaucoma due to trabecular dysgenesis. Eye 1992; 6: 197-200.
- Barkan O. Pathogenesis of congenital glaucoma: gonioscopic and anatomic
observations of the anterior chamber in the normal eye and in congenital
glaucoma. Am J Ophthalmol 1955; 40: 1-15.
- Worst JG. Congenital glaucoma. Remarks on the aspect of chamber angle,
ontogenic and pathogenetic background, and mode of action of goniotomy. Invest
Ophthalmol 1968; 7: 127-134.
- Anderson DR. The development of the trabecular meshwork and its
abnormality in primary infantile glaucoma. Trans AM Ophthalmol Soc 1981; 79:
458-485.
- Smith R. A new technique for opening the canal of Schlemm. Preliminary
report. Br J Opthalmol 1960; 44: 370-373.
- Burian HM. A case of Marfan´s syndrome with bilateral glaucoma with a
description of a new type of operation for developmental glaucoma (trabeculotomy
ab externo). Am J Ophthalmol 1960; 50: 1.187-1.192.
- Burian HM, Allen L. Trabeculotomy ab externo. A new glaucoma operation:
Technique and results of experimental surgery. Am J Ophthalmol 1962; 53: 19-26.
- Mc Pherson SD Jr. Results of external trabeculotomy. Am J Ophthalmol
1973; 76: 918-920.
- Mc Pherson SD Jr, Mc Farland D. External trabeculotomy for developmental
glaucoma. Ophthal-mology 1980; 87: 302-305.
- Luntz MH. Primary buphthalmos (infantile glaucoma) treated by
trabeculotomy ab externo. S Afr Arch Ophthalmol 1974; 2: 319-333.
- Anderson DR. Trabeculotomy compared to goniotomy for glaucoma in
children. Ophthalmology 1983; 90: 805-806.
- Luntz MH. The advantages of trabeculotomy over goniotomy. J Pediatr
Ophthalmol Strabismus 1984; 21: 150-153.
- Wada Y, Nakatsu A, Kondo T. Long-term results of trabeculotomy ab
externo. Ophthalmic Surg 1994; 25: 317-320.
- Meyer G, Schwenn O, Pfeiffer N, Grehn F. Trabeculotomy in congenital
glaucoma. Graefes Arch Clin Exp Ophthalmol 2000; 238: 207-213.
- Elder MJ. Combined trabeculotomy-trabeculectomy compared with primary
trabeculectomy for congenital glaucoma. Br J Opthalmol 1994; 78: 745-748.
- Mandal AK, Naduvilath TJ, Jayagandan A. Surgical results of combined
trabeculotomy-trabeculectomy for developmental glaucoma. Ophthalmology 1998;
105: 974-982.
- Mullaney PB, Selleck LVN, Al-Awad A, Al-Mesfer S, Zwann J. Combined
trabeculotomy and trabeculectomy as an initial procedure in uncomplicated
congenital glaucoma. Arch Ophthalmol 1999; 117: 457-460.
- Shaffer RN. Prognosis of goniotomy in primary infantile glaucoma
(trabeculodysgenesis). Trans Am Ophthalmol Soc 1982; 80: 321-325.
- Luntz MH, Harrison R. Surgery for congenital glaucoma. In: Ritch R,
Shields MB, Krupin T eds. The glaucomas. St Louis: Mosby; 1996; vol. III:
1.761-1.781.
- Walton DS. Aniridic glaucoma: the results of gonio-surgery to prevent and
treat this problem. Trans Am Ophthalmol Soc 1986; 84: 59-70.
- Chen TC, Walton DS. Goniosurgery for prevention of aniridic glaucoma.
Arch Ophthalmol 1999; 117: 1.144-1.148.
- Hoskins HD Jr, Shaffer RN, Hetherington J. Goniotomy vs trabeculotomy. J
Pediatr Ophthalmol Strabismus 1984; 21: 153-158.
- Adachi M, Dickens CJ, Hetherington J Jr, Hoskins HD Jr, Iwach AG, Wong
PC, Nguyen N, Ma AS. Clinical experience of trabeculotomy for the surgical
treatment of aniridic glaucoma. Ophthalmology 1997; 104: 2.121-2.125.
- Wiggings R, Tomey K. The results of glaucoma surgery in aniridia. Arch
Ophthalmol 1992; 110: 503-505.
- Shields MB. Axenfeld-Rieger syndrome: a theory of mechanism and
distinctions from the iridocorneal endothelial syndrome. Trans Am Ophthalmol Soc
1983; 81: 736-784.
- Shields MB, Buckley E, Klintword GK, Tresher R. Axenfeld-Rieger syndrome.
A spectrum of developmental disorders. Surv Ophthalmol 1985; 29: 387-409.
- Shields MB. Axenfeld-Rieger syndrome. In: Ritch R, Shields MB, Krupin T
eds. The glaucomas. St Louis: Mosby; 1996; vol. III: 875-885.
- Mandal AK, Prasad K, Naduvilath TJ. Surgical results and complications of
mitomycin C-augmented trabeculectomy in refractory developmental glaucoma.
Ophthalmic Surg Lasers 1999; 30: 473-480.
- Heath DH, Shields MB. Glaucoma and Peters´ anomaly. A clinicopathologic
case report. Graefes Arch Clin Esp Ophthalmol 1991; 229: 277-280.
- Parmley VC, Stonecipher KG, Rowsey JJ. Peters´ anomaly: A review of 26
penetrating keratoplasties in infants. Ophthalmic Surg 1993; 24: 31-35.
- Althaus C, Sundmacher R. Keratoplasty in newborns with Peters' anomaly.
Ger J Ophthalmol 1996; 5: 31-35.
- Weiss JS, Ritch R. Glaucoma in the phakomatoses. In: Ritch R, Shields MB,
Krupin T eds. The glaucomas. St Louis: Mosby; 1996; vol. II: 899-924.
- Jorgensen JS, Guthoff R. Sturge-Weber syndrome: glaucoma with elevated
episcleral venous pressure. Klin Monatsbl Augenheilkd 1987; 191: 275-278.
- Theodossiadis G, Damanakis A, Koutsandrea C. Choroid effusion in an
antiglaucoma operation in a child with Sturge-Weber syndrome. Klin Monatsbl
Augenheilkd 1985; 186: 300-302.
- Board RJ, Shields MB. Combined trabeculotomy-trabeculectomy for the
management of glaucoma associated with Sturge-Weber syndrome. Ophthalmic Surg
1981; 12: 813-817.
- Agarwal HC, Sandramouli S, Sihota R, Sood NN. Sturge-Weber syndrome:
management of glaucoma with combined trabeculotomy and trabeculectomy.
Ophthalmic Surg 1993; 24: 399-402.
- Mandal AK. Primary combined trabeculotomy- trabeculectomy for early-onset
glaucoma in Sturge-Weber syndrome. Ophthalmology 1999; 106: 1.621-1.627.
- Lytle RA, Thomas JV, Simmons RJ. Glaucoma surgical techniques in eyes
with enlarged epiescleral vessels. In: Thomas JV ed. Glaucoma surgery. St Louis:
Mosby-Year Book; 1992; 235-243.
- Hamush NG, Coleman AL, Wilson MR. Ahmed glaucoma valve implant for the
management of glaucoma in Sturge-Weber syndrome. Am J Ophthalmol 1999; 128:
758-760.
- Cantor LB. Glaucoma associated with congenital disorders. In: Ritch R,
Shields MB, Krupin T eds. The glaucomas. St Louis: Mosby; 1996; vol. II:
925-954.
- Cryotherapy for Retinopathy of Prematurity Cooperative Group. Multicenter
Trial of Cryotherapy for Retinopathy of Prematurity: Snellen visual acuity and
structural outcome at 51/2 years after randomization. Arch Ophthalmol 1996; 114:
417-424.
- White JE, Repka MX. Randomized comparison of diode laser photocoagulation
versus cryotherapy for threshold retinopathy of prematurity: 3-year outcome. J
Pediatr Ophthalmol Strabismus 1997; 34: 83-87.
- Trese MT, Droste PJ. Long-term postoperative results of a consecutive
series of stages 4 and 5 retinopathy of prematurity. Ophthalmology 1998; 105:
992-997.
- Dass AB, Trese MT. Surgical results of Persistent Hyperplastic Primary
Vitreous. Ophthalmology 1999; 106: 280-284.
- Sharpe ED, Thomas JV, Simmons RJ. Goniosynechialysis. In: Thomas JV ed.
Glaucoma surgery. St Louis: Mosby-Year Book; 1992; 245-249.
- Pendergast SD, Trese MT. Familial Exudative Vitreoretinopathy. Results of
surgical treatment. Ophthalmology 1998;105: 1.015-1.023.
- Shields JA, Shields C, Shields MB. Glaucoma associated with intraocular
tumors. In: Ritch R, Shields MB, Krupin T eds. The glaucomas. St Louis: Mosby;
1996; vol. II: 1.131-1.139.
- Shields JA, Eagle RC, Shields C, De Potter P. Congenital neoplasm of the
nonpigmented ciliary epithelium (medulloepithelioma). Ophthalmology 1996; 103:
1.998-2.006.
- Lambert S. Lens. In Taylor D ed: Paediatric Ophthalmology. London:
Blackwell Science; 1997; 445-476.
- Liebmann JM, Ritch R. Glaucoma assiciated with lens intumescence and
dislocation. In: Ritch R, Shields MB, Krupin T eds. The glaucomas. St Louis:
Mosby; 1996; vol. II: 1.033-1.053.
- Hoskins DH Jr, Kass M. Becker - Shaffers´ diagnosis and therapy of the
glaucomas. 6.ª ed. St Louis: Mosby; 1989; 616.
- Da Mata A, Burk SE, Netland PA, Baltatzis S, Chisten W, Foster CS.
Management of uveitic glaucoma with Ahmed glaucoma valve implantation.
Ophthalmology 1999; 2.168-2.172.
- Johnson DA, Parks MM. Cataracts in childhood: Prognosis and
complications. Semin Ophthalmol 1991; 6: 201-211.
- Lyons C, Rootman J. Histiocytic, haematopoietic and lymphoproliferative
disorders. In Taylor D ed: Paediatric Ophthalmology. London: Blackwell Science;
1997; 356-365.
- Taylor D. Leukaemia. In Taylor D ed: Paediatric Ophthalmology. London:
Blackwell Science; 1997; 816-827.
- Mermoud A, Heuer DK. Glaucoma associated with trauma. In: Ritch R,
Shields MB, Krupin T eds. The glaucomas. St Louis: Mosby; 1996; vol. II:
1.259-1.275.
|