|
INTRODUCCIÓN
La ptosis o posición extremadamente baja del párpado superior, puede ser
congénita o adquirida. En la edad infantil la mayoría son congénitas y por
tanto presentes desde el nacimiento.
ANATOMÍA
Los músculos elevadores del párpado superior son:
1. El músculo elevador del párpado superior (inervación voluntaria por el
III par craneal): es el más importante en la excursión palpebral.
2. El músculo de Müller (inervación simpática): solamente aporta una
excursión máxima de 4 mm.
Como músculo antagonista está el músculo orbicular.
CLASIFICACIÓN DE LAS PTOSIS CONGÉNITAS
1. Ptosis congénita simple. Son las más frecuentes y pueden ser
unilaterales (80%) o bilaterales (20%). No mejoran con el paso del tiempo y
suelen tener antecedentes familiares. Histológicamente se aprecia una atrofia
del músculo elevador, que en los casos más graves puede estar totalmente
fibrosado. Muchos síndromes presentan ptosis palpebrales dentro de su contexto:
Displasia craneocarpatotarsal, Displasia frontonasal...
2. Síndrome de Blefarofimosis. Es una anomalía órbitopalpebral
congénita que se asocia a ptosis bilateral, hendidura palpebral horizontalmente
estrecha, telecanto, aplanamiento del dorso nasal y epicanto. La órbita
morfológicamente es anómala, al tener el eje vertical mayor que el horizontal.
El músculo orbicular supraadyacente a la órbita presenta, por tanto, un
disposición anatómica alterada. En la parte medial sobrepasa el canto interno,
originando el epicanto muscular (epiblefaro). Los casos severos presentan
hipertelorismo leve.
Callahan (1974) (1) clasificó las blefarofimosis en tres tipos: TIPO I:
con epicantus inversus, ptosis y hendidura palpebral transversal disminuída. TIPO
II: con telecanto sin epicanto, ptosis y deficiencia de piel en los cuatro
párpados. TIPO III: es como el tipo II, pero además presenta hendidura
antimongoloide y ligero hipertelorismo.
Algunas veces se asocia a otras anomalías aisladas: auriculares, frontales,
óseas, artrogriposis, infertilidad, pubertad tardía, microcefalia, retraso
mental, etc. o como una entidad dentro de síndromes específicos (S. De
Schwartz-Jampel, S. De Simosa, S. De Ohdo, S. De Midas, S. de Young-Simpson, S.
De Michels, S. De Marden-Walker, S. De Dubowitz, etc.)
La mayoría de los casos son esporádicos, y en un porcentaje menor se ha
encontrado relación familiar con un patrón hereditario autosómico dominante.
Los estudios genéticos han revelado alteraciones en el cromosoma 3q23, 13 y 16.
Se debe hacer diagnóstico diferencial con: epicanto cutáneo, telecanto
óseo, hipertelorismo y el Síndrome de Waardenburg.
3. Ptosis sincinéticas. Se producen por una inervación anómala del
músculo elevador.
La más frecuente es la de Marcus Gunn. Consiste en la inervación por parte
del V par craneal del músculo elevador con lo cual el párpado ptósico se eleva
al contraer los músculos pterigoi deos, inervados por este mismo nervio
(ejemplo: al abrir la boca o masticar). Pueden mejorar con el paso del tiempo.
Tienen tendencia familiar y se puede confirmar el diagnóstico con
electromiografía (figura 1).

Figura 1. Ptosis de Marcus-Gunn que se corrige al abrir la boca.
CLASIFICACIÓN DE LAS PTOSIS ADQUIRIDAS EN LA INFANCIA
En la edad infantil son menos frecuentes que las congénitas. Pueden ser:
1. Neurógenas.
Por afectación del tercer nervio craneal o la cadena
neuronal simpática (síndrome de Horner). En nuestro hospital los traumatismos
del techo orbitario son la causa más frecuente de ptosis neurógenas.
2. Miogénicas. Por miastenia gravis (la miastenia gravis neonatal
genética debuta de forma congénita), distrofia del músculo elevador del
párpado superior aislada (en edad senil) o asociada a distrofia de otros
músculos oculares o Síndrome de Von Graefe (en jóvenes, sí es familiar),
Síndrome de Kearn (autosómica dominante, retinitis pigmentaria, cardiopatía y
Von Graefe), miopatía mitocondrial oculofaríngea, terapia con toxina A
botulínica, desinserción del elevador por traumatismos, yatrogenia (colirios,
lentes de contacto duras) y espontánea (sólo en edad senil), etc.
3. Mecánicas. Son aquellas que se producen por el aumento de volumen del
párpado, como una inflamación traumática, alérgica, un hematoma, u otro tipo
de tumor benigno o maligno que puede ocluir el ojo [ejemplo un angioma (figura
2), un neurofibroma de una neurofibromatosis orbitopalpebral (neurofibromatosis
tipo I) (figura 3), un sarcoma, etc].

Figura 2. Ptosis mecánica por la presencia de un angioma en el
párpado superior.

Figura 3. Ptosis mecánica por un neurofibroma palpebral en una
niña con una neurofibromatosis tipo I.
EXPLORACIÓN Y EVALUACIÓN DEL PÁRPADO PTÓSICO
En un niño con ptosis palpebral se debe realizar una exhaustiva evaluación
oftalmológica desde el momento de su descubrimiento, porque nos va a
condicionar el tipo y el momento de comenzar la terapia.
En la anamnesis se pregunta a los padres: los antecedentes familiares
y personales del niño, el momento exacto de su aparición, como ha ido
evolucionando el grado de severidad, la posición de la cabeza y del cuello en
posición espontánea, si ha sufrido traumatismos en los párpados o cirugías
previas etc.
En la exploración es importante apuntar las asimetrías, observar el
párpado inferior, la forma de las hendiduras palpebrales, la cara en su
conjunto, la posición de la cabeza y de las cejas en la mirada de frente,
superior e inferior, valorar posibles heterocromías, anisocorias, epicanto,
telecanto, fenómeno de Bell, ptosis de Marcus Gunn (abriendo la boca o
masticando) y la morfología de las órbitas con teleradiografía de ambas
órbitas o Tomografía Computerizada en 3 dimensiones.
La exploración oftalmológica para la agudeza visual, motilidad ocular
(especialmente el recto superior que frecuentemente está hipofuncionante en las
ptosis congénitas) y la medición de la función del elevador completan la
batería de pruebas que nos ayudan a clasificar y a elegir el tratamiento mejor,
para la ptosis que estamos estudiando.
El grado de severidad de la ptosis se puede medir de manera estática,
dependiendo de la posición del párpado que está debajo del limbo corneal.
• Leve: 2 mm.
• Moderada: entre 2 y 4 mm..
• Severa:más de 4 mm.
La medición dinámica evalúa el grado de funcionamiento del músculo
elevador. Para ésto el médico debe inmovilizar el músculo frontal con una
mano y pedir al niño, que sin mover la cabeza, mire en su posición más alta y
superior. Luego en su posición más baja e inferior; así varias veces midiendo
la excursión vertical que hace el párpado. En condiciones normales el párpado
se mueve entre 8 y 15 mm. Conforme esta cifra sea menor el grado de severidad de
la ptosis será mayor. De esta manera los casos en los que el párpado se mueva
solamente 2 mm consideraremos que el músculo apenas funciona.
Todas estas pruebas deben reflejarse fotográficamente.
TRATAMIENTO
La cirugía hay que evitarla en los casos en los que se suponga una posible
regresión espontánea de la ptosis [origen traumático (se aconseja esperar por
lo menos 6 meses), alérgico, etc...]. En todos los demás casos hay que
practicar una intervención quirúrgica que corrija el defecto.
No se debe realizar cirugía correctora de ptosis antes de los 5 años de
edad, debido a la escasa cooperación de los niños para su evaluación
prequirúrgica, a la mayor dificultad por la falta de desarrollo de las
estructuras anatómicas a restaurar y al postoperatorio más difícil de
sobrellevar. La única excepción sería el riesgo de una ambliopía por
oclusión de la pupila o tortículis, en cuyo caso se debe corregir el párpado
ptósico inmediatamente.
TRATAMIENTO DEL SÍNDROME DE LA BLEFAROFIMOSIS
Existen varias técnicas descritas que corrigen todos los defectos de este
síndrome en un tiempo quirúrgico (realizando la corrección de la ptosis y la
cantoplastia simultáneamente) (2,3) o en diferentes tiempos quirúrgicos (1).
En este caso, la primera cirugía tendría la finalidad de corregir el epicanto
(con la técnica de Mustardé´s o colgajos cuadriláteros, la técnica de
Fuente del Campo (4), la técnica de Anderson o de cinco colgajos (5), etc.), el
telecanto (con cantoplastias con fijación alámbrica transnasal) y el déficit
de piel (con injertos cutáneos). La segunda cirugía para medialiazación de
paredes internas de órbita o de toda la órbita si fuese preciso. Y para
finalizar, en la última cirugía se rectifica la ptosis palpebral (con
suspensión al músculo frontal, en la mayoría de los casos).
Krastinova (6), cirujano plástico y discípula de Paul Tessier (padre de la
Cirugía Craneofacial) aboca por una cirugía ósea orbitaria como primera fase
del tratamiento, con el fin de aumentar transversalmente la órbita y
disminuirla verticalmente. Para ello remodela mediante fresado los rebordes
orbitarios y coloca injertos de calota craneal en el suelo de la órbita y en el
reborde superoexterno. En una segunda fase quirúrgica aumenta y estrecha el
dorso nasal con un injerto óseo de calota y una cantoplastia transnasal
alámbrica. En una tercera cirugía repara la ptosis palpebral (figura 4).
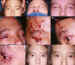
Figura 4. Blefarofimosis: A) Foto preoperatoria; B) Cantoplastia
interna alámbrica transnasal; C) Mantenimiento de la cantoplastia con botones
externos; D) Diseño intraoperatorio del surco supratarsal e incisiones en la
frente para la SPMF; E) Esquema de la colocación de las tiras de fascia lata en
la frente; F) Corrección de la ptosis al traccionar las tiras de fascia lata;
G) Cantoplastia externa para alargar transversalmente la hendidura palpebral; H)
e I) Postoperatorio.
TRATAMIENTO DE LA PTOSIS DE MARCUS GUNN
Lo ideal sería enseñar a los niños a evitar las sinquinesias con
movimientos mandibulares cada vez menores y al final apenas perceptibles. Si
esto no es posible siempre se puede recurrir a la cirugía.
TRATAMIENTO DE LA PTOSIS DE VON GRAEFE
Su tratamiento es muy delicado ya que no presentan fenómeno de Bell, el
cierre palpebral no es bueno y la producción de lágrima está disminuida. Por
todo ello, se debe perseguir no una posición estéticamente adecuada del
párpado, sino sólo una corrección leve para que las pupilas queden libres
pero a la vez bastante protegidas.
TÉCNICAS QUIRÚRGICAS
Siempre que sea posible se debe operar con anestesia local para que mediante
las pruebas de motilidad y comparando ambos ojos, se pueda calcular
perfectamente la posición adecuada de los párpados. Como en los niños esto
no es posible, es aconsejable informar a los padres sobre la dificultad en
conseguir una perfecta simetría y corrección y así alertarles sobre una
posible segunda cirugía.
Común a cualquier técnica que utilicemos, es importante realizar una
valoración prequirúrgica muy precisa con el niño despierto. Ya en el
quirófano es esencial, una hemostasia cuidadosa con coagulación bipolar,
utilizar gafas lupa que facilitan el reconocimiento de las distintas estructuras
anatómicas y tener en cuenta la necesaria hipercorrección de la ptosis. En el
postoperatorio, es conveniente la oclusión palpebral durante 24 horas con un
punto desde el párpado inferior a la frente fijado con esparadrapo (punto de
Frost). En caso de existir lagoftalmos aplicar pomadas nocturnas y gotas
humectantes. Controlar la córnea con la lámpara de hendidura durante las dos
primeras semanas y usar gafas de sol debido a la intensa fotofobia matutina.
Nosotros utilizamos tres técnicas, de forma aislada o combinadas según la
severidad de la ptosis y el funcionamiento del músculo elevador:
1. Müllerectomía. La extirpación del músculo de Müller se hace en
las ptosis leves. Específicamente en aquellas que mejoran temporalmente con la
instilación de unas gotas de fenilefrina al 2,5% en el fondo de saco
conjuntival.
A) Operación de Fasanella Servat (7): Es una técnica sencilla, pero
conlleva una mutilación considerable del párpado superior. Tras evertir el
párpado, se reseca en bloque 2-3 mm de tarso, músculo de Müller y la
conjuntiva adyacente. Corrige ptosis muy leves (hasta 3 mm).
B) Técnica de Puttermann (8): es igual que la anterior preservando el tarso.
2. Resección de la aponeurosis del músculo elevador
(9). Es la más
utilizada en nuestro servicio. Se aplica, como primera opción de tratamiento,
en las ptosis unilaterales leves-moderadas con un funcionamiento del músculo
elevador de por lo menos 4mm. Para calcular los milímetros a resecar se
multiplica los milímetros de ptosis por tres en las ptosis leves y hasta por
cinco en las más severas. Aparte se le suma de uno a dos milímetros de
sobrercorrección, según la ptosis más o menos grave.
Técnica: Con el niño aún despierto se marca el surco supratarsal
(ausente en las ptosis), en relación al ojo sano. Ya anestesiado, se infiltra
por la marca del surco supratarsal prefijado, una solución de lidocaína (1%)
con adrenalina al 1/200.000 y se espera 5 minutos. Se incide la piel y el
músculo orbicular hasta el tarso donde se localiza la aponeurosis del músculo
elevador que se va disecando hasta el ligamento de Whitnall. Se marca lo que se
desea recortar, se recorta y se fija de nuevo el músculo elevador recortado al
tarso con suturas discontinuas no reabsorbibles. Aunque no es fácil, se intenta
conformar el reborde curvado del borde libre del párpado, situando de forma
estratégica las suturas. Además se puede recortar el músculo orbicular
pretarsal y la piel sobrante. Se sutura con monofilamento reabsorbible la piel
con el músculo elevador, con el fin de marcar la hendidura supratarsal (figura
5).
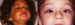
Figura 5. Corrección de una ptosis unilateral congénita con
resección de la aponeurosis del elevador.
En los casos muy severos se puede llegar hasta el ligamento de Whitnall y
suturar directamente éste a la placa tarsal, que a su vez puede recortarse para
conseguir mayores resultados [5 mm de tarso extirpado corrige 1-1,5 mm de ptosis
(10)].
3. Suspensión palpebral del músculo frontal (SPMF). Se realiza cuando
el músculo elevador casi no funciona y el músculo frontal lo hace adecuada y
simétricamente. Esto es típico en las ptosis severas infantiles y en las
blefarofimosis, en las que los niños intentan elevar los párpados subiendo las
cejas. Basado en este hecho esta técnica consiste en crear una unión no
elástica, a modo de tendones, entre el músculo frontal y el párpado superior
que pueda mejorar este efecto. Payr (1928) describió el uso de fascia lata
para realizar la SPMF. Se han descrito muchas variaciones de esta técnica
usando diferentes esquemas en la colocación de la fascia desde la zona tarsal
al músculo frontal [dos rombos (técnica de Friedenwald-Guyton), dos
triángulos (técnica de Crawford) etc.)] y se han usado diferentes materiales
para realizar la suspensión (fascia lata, fascia temporal, silicona,
GORE-TEX expandido etc.).
En nuestra experiencia la fascia lata es el material idóneo para la
SPMF. Es resistente, no elástico y autólogo. Se integra como un verdadero
tendón entre el párpado y el músculo frontal y no tenemos en nuestra
casuística ninguna infección ni rechazo. El uso de fascia lata no se
aconseja en niños menores de tres años por no estar totalmente desarrollada.
El músculo frontal debe funcionar simétricamente al igual que los
elevadores. Si existe una asimetría en la función de los elevadores lo más
seguro es desinsertar ambos músculos del tarso y por tanto anular su acción y
después realizar la SPMF bilateral. Siempre que sea posible se debe realizar la
SPMF bilateral y así conseguir resultados más estéticos y simétricos.
Técnica: Después de marcar el futuro pliegue supratarsal se infiltra
con lidocaiana (1%) y epinefrina al 1/200.000. Se incide la piel y el músculo
orbicular hasta llegar al tarso. En la frente se dibujan tres incisiones de 3-4
mm cada una. La medial se situa encima de la ceja a nivel del canto interno. La
lateral encima de la ceja en el canto externo. La tercera entre las dos
anteriores pero 1,5 cm por encima verticalmente de la ceja. Se infiltran con la
misma solución y se inciden hasta el periostio.
La fascia lata, en tiras de 10-13 cm de largo por 2-3 mm de ancho, se
coloca a través de túneles creados con pinzas mosquito finas, conformando un
triángulo medial, otro lateral y un cuadrado central, entre tres fijaciones
tarsales y las tres incisiones de la frente (dibujo 1, figura 4E). Los túneles
se hacen en profundidad por delante del septum orbitario. No usamos la aguja de
Wright para evitar accidentes en el globo ocular.
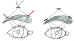
Dibujo 1. Esquema de la técnica doble triangular. En rojo y azul
las tiras de fascia lata. En negro las incisiones frontales y tarsales.
Las tiras de fascia se tensan, primero en la zona medial y luego la lateral,
hasta corregir la ptosis y conseguir simetría entre ambos ojos. Se fijan al
espesor del músculo frontal con suturas no reabsorbibles. Para finalizar y
afinar la posición final del párpado, se tensan las dos tiras de fascia que
emergen por la incisión más superior de la frente (figuras 4E y 4F). En
posición de reposo el margen inferior del párpado debe quedar a nivel del
limbo corneal.
COMPLICACIONES
Por la extracción de la fascia lata puede producirse una cicatriz
hipertrófica en la pierna o una hernia muscular por el cierre defectuoso de la
fascia lata remanente.
En el párpado un hematoma impediría valorar intraoperatoriamente la
corrección adecuada de la ptosis.
La infracorrección de la ptosis se corrige con reintervención quirúrgica.
Si es leve, precisaría simplemente la resección de una porción de tarso de la
zona media en forma de semiluna, equi valente a los milímetros que deseamos
corregir (11).
La hipercorrección de la ptosis ocasiona exposición corneal prolongada que
requerirá protección de la córnea de día y de noche. Si la hipercorrección
es muy severa se debería relajar algún punto mediante tracción ligera del
párpado en el postoperatorio inmediato. Si es leve los masajes palpebrales y
frontales serían suficientes.
El prolapso de la conjuntiva se corrige ocluyendo el ojo, reponiendo
adecuadamente la conjuntiva y empleando pomadas de cortisona. En casos
excepcionales requiere una recolocación quirúrgica.
Las infecciones tras la implantación de fascia lata son muy raras. La
suspensión al múculo frontal con otro tipo de material no autólogo tiene más
probabilidades de rechazo e infección.
BIBLIOGRAFÍA
- Callahan A. Ptosis associated with congenital defects; blepharophimosis,
epicanthus and other syndromes. IN: Symposium on surgery of the orbit and
adnexa. Transactions New Orleans Academy of Ophtalmology. St. Louis, MO, C. V.
Mosby Company, 1974.
- Nakajima T, Yoshimura Y, Onishi K y Sakakibara A. One stage repair of
blepharophimosis. Plast Reconstr Surg. 1991; 87: 24.
- Karacaoglan N, Sahin U, Ercan U y Bozdogan N. One stage repair of
blepharophimosis: anew method. Plast Recostrtr Surg. 1994; 93: 1406-9.
- Fuente del Campo A. A simple procedure for aesthetic correction of the
medial epicanthal fold. Aesthetic Plast Surg 1997; 21: 381-4.
- Anderson RL, Nowinski TS. The five flap technique for blepharophimosis.
Arch Ophthalmol. 1989; 107: 448-52.
- Krastinova A. Blepharophimosis. (Abstract. Presentado en el Congreso
Mundial de Cirugía Plástica y Reparadora, MADRID, Mayo de 1992).
- Fasanella RM, Servat J. Levator Resection for minimal ptosis. Arch Ophthal
1961; 65: 493-6.
- Putterman AM y Fett DR. Müller muscle in the treatment of upper eyelid
ptosis: a ten-year study. Ophthalmic Surg 1986; 17: 354-60.
- Carraway JH y Vincent MP. Levator advancement technique for eyelid ptosis.
Plast Reconstr Surg 1986; 77: 394-403.
- Holds JB y Anderson RL. Blepharoptosis. In: Tse DT, Wright KW, Ryan SJ,
eds. Oculoplastic Surgery. Pennsylvania: Lippincott Company 1992: 164.
- Lesavoy MA, Dubrow TJ, Eisenhauer DM y Sanders G. Upper eyelid ptosis
correction by a revised tarsal resection technique. Ann Plast Surg 1990; 25:
7-13.
|