Anestesia y sedación en cirugía vitreorretiniana
M. Ballvé, M. Gibert, J. Mestre
La anestesia local en la cirugía ocular se utiliza desde hace más de 100 ańos. Koller en 1884 realizó la primera instilación de cocaína para realizar una operación de catarata. En el mismo ańo, Knapp describió la anestesia retrobulbar (1). En la cirugía ocular el riesgo vital es mínimo, por lo que el riesgo de accidentes depende sobretodo de la edad del paciente, de su estado de salud y de la técnica anestésica.
En un trabajo sobre 47.000 intervenciones durante un período de 20 ańos el índice de mortalidad era del 0,10% (2). Estos índices probablemente sean muy inferiores en la actualidad. Los índices de mortalidad postoperatoria global (3) y de reinfarto de miocardio (4) después de la anestesia general para todas las intervenciones ha disminuido en los últimos ańos. En un estudio retrospectivo de 10.278 intervenciones de los ojos en pacientes que habían padecido infarto de miocardio se observó que el índice de reinfarto después de la anestesia local era inferior que para las restantes intervenciones con anestesia general (5). Aunque la anestesia local y general se asocian con la misma mortalidad (6), ambas técnicas no presentan necesariamente el mismo grado de seguridad (2). Por otra parte, se ha demostrado que la anestesia local es más segura en los pacientes de edad avanzada (7).
La anestesia general fue durante mucho tiempo el sistema más empleado para la cirugía ocular pero, desde hace unos 10 ańos, ha aparecido una inversión de esta tendencia en favor de la anestesia locorregional. Todavía los estudios actuales son poco concluyentes, pero todo parece indicar que la morbilidad es mínima con una anestesia local asociada a una sedación del paciente.
CONSIDERACIONES PREOPERATORIAS
Antes de cualquier intervención quirúrgica debe de realizarse una valoración preoperatoria del paciente con el objetivo de reducir los riesgos preoperatorios, la cual incluye los siguientes apartados:
HISTORIA CLÍNICA
Empezaremos por efectuar una historia clínica que debe incluir:
- Diabetes: Es la patología que nos encontrarnos con mayor frecuencia. La prioridad inicial en el paciente diabético es prevenir los desajustes metabólicos evitando oscilaciones de la glicemia antes, durante y después de la intervención.
- Hipertensión arterial: También es muy frecuente en pacientes de edad avanzada. Por sí misma, no presenta un riesgo particular, salvo cuando se asocia a otras patologías como coronariopatías, insuficiencia cardíaca, alteraciones vasculares cerebrales o insuficiencia renal.
El tratamiento antihipertensivo debe mantenerse antes y después de la intervención. Si la hipertensión no está bien controlada nos vamos a encontrar ante un paciente hemodinámicamente más inestable durante el acto quirúrgico.
Si se sigue algún tratamiento con anticoagulantes cumarinicos, deberá suspenderse tres días antes de la intervención. También deberá suspenderse la toma de antiagregantes plaquetarios durante la semana previa a la intervención.
El tabaquismo puede provocar la aparición de tos durante el acto quirúrgico. Si es necesario, administramos codeína 30orales antes de iniciar la cirugía como agente antitusígeno.
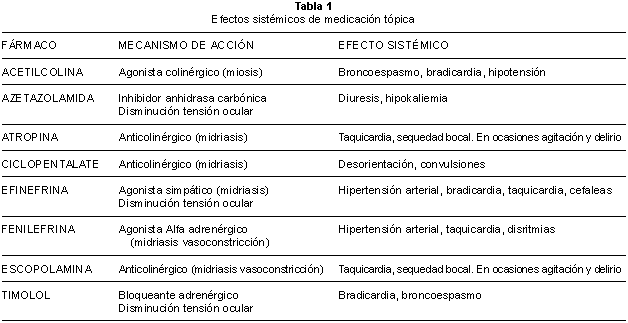
También hay que valorar los efectos sistémicos de los tratamientos oculares seguidos (tabla 1).

La valoración preanestésica sirve también para que paciente y anestesiólogo se conozcan, y para exponer el procedimiento anestésico que vamos a seguir. Los pacientes suelen aceptar bien la anestesia local, incluso los más aprensivos, al saber que la inyección del anestésico en la órbita no producirá ningún dolor ya que estarán inconscientes en este momento.
EXPLORACIÓN FÍSICA
En todos los pacientes la exploración física debe consistir en:
EXÁMENES DE LABORATORIO
Las series de exámenes de laboratorio sistemáticos raramente revelan alteraciones que no se hayan puesto de manifiesto a través de la anamnesis y la exploración física (8,9).
Podríamos proponer de acuerdo con el protocolo elaborado por Blery y Cols (10) la realización de las siguientes pruebas:
Placa de tórax sólo cuando esté clínicamente indicado a las personas ancianas (más de 70 ańos) o con síntomas respiratorios.
MANEJO DEL PACIENTE DIABÉTICO
El procedimiento que seguimos en el paciente diabético tiene como objetivo no interrumpir ni variar el tratamiento antidiabético diario, sea éste a base de insulina, o de antidiabéticos orales, para, de este modo, poder efectuar la cirugía sin ingreso y siga su pauta habitual sin descompensación.
Para ello seguimos el siguiente protocolo: El día previsto para la intervención quirúrgica el paciente debe tomar la dosis diaria de insulina que le corresponda por la mańana o bien tomar el antidiabético oral que utilice habitualmente, seguido de un desayuno ligero rico en hidratos de carbono. La cirugía se programará al final de la mańana o a primera hora de la tarde para respetar el intervalo de 6 horas necesario para el vaciamiento gástrico.
Al llegar el paciente a quirófano practicamos una glicemia: si esta es inferior a 120 mg/dl se administra suero glucosado 5% antes y durante la intervención ajustando la velocidad de infusión, para intentar conseguir glicemias entre 100 y 150 mg/dl al finalizar, momento en que realizamos una nueva valoración de glicemia.
Si hallamos valores entre 120 y 200 mg/dl nos limitamos a perfundir un suero glucosado 5% de 100durante la intervención a ritmo lento para mantener la vía venosa.
Si nos encontramos niveles de glucosa superiores a 200 mg/dl administramos insulina rápida subcutánea según la siguiente pauta:
| Glicemia | Insulina |
| 200-250 | 3UI |
| 250-300 | 6UI |
| superior a 300 | 9UI |
más un suero glucosado 5% de 100al que hemos ańadido ClK 5a una velocidad de unos 50 ml/h.
Al finalizar la intervención el paciente es dado de alta iniciando la ingesta oral inmediatamente de forma progresiva. De este modo, conseguimos que por la noche el paciente cene su dieta habitual y reciba la dosis de insulina que le corresponde según su tratamiento previo, o en su caso el antidiabético oral correspondiente.
MONITORIZACIÓN
La monitorización consiste en disponer de los medios adecuados para obtener información específica y continua de los parámetros implicados durante la anestesia y la intervención quirúrgica.
La monitorización tiene tres objetivos: diagnosticar precozmente cualquier cambio durante la intervención, evaluar la gravedad de la situación y valorar la respuesta al tratamiento.
Antes de la intervención se valora el nivel de conciencia del paciente, mediante la orientación verbal y temporo espacial, lo que favorecerá la cooperación del paciente durante la intervención quirúrgica. Al administrar la anestesia retrobulbar el paciente está dormido bajo los efectos del hipnótico, a los pocos minutos recupera la conciencia.
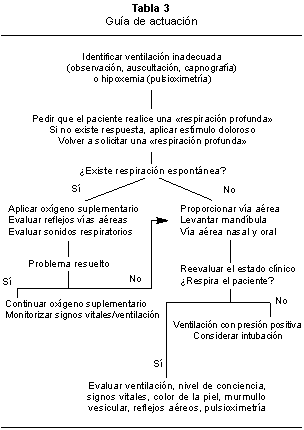
Ha de asegurarse una correcta ventilación a nivel pulmonar, por lo que se colocarán unas gafas nasales para administrar oxígeno y aire, dado que el paciente permanece con la cara tapada por las sábanas estériles. El control de la oxigenación se realizara mediante la pulsioximetría. El pulsioxímetro es un instrumento fotoeléctrico capaz de determinar de forma no invasiva y continua la saturación de oxígeno de la hemoglobina arterial.
El control hemodinámico durante la intervención consiste en mantener una presión arterial y una frecuencia cardíaca dentro de los límites habituales para el paciente. El estrés quirúrgico produce una liberación de catecolaminas por lo que favorece la aparición de taquicardia e hipertensión.
El control de la presión arterial tiene que realizarse cada 10-15 minutos. El control contínuo del ECG permite diagnosticar la aparición de arritmias, isquemia y cuando aparece bradicardia más frecuente en esta cirugía debido al reflejo oculocardíaco.
PROBLEMAS ESPECÍFICOS DE LA CIRUGÍA DEL OJO
- Reflejo oculo-cardíaco (ROC): Se considera que existe activación del ROC cuando, en el curso de una estimulación del ojo o de sus anejos, se observa un descenso de la frecuencia cardíaca del 10 o del 20% y/o aparición de alteraciones varias del ritmo cardíaco.
- Vías anatómicas: La vía aferente pasa por los nervios ciliares cortos y largos, para hacer sinapsis en el ganglio de Glasser, de donde seguirán a través de la rama oftálmica del trigémino hasta el núcleo del nervio sensitivo del mismo, situado en el suelo del IV ventrículo. La vía eferente nace en el núcleo del nervio vago en el suelo del IV ventrículo, después sigue las fibras simpáticas del X par craneal hasta las estructuras miocárdicas y nodales.
- Estímulos desencadenantes: Son numerosos los estímulos que pueden desencadenar un ROC. El más conocido es el desplazamiento sobre el globo ocular. La tracción sobre los músculos oculomotores representa el factor quirúrgico incriminado con mayor frecuencia, sobre todo si esta tracción es súbita, intensa y prolongada. Las intervenciones más reflexógenas son la cirugía del estrabismo y las intervenciones de desprendimiento de la retina.
También existen numerosos factores favorecedores. Los pacientes con riesgo de desarrollar un ROC son aquellos en los que el tono vagal es predominante: nińos y adolescentes, mujeres, pacientes con problemas de ansiedad, pacientes en tratamiento con betabloqueantes por vía general o en colirio. La aparición del ROC puede estar favorecida por la hipoxia, la hipercapnia y la acidosis.
- Consecuencias: La respuesta observada con mayor frecuencia es una bradicardia sinusal. Pueden aparecer también diversas alteraciones de la conducción, como: paro sinusal, bloqueo sino-auricular, bloqueo aurículo-ventricular u otras alteraciones del ritmo. El ROC es un reflejo agotable, puesto que la repetición de estímulos conduce a una alteración de las respuestas provocadas. Por último, generalmente el ROC cede espontáneamente en algunos segundos al cesar el estímulo.
- Tratamientos preventivos: La prevención se basa ante todo en manipulaciones lentas y progresivas del ojo por el cirujano. La anestesia retrobulbar evita la aparición del ROC, pero éste puede aparecer durante la inyección del anestésico. La anestesia peribulbar sólo parece eficaz de modo incompleto para prevenir el ROC (11).
La prevención del ROC con la administración sistemática de un anticolinérgico en la premedicación está actualmente en estudio.
- Tratamiento curativo: La aparición de un ROC debe hacer cesar inmediatamente la estimulación quirúrgica responsable. El retorno al ritmo cardíaco anterior se produce en algunos segundos. Si la repetición del estímulo desencadenante es previsible, entonces si que se impone la inyección intravenosa de atropina.
SEDACIÓN DEL PACIENTE
Los objetivos de la sedación son evitar el dolor al realizar la anestesia local, evitar la aparición de náuseas y vómitos intra y postoperatorios, disminuir la ansiedad, favorecer la amnesia y mantener al paciente colaborador y despierto.
El paciente siempre ha de estar unas seis horas en ayunas antes de realizar una sedación, sino existe un riesgo de aspiración gástrica, lo que puede tener malas consecuencias para el enfermo, tales como la aparición de la neumonitis química y, en algunas ocasiones, se puede producir la muerte del paciente. Para saber el tiempo que el paciente ha de estar en ayunas antes de la sedación es útil conocer de forma aproximada el tiempo de vaciado gástrico de los diferentes alimentos (tabla 2).

FÁRMACOS EMPLEADOS EN LA SEDACIÓN
Ansiolíticos han supuesto un gran avance en el control farmacológico de la ansiedad. Las benzodiacepinas, al facilitar la función inhibidora del ácido gamma-aminobutírico, inducen la aparición del sueńo. En función de la dosis administrada poseen propiedades anticonsulvivantes, actúan como relajantes musculares y producen amnesia anterógrada. Es, en cambio, desconocido el mecanismo por el que producen amnesia. Las benzodiacepinas producen mínimas reducciones del gasto cardíaco y de la presión arterial. Anteriormente se utilizaba el diacepam intravenoso para sedar a los pacientes, sin embargo, este fármaco tiene el inconveniente de producir metabolitos activos, lo que supone que después de haberse recuperado aparentemente de los efectos del diacepam, muchos pacientes pueden experimentar un nuevo episodio de sedación, que comienza algunas horas después de esta recuperación, prolongándose unas horas más. Con el peligro de depresión respiratoria, alteraciones motoras y otras especialmente en pacientes debilitados o ancianos. Para obviar este problema se desarrollaron benzodiacepinas que carecen de metabolitos activos como es el midazolam. El midazolam, es una benzodiacepina hidrosoluble se presenta en ampollas de 5 y 3 ml, que contienen 5 y 15 de substancia activa, respectivamente. Su inicio de acción se sitúa entre los 30 y 60 seg, el efecto máximo se produce a los 2-3de su administración y su vida media es de unas 3 horas. Las principales ventajas del midazolam, que hacen que sea la benzodiacepina de elección para la sedación, son su capacidad para producir ansiolisis, su efecto hipnótico en relación a la dosis, la amnesia retrógrada y la elevación del umbral convulsionante de los anestésicos locales. También su efecto protector frente a la hipoxia cerebral puede ocasionar reducciones mínimas del gasto cardíaco y de la tensión arterial, su margen de seguridad es relativamente amplio y está desprovisto de reacciones alérgicas. Además es hidrosoluble y no necesita solventes, y produce menos tromboflebitis local que el diacepam. Su biotransformación se realiza en el hígado mediante reacciones de oxidación y glucuronoconjugación. La dosis para obtener una sedación óptima se consigue mediante la administración de bolos pequeńos hasta obtener el efecto clínico deseado. La dosis es de 0,1-0,2 mg/kg por vía intravenosa en pacientes adultos sin patología asociada. En pacientes ancianos las dosis se deben reducir aproximadamente en un 20%. Las reacciones adversas que pueden aparecer tras la administración de midazolam son alteraciones de funciones motoras y mentales, somnolencia, debilidad muscular, hipotensión, taquicardia y depresión respiratoria.
Opiáceos actúan sobre receptores farmacológicos específicos, denominados receptores opioides, que se encuentran distribuidos por el sistema nervioso central y periférico. El efecto principal de los opiáceos es la analgesia, mientras que la sedación obtenida suele ser leve. Todos los opiáceos inducen depresión respiratoria e hipertonia muscular. Reducen la resistencia vascular periférica, pero tienen escaso o nulo efecto depresor miocárdico. Todos los opiáceos, con excepción de la meperidina, causan bradicardia. La estimulación de quimiorreceptores medulares producen náuseas y vómitos, por lo que al inicio de la sedación se administra un antiemético para evitar estos efectos indeseables. Todos los opiáceos se distribuyen rápidamente por el organismo tras su administración intravenosa, mostrando un volumen de distribución amplio. Se eliminan por el hígado y los metabolitos inactivos se excretan por la orina. El opiáceo más utilizado es el fentanilo, es un opiáceo sintético 80 veces más potente como analgésico que la morfina. Se presenta en ampollas de 3ml, que contienen 0,15 mg. Se administra a dosis pequeńas de 0,025-0,05 mg. Su inicio de acción es rápido y su efecto máximo se produce a los 5-7 min. de su administración. Sus efectos duran entre 30-45 min. También se puede utilizar el alfentanilo, que es menos potente y menos liposoluble que el anterior. Tiene un comienzo de acción rápido 1-2 min. y su duración es breve 15 min. En la cirugía vitreo-retiniana se utiliza el fentanilo por ser más potente como analgésico y tener un tiempo de duración de acción más prolongado.
Hipnóticos son fármacos que se utilizan para inducir el sueńo. El más utilizado es el propofol, que es un hipnótico de acción corta y de recuperación rápida, que carece de propiedades analgésicas. Pertenece al grupo de los alquifenoles. Su vida media plasmática es de alrededor de 2,5 minutos, se metaboliza a nivel hepático y se elimina totalmente en unos 55 minutos. El propofol se prepara como una emulsión hidro-oleosa isotónica al 1% que contiene lecitina de huevo, glicerol y aceite de soja, es por ello que en ocasiones produce dolor a la inyección sobretodo si la vena periférica empleada para su administración es de calibre fino, por lo tanto es aconsejable canalizar una vena mayor. A nivel cardiovascular el propofol es un depresor cardiovascular que produce un descenso de la presión arterial y del gasto cardíaco, mientras que la frecuencia cardíaca apenas se modifica. Produce, además, una disminución dosis dependiente de la frecuencia respiratoria y del volumen respiratorio. A nivel del sistema nervioso central induce rápidamente la pérdida de la conciencia. aproximadamente en unos 30-45 segundos después de su administración. La dosis habitual de inducción es de 1-2,5mg/kg por vía intravenosa. La dosis debe disminuirse si se administra asociado con otros ansiolíticos, opiáceos o en pacientes ancianos o hemodinámicamente comprometidos. Parece tener un efecto protector sobre la aparición de náuseas y vómitos postoperatorios (8). Como reacciones adversas puede producir movimientos involuntarios, convulsiones y reacciones de hipersensibilidad.
Se realiza la anestesia retrobulbar, cuando el paciente está dormido, después de la administración del propofol, y con todos los parámetros hemodinámicos monitorizados, además se administra continuamente oxígeno y aire para evitar una posible hipoxia.
Antagonistas son unos fármacos que actúan ocupando unos receptores específicos de los opiáceos y de las benzodicepinas a nivel del sistema nervioso central, estos fármacos permiten revertir sus efectos farmacológicos. En la tabla 3 se muestran las principales características de los dos fármacos antagonistas comúnmente empleados: flumacenil y naloxona. Estos fármacos tienen que estar a mano siempre que se realice una sedación. El flumacenil es un antagonista de las benzodiacepinas que revierte el efecto de sedación y de depresión respiratoria a las dosis de 0,1-0,2 mg, que se pueden repetir hasta administrar un máximo de 3 mg.
La naloxona es un antagonista de los opiáceos que revierte la analgesia y que se utiliza fundamentalmente para revertir la depresión respiratoria producida por los opiáceos. Se administra a la dosis de 0,5-1 microgramos/kg por vía endovenosa y no es aconsejable repetir la dosis. Su inicio de acción es rápido (1-2 minutos) y se metaboliza por vía hepática. Los efectos adversos que puede producir son un aumento de la frecuencia cardiaca y de la presión arterial y, en ocasiones, edema pulmonar. Ambos antagonistas, naloxona y flumacenil, tienen una corta duración de acción por lo que se debe controlar a los pacientes por lo menos durante un periodo de 2 horas, hasta asegurar que no aparezca la depresión respiratoria (9).
Cuando la sedación es demasiado profunda puede dar lugar a depresión respiratoria, obstrucción de las vías aéreas, hipotensión y/o desorientación (tabla 3), es entonces cuando se debe valorar la posibilidad de administrar los antagonistas. Se administra flumacenil en casos de sedación excesiva producida por benzodiacepinas, o se puede administrar la naloxona cuando se presupone una existencia excesiva a nivel sanguíneo de opiáceos.
Por otra parte, si la sedación es insuficiente puede dificultar la realización del bloqueo ocular anestésico por movimientos incoordinados con el riesgo de complicaciones como punción del globo ocular. Además en aquellos pacientes con patología cardiaca puede favorecer la aparición de hipertensión y taquicardia, efectos indeseables especialmente en pacientes coronarios.
Antieméticos: para evitar la aparición de náuseas y vómitos intra y postoperatorios en la cirugía vítreorretiniana se administra ondansetron unos 20 minutos antes del inicio de la intervención. Este fármaco es un antiserotonínico que bloquea los receptores 5-HT3 de la serotonina. Se metaboliza a nivel hepático. Su vida media es de aproximadamente unas 3,5 horas. Es un fármaco de larga duración que se administra por vía endovenosa a la dosis de 4 mg. No presenta efectos secundarios importantes, salvo en ocasiones cefalea y moderada sedación. Es importante administrar un antiemético, ya que muchos pacientes que se intervienen de cirugía vitreo-retiniana son diabéticos y tienen un retraso en el vaciado gástrico por presentar una gastroparesia, lo que facilitaría la presencia de náuseas y vómitos. Además la etiología de las náuseas y vómitos en este tipo de cirugía no es bien conocida aunque probablemente sea debida a la tracción de los músculos oculares que estimula las vías aferentes del centro del vómito a través del ganglio ciliar o de las vías laberínticas (reflejo oculogástrico o oculoemético).
Hasta hace unos ańos se utilizaba siempre la atropina en la premedicación preoperatoria para reducir las secreciones y prevenir efectos vagales nocivos. Sin embargo, en la actualidad se ha reducido notablemente este fármaco excepto en los nińos. La atropina es un fármaco vagolítico, que reduce de forma selectiva los efectos de la estimulación parasimpática. Es un antagonista competitivo de la acetilcolina a nivel de los receptores muscarínicos. Presenta una acción excitadora del sistema nervioso central. La dosis en los adultos es de 0,5 a 1 mg.
ANESTÉSICOS LOCALES
Mecanismo de acción: Los anestésicos locales (AL) producen un bloqueo reversible de la conducción de impulsos a lo largo de las fibras nerviosas. Recordemos que la conducción nerviosa es debida al cambio del gradiente eléctrico de la membrana nerviosa: al producirse un estímulo suficientemente intenso ésta pasa a tener un potencial de reposo de unos -90a una fase de despolarización seguida de una fase de repolarización. La despolarización de un segmento de nervio produce la despolarización del segmento adyacente. De esta manera, un estímulo aplicado a un extremo del nervio será transmitido a lo largo de toda la fibra nerviosa.
La despolarización es debida a la entrada de iones sodio desde el espacio extracelular al intracelular, a través de unos canales específicos del sodio en la membrana. Los AL evitan la despolarización de la membrana nerviosa al bloquear dichos canales, inhibiendo así el flujo de iones sodio.
Características químicas: los anestésicos locales son bases débiles cuya estructura química incluye un radical aromático ligado a una amina a través de un enlace tipo éster o amida. En base a este enlace podemos clasificar los AL en dos grupos:
Ésteres:
Amidas:
Los AL también pueden clasificarse según la duración de su efecto:
A.L. de duración media:
A.L. de duración larga:
Metabolismo:
Ésteres: la colinesterosa plasmática rompe rápidamente el enlace éster dando lugar a metabolitos que se eliminan en poco tiempo por el rińón. Uno de los principales metabolitos es el ácido paraaminobenzoico, capaz de inducir reacciones de tipo alérgico en un pequeńo porcentaje de pacientes.
Amidas: son metabolizados en el hígado dando lugar a metabolitos más hidrosolubles que son eliminados por el rińón. Están prácticamente exentos de riesgo alérgico.
Es por esto que en la actualidad prácticamente sólo se utilizan los AL del grupo de las amidas. Los principales aspectos que influyen en la elección del AL son el tiempo de latencia necesario para el inicio del bloqueo, la duración de los efectos del preparado y las propiedades concretas de cada fármaco, incluida su toxicidad y la dosis total necesaria.
Descripción individual:
Lidocaína: fué sintetizada en 1943. Es el más estable de los AL pudiendo ser esterilizado en autoclave. Posee un gran poder de difusión presentado un inicio rápido de su acción anestésica (2-3 minutos). Tiene efecto vasodilatador local lo que puede provocar un mayor sangrado quirúrgico. La duración de su acción es moderada (1-2 horas). Se utiliza a concentraciones del 0,5% al 2% para inyección y al 4 ó 5% como anestesia tópica.
Mepivacaína: fué sintetizada en 1956. El inicio del efecto anestésico es similar al de la lidocaína. No tiene efecto vasodilatador y es preferida en la cirugía ocular. La duración de la anestesia es algo más prolongada que la de la lidocaína. Se utiliza a concentraciones del 0,5 al 2%. No es eficaz como anestesia tópica.
Bupivacaína: fué sintetizada en 1957. Su periodo de latencia es algo más prolongado (±10 minutos) y la duración de su efecto es tres veces mayor que el de la mepivacaína (3-8 horas). No tiene efecto vasodilatador. Es por estas características que es el AL más utilizado en cirugía ocular a concentraciones del 0,5 ó 0,75%.
Prilocaína: fué sintetizada en 1960. Su inicio de acción es más lento que el de la lidocaína y su efecto es algo más prolongado. Es un buen anestésico para aplicación tópica. Se utiliza a concentraciones del 1 ó 2% para infiltración y al 4% como anestésico tópico.
Ropivacaína: fué sintetizada en 1957, no se ha introducido en la clínica hasta 1988. Es muy similar a la bupivacaína. Su inicio de acción es relativamente corto (6-7 minutos) y su duración como la de la bupivacaína. Presenta un efecto vasoconstrictor moderado.
BLOQUEO RETROBULBAR
La anestesia retrobulbar se describió por primera vez en 1884 cuando Herman Knapp utilizó la inyección de cocaína por detrás del globo ocular para realizar una enucleación (1).
Atkinson en 1936 popularizó esta técnica. La inyección retrobulbar de anestésicos locales proporciona acinesia de la musculatura extraocular al bloquear los pares craneales III, IV, y VI, así como anestesia los tejidos del globo ocular al bloquear los nervios ciliares. El objetivo de la inyección retrobulbar es depositar el anestésico local dentro del cono formado por los músculos extraoculares, lo más cerca posible del ganglio ciliar. El espacio retrobulbar intracónico está definido por la musculatura de los rectos; el espacio peribulbar está por fuera del espacio retrobulbar. El bloqueo retrobulbar afecta principalmente al ganglio ciliar y a los nervios ciliares posteriores largo y corto. De esta manera se produce una denervación eficaz del globo, que queda paralizado con las pupilas dilatadas y una disminución de la presión intraocular. En general, suele observarse un cierto grado de exoftalmia dependiendo del volumen de líquido inyectado.
TÉCNICA DE LA PUNCIÓN RETROBULBAR
Para efectuar la inyección retrobulbar debe colocarse al paciente en decúbito supino y con la mirada al frente, ya que de esta manera se protege al nervio óptico (13) de una punción accidental que puede ocurrir más fácilmente en la mirada hacia arriba y afuera. Al realizar la anestesia retrobulbar el paciente está bajo los efectos del propofol es decir dormido, en nuestra experiencia se presentan tres situaciones: a) mirada espontánea al frente, es correcta para la realización de la anestesia retrobulbar y es la más frecuente. b) mirada discreta hacia arriba adentro y afuera es también correcta para la anestesia retrobulbar y por último c) mirada hacia abajo. En esta situación que hace difícil la inyección retrobulbar podemos inyectar más propofol y esperar a que se posicione el globo ocular o desplazarlo mecánicamente con el dedo para realizar la inyección retrobulbar. Este movimiento es más frecuente en pacientes con trastornos motores de tipo nistágmico con baja visión de nacimiento.
Con una aguja de 30de longitud y del calibre 23, la punción de la aguja debe efectuarse en dirección perpendicular a la superficie cutánea en el tercio externo del borde inferior de la órbita. Se atraviesan dos resistencias, el septum orbitario o cápsula orbitaria y después la membrana intermuscular que une los músculos rectos externo e inferior, lo que confirma la penetración en el cono musculoaponeurótico. Después se dirige la aguja dorsalmente paralela al plano sagital y al suelo de la órbita, penetrando la aguja entre los músculos rectos lateral e inferior. El bisel de la aguja debe orientarse hacia el globo para reducir el riesgo de perforación. Después de su inserción, y antes de inyectar el anestésico, debe efectuarse una aspiración suave para descartar una punción intravascular. Si la prueba de la aspiración es negativa, el anestésico local se inyectará lentamente (1cada 10 segundos hasta los 4-6necesarios). Es mejor ańadir hialuronidasa (a la dosis de 5-15 UI/ml) al anestésico local, lo que facilitará su difusión (14). Sin embargo, en ocasiones, la asociación de hialuronidasa se ha descrito que puede producir un edema retiniano (15).
Utilizamos una mezcla de al 50% de bupivacaína al 0,75% con mepivacaína al 2% inyectando entre 3 y 6dependiendo del volumen orbitario. Otra posibilidad sería efectuar el bloqueo con ropivacaína, pero aún no se dispone de suficiente información, habiéndose empleado sólo para realizar anestesia peribulbar (16).
No es aconsejable el uso de vasoconstrictores con los anestésicos locales ya que podría producirse una vasoconstricción de la arteria oftálmica y ciertos efectos a nivel sistémico (17).
COMPLICACIONES DE LA ANESTESIA RETROBULBAR
La más frecuente es la insuficiente anestesia de los tejidos externos por lo que tendremos que realizar unas inyecciónes suplementarias subconjuntivales de mepivacaina. En segundo lugar aparece la falta de aquinesia que puede ser leve o severa en este caso deberemos reinyectar anestésico peribulbar en todos los cuadrantes.
La posibilidad de que aparezca hemorragia orbitaria es baja: 1/1050 casos, según un estudio de Hamilton (18). Para evitarla se puede realizar compresión orbitaria durante unos minutos. Si es leve y no exite sangrado se puede realizar la intervención. Si es severa debemos observar la arteria central de la retina y si existe isquemia se debe evaluar una posible descompresión orbitaria. El diagnóstico se establece por la presencia de exoftalmia, equimosis y aparición de sangre a nivel subconjuntival. Puede aumentar la presión intraocular y aparecer, más tarde, el reflejo oculocardíaco, por lo que es aconsejable posponer la cirugía.
La perforación del globo ocular es una complicación grave que puede ocasionar la pérdida o la disminución importante de la visión (19), la aparición de la hemorragia vítrea y/o el desprendimiento de la retina (20,21). La causa primera es la miopía siendo las demás menos frecuentes. Se produce especialmente en pacientes con alta miopía que tengan gran diámetro antero posterior y que tienen órbitas pequeńas. Es difícil entonces hallar el espacio intracónico y fácil puncionar la pared del ojo debilitada por la miopía. Existen una serie de factores que aumentan el riesgo de perforación ocular como son el enoftalmos grave, la colocación previa de una banda de silicona escleral, las intervenciones previas, las inyecciones repetidas y la falta de colaboración del paciente en el momento de efectuar la punción 22-24.
El traumatismo o punción del nervio óptico es una complicación infrecuente pero potencialmente grave ya que puede ocasionar severas lesiones intraoculares como la hemorragia vítrea. Los pacientes miopes son los más expuestos a esta complicación.
La estimulación del reflejo oculocardíaco puede producir manifestaciones muy variables como bradicardia con hipotensión arterial o, todo lo contrario, taquicardia con hipertensión. Se han descrito también alteraciones del ritmo y de la conducción cardíaca. El reflejo oculocardíaco puede desencadenarse por manipulación o presión del globo, por tracción excesiva en los músculos extrínsecos del ojo, por inyección intraocular y/o por hematoma intraorbitario. En el estudio de Hamilton sobre 12000 anestesias locorregionales estas reacciones vagales se produjeron en menos del 1% de los casos (18).
Otras complicación que es excepcional consiste en la inyección intraarterial de anestésico local. La inyección en la arteria oftálmica llega, por vía retrógada, a la arteria carótida interna y después difunde hacia el cerebro. En este caso pueden aparecer todos los signos neurotóxicos de una sobredosis de anestésicos locales como bostezos, temblores, parestesias labiales, entumecimiento de la lengua, zumbidos de oído, mareo, vértigos y convulsiones. Esta complicación puede evitarse si se tiene la precaución de efectuar una aspiración antes de inyectar el anestésico, que se administrará lentamente.
La diplopia (complicación rara), la ptosis (más frecuente) o ambas, ya sea temporal o permanente, pueden aparecer tanto en el bloqueo retrobulbar como en el peribulbar, creyéndose que pueden deberse al efecto miotóxico de los anestésicos locales (25).
La inyección subaracnoidea de anestésicos locales, con la consiguiente depresión del sistema nervioso central es una complicación poco frecuente en el bloqueo retrobulbar. Dependiendo de las áreas afectadas pueden aparecer escalofríos, amaurosis contralateral, eventual pérdida de conciencia, hipotensión y bradicardia, apnea, hemiplejía, paraplejía o hiperreflexia. El bloqueo del VIII al XII par craneal puede producir sordera, vértigo, vagolisis, disfagia, afasia e, incluso, paro respiratorio, lo que requerirá la intubación del paciente y la instauración de las maniobras de reanimación cardiopulmonar (26).
BLOQUEO PERIBULBAR
La anestesia peribulbar fue descrita por Bloomberg en 1986 (27) y consiste en la inyección de anestésico en el espacio extracónico. Desde el punto de vista técnico el bloqueo peribulbar se considera más sencillo, seguro, menos doloroso y con menos complicaciones que el bloqueo retrobulbar (28-30). Se inicia con una desinfección de los párpados y conjuntiva y una anestesia tópica superficial. Normalmente se realizan dos inyecciones, una en el cuadrante inferoexterno, en la unión del tercio externo y de los dos tercios internos, y la segunda en el cuadrante superointerno, en la unión del tercio interno y de los dos tercios externos. Las punciones pueden ser transpalpebrales o transconjuntivales. La aguja se dirige hacia atrás en una profundidad de 30 mm. Puede percibirse un resalte, correspondiente al paso del septo orbitario. Después de una prueba de aspiración se inyectan de 4 a 6de anestésico en cada punción. El anestésico local se coloca por fuera de la musculatura del cono. Para la punción el paciente se coloca en decúbito supino, la mirada al frente. Se utiliza una aguja desechable de 25 mm de longitud y de calibre 30 de grosor, conectada a una jeringa de 5ml con el anestésico local, que se introduce en la cara nasal de la carúncula (después de instilar anestesia tópica en la conjuntiva). Habitualmente se ańade hialuronidasa (31), para favorecer que el anestésico local se disperse y aliviar la presión dentro de la órbita, después de la inyección debe aplicarse una compresión firme durante 15 minutos mediante el balón de Honan o similar.
En la anestesia peribulbar las posibles complicaciones de este tipo de bloqueo son la hemorragia y la perforación del globo ocular (32,33). En el plano farmacológico, la anestesia peribulbar realiza un bloqueo por difusión, su inicio de acción es más lenta que la retrobulbar. Por las mismas razones, el bloqueo del nervio óptico es, a menudo, incompleto por que existe percepción visual (34). La compresión que se realiza después de la inyección del anestésico es importante ya que facilita la difusión y reduce la equimosis, que es casi constante con esta técnica (35). La anestesia peribulbar se puede realizar con una sola punción inferior, aumentando el volumen de anestésico local inyectado como han demostrado Korneef y Cols (36). En efecto, en este nivel no existe un límite franco entre los sectores extracónicos e intracónicos, ambos compartimentos están conectados, y es por ello que tanto la anestesia peribulbar como la retrobulbar tienen efectos parecidos.
VENTAJAS DE LA ANESTESIA LOCAL
El objetivo de la anestesia local es evitar el dolor intraoperatoriamente también se consigue una buena analgesia postoperatoria durante un intervalo de tiempo 4-6 horas, que en algunos casos puede llegar a las 24 horas, produciendo una analgesia prolongada. Otras ventajas se basan en su seguridad, ya que evita los problemas derivados de una anestesia general tales como complicaciones respiratorias, trastornos metabólicos y la aparición de náuseas y vómitos.
Con la anestesia local se produce acinesia, mínima hemorragia, se controla la presencia del reflejo oculocardíaco, la presión intraocular y las posibles interacciones medicamentosas. También se evita la aparición de tos, nauseas y vómitos disminuyendo las maniobras de Valsalva en el postoperatorio que inducen al sangrado. Se facilita el control estricto del paciente diabético mediante el ayuno y el control de la glucemia pre y postoperatoria. La anestesia local también reduce la incidencia de las infecciones y de las enfermedades propias del encamamiento. Además también, al no requerir la hospitalización del paciente, reduce los costes de las intervenciones.
ANESTESIA GENERAL EN CIRUGíA VÍTREO-RETINIANA
Los principios a tener en cuenta en la conducta de la anestesia general (AG) son:
INDICACIONES
En la mayoría de los casos, la AL puede ser aplicada para realizar cualquier intervención en oftalmología.
Existen una serie de casos en los que la AL es imposible:
Los pacientes por debajo de los 14 ańos normalmente no son cooperativos para realizar AL y, aunque no existe una clara línea respecto a la edad en la cual puede hacerse uno u otro tipo, habitualmente por encima de los 14 ańos suelen ser coooperativos.
Algunos pacientes adultos no son colaboradores, ya que tienen transtornos profundos de carácter con fobias o tienen hipercinesia patológica.
Los pacientes con deficiencia mental que tengan un coeficiente intelectual bajo y no sean cooperadores debe realizarse con AG; en algunos casos de deficiencias leves, puede utilizarse AL.
Pacientes con enfermedades neurológicas que les impidan permanecer quietos durante la intervención: enfermedad de Parkinson, espasticidad, movimientos involuntarios como los tics son candidatos a la AG.
Pacientes con transtornos de la coagulación severos que la anestesia retro o peribulbar pueda provocar una hemorragia severa. Normalmente esta indicación es para la cirugía de la catarata en la que no se tocan los vasos oculares y por tanto la posibilidad de hemorragia es mínima, ya que no damos posibilidad de sangrado a los vasos oculares ni orbitarios.
TÉCNICA
Los pasos en intervenciones vitreorretinianas tienen sus particularidades técnicas incluyendo los mismos pasos que otras intervenciones como son:
1. Preanestesia.
2. Monitorización.
3. Inducción.
4. Intubación.
5. Mantenimiento.
6. Recuperación.
1. PREANESTESIA
El objetivo principal de la premedicación es aliviar la ansiedad preoperatoria y minimizar las náuseas y vómitos en el postoperatorio; estos se pueden producir tanto por la administración de algunos fármacos anestésicos tipo mórfico como por el tipo de intervención que se realice. Especialmente en las que se practican sobre la esclerótica y con procedimientos de identación de 360°, ya que tienen tendencia a desencadenar mayores reacciones de náuseas y vómitos.
En la visita preanestésica valoraremos el paciente y programaremos la premedicación, ajustándola de forma individualizada y en relación a la edad, peso y patologías conocidas. Es mejor evitar siempre las pautas rutinarias de prescripción ya que son menos precisas.
En pacientes cardiópatas es muy importante hacer una buena premedicación con el fin de evitar la ansiedad y la hipertensión, ya que podrían descompensar su cardiopatía. Por tanto, hay que sedarlos más profundamente, ya que muchas veces al preocuparnos de su cardiopatía tendemos a administrar dosis de sedantes mucho más bajas.
Especial cautela debemos tener en los pacientes más ancianos con la premedicación de benzodiacepinas, ya que de por sí producen amnesia retrógrada y pueden desarrollar con más facilidad cuadros de desorientación temporo-espacial; por tanto, hay que reducir mucho las dosis.
En los pacientes pediátricos sólo usaremos como premedicación:
Ondasetrom:
Atropina:
El Ondasetrom es un antiemético y se usa como profilaxis de náuseas y vómitos postoperatorios. La dosis en los pacientes pediátricos serán según edad debido a su inmadurez en el metabolismo de los fármacos.
La Atropina es un parasimpaticolítico y antisialogogo. Se usa como profilaxis para evitar los reflejos vagales, las bradicardias que se producen tras la administración de fármacos para la sedación pero en la mayoría de los pacientes les produce sequedad de boca, lo que crea una incomodidad. Se puede prescindir de ella en la AL pero en la AG es más difícil por todas las maniobras de la intubación que son más traumáticas y van acompańadas de reflejos vagales más importantes.
En nińos mayores de 5 ó 6 ańos, ańadimos a la premedicación pediátrica descrita, la benzodiacepina si se precisa ya sea por vía endonasal o endovenosa.
Midazolam:
El midazolam es una benzodiacepina de efecto rápido y duración corta. La vía endonasal la utilizamos en nińos que no son nada colaboradores y se evita la vía intramuscular. Consiste en la instilación a través de la nariz de la dosis de midazolam que le corresponda por su peso. Tiene además la ventaja que esta vía de administración es menos agresiva para el nińo.
Se tiende a evitar los mórficos en los nińos ya que prolongan el tiempo de despertar postanestesia y ello nos va a dificultar un alta precoz del paciente en cirugía sin ingreso.
2. MONITORIZACIÓN
Es imprescindible para detectar cualquier transtorno durante el acto quirúrgico, ya sean pacientes adultos o en edad pediátrica. El paciente permanece cubierto con tallas quirúrgicas estériles pero debemos tener acceso en todo momento a parte del paciente como por ejemplo la mano, lo cual nos permitirá controlar el color, temperatura y pulso radial. Por otra parte, debemos disponer de un electrocardiograma, un pulsioxímetro y la tensión arterial indirecta, con el fin de controlar probables alteraciones de la ventilación, perfusión y tensión arterial.
3. INDUCCIÓN
El objetivo de la inducción es lograr una AG profunda para poder ventilar mejor al paciente y proceder a las maniobras de intubación orotraqueal que pueden ser muy traumáticas si el plano de anestesia no es profundo.
Los inductores que usamos son:
Paciente adulto
Paciente pediátrico
Los inductores en edad pediátrica los administramos por vía inhalatoria lo que nos permite una venoclisis correcta para la administración de drogas endovenosas y la sueroterapia si se precisa.
En la anestesia de edad pediátrica es importante disponer de una vía endovenosa permeable y de fácil acceso una vez el campo quirúrgico esté preparado: las vías aconsejables las de las extremidades inferiores que son las más distales de la zona a intervenir.
Como anestésico inductor usamos el sevorane (46) que es un gas inhalatorio que tiene una menor incidencia de náuseas y vómitos en el postoperatorio comparado con otros elementos halogenados como son el halotano e isofluorano. El sevorane es un derivado fluorado del metilisopropil-eter y no contiene otro halógeno fuera del fluor. En general es mejor tolerado que el halotano por no tener un olor pungente por lo que mejora su tolerancia a la inspiración y reduce el rechazo a la mascarilla en los nińos y adultos (37). Proporciona una inducción rápida con un ajuste más rápido de la profundidad del plano anestésico y una buena estabilidad hemodinámica. Por su baja solubilidad tiene una rápida eliminación por vía respiratoria teniendo una rápida recuperación de la AG.
4. INTUBACIÓN
La maniobra de intubación debe ser rápida y atraumática. Se puede realizar la intubación sin relajante muscular, pero es mejor aplicar lidocaina tópica 2% (20 mg.) en las cuerdas bucales antes de la intubación para evitar la tos y las maniobras de Valsalva que se producen tras la intubación. Procederemos de esta manera y de forma preferente cuando realizamos anestesia en prematuros y neonatos en los que la inducción se ha practicado únicamente con sevofluorano ya que la administración de relajantes musculares no es bien tolerada por su inmadurez en la respuesta muscular.
Independientemente de que la inducción se haya realizado con sevofluorano o propofol, como relajante muscular utilizamos para la intubación el vecuronio Norcuron®, al igual en nińos y adultos. Las dosis son 1 mg./10 kg. peso. El vecuronio es un relajante muscular no despolarizante de acción rápida (90 segundos) y veinte minutos de duración si no se potencia con ningún otro agente anestésico halogenado. En el caso de asociarse, su duración se prolonga unos 30 minutos. Su eliminación es muy poco dependiente de mecanismos renales; se realiza principalmente a través del hígado y sólo un 10-20% a través del rińón. En pacientes menores de un ańo la duración de acción del vecuronio se encuentra aumentada mientras que en los nińos de edades comprendidas entre 2 y 9 ańos disminuye (38). El vecuronio no es liberador de histamina y por tanto está desprovisto de efectos vagolíticos. Aunque se metaboliza por el hígado no tiene efectos acumulativos demostrados, y no hay una recurarización a las 2 h. de intervención como en el caso de otros relajantes del tipo bromuro de pancuronio, Pavulon®, con efectos residuales que son negativos para una AG ambulatoria.
Material de intubación
5. MANTENIMIENTO
El mantenimiento de la AG se efectúa con una mezcla de oxígeno con aire al 45-50% y el agente anestésico inhalatorio sevorane según la concentración alveolar mínima que se necesite ya sea para nińos o para adultos.
Hay que tener en cuenta que durante el mantenimiento de la anestesia general, no debe usarse otra droga analgésica de tipo mórfico ya que prolonga el despertar de la anestesia y la recuperación postoperatoria del paciente.
En la cirugía vitreorretiniana se utilizan gases para manipular y taponar los tejidos intraoculares. El óxido nitroso es un agente anestésico utilizado en el mantenimiento, pero por su difundibilidad dentro de los gases hace desplazar el gas intraocular si lo utilizamos durante las maniobras de intercambio con gas intraocular. De esta manera, puede ocurrir que al final de la intervención, al eliminarse el óxido nitroso de la sangre del paciente y del ojo, que el volumen efectivo del gas que se esperaba en la intervención sea menor. Por ello, hay que desconectarlo unos 10-15 minutos antes de inyectar el gas o bien es más conveniente no utilizarlo para evitar posibles accidentes por uso indebido.
6. RECUPERACIÓN ANESTÉSICA
Es el despertar del paciente y para ello procederemos a la extubación que habrá que evitar todas las maniobras de valsalva en lo posible ya que aumentan la presión venosa y puede aparecer un sangrado brusco de los vasos retinianos; por ello, hay que aspirar con delicadeza las secreciones faríngeas y gástricas que se producen durante el acto anestésico.
La lidocaina 2% a dosis de 1.5 mg./kg. endovenosa unos dos minutos antes de la extubación, puede reducir la obstrucción de las vías aéreas y prevenir el laringoespasmo en pacientes jóvenes con cuello muy largo, los bronquíticos y sobre todo los fumadores.
ANALGESIA POSTOPERATORIA
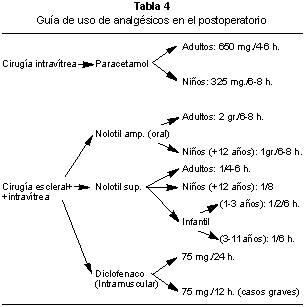
Debido a la rapidez de eliminación de los anestésicos generales, hay que tener en cuenta la aparición precoz de dolor postoperatorio. Es necesaria la administración de analgésicos inmediata ya sea por vía parenteral o rectal. Los analgésicos tipo dipirona y diclofenaco tienen las ventajas de que son más potentes que el paracetamol; se utilizan especialmente cuando se ha realizado cirugía vitreorretiniana y se ha trabajado en la pared exterior del ojo poniendo procedimientos de identación escleral. En general, en los procesos que solamente se ha trabajado en el interior del ojo con procedimientos intraoculares de vitrectomía tienden a ser menos dolorosos; a estos, la administración de paracetamol estaría indicada.
En nińos menores de 1 ańo se puede dar paracetamol en gotas por vía oral.
En la tabla 4 se resume la guía de uso de analgésicos en el postoperatorio.
ANESTESIA COMBINADA
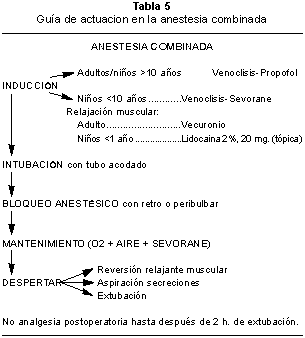
Se trata de combinar la AG con una anestesia retrobulbar o peribulbar que va a potenciar el efecto analgésico ocular de tal manera que va a beneficiarnos al necesitar menos agentes anestésicos de tipo mórfico y también menos concentración de inhalatoria. Está indicada en pacientes de 4-14 ańos o en algunos pacientes en los que no se puede realizar una AL.
En pacientes por debajo de 4 ańos no se emplea la anestesia combinada porque es más difícil y peligroso en estos casos inyectar anestésico local en la órbita por problemas de espacio orbitario, y la poca rigidez del globo ocular y es más fácil penetrar en la pared del globo. Por eso es mejor realizar solo la anestesia general evitando la inyección retrobulbar. Las dosis y guía de actuación, están resumidas en la tabla 5.
VENTAJAS E INCONVENIENTES DE LA ANESTESIA GENERAL Y COMBINADA
Ventajas de la anestesia combinada:
No es necesaria la analgesia endovenosa en toda la intervención puesto que el ojo lleva un bloqueo anestésico suficiente que evita el reflejo doloroso.
El plano anestésico general es menos profundo yconlleva a un despertar más rápido del paciente.
La analgesia postoperatoria es más duradera ya que el ojo tiene bloqueo anestésico y si es con bupivacaina puede prolongarse durante unas horas. En los nińos esta analgesia postoperatoria hace que tengan un despertar menos agitado.
Permite una ingesta más rápida lo que lo hace muy beneficioso en ciertos pacientes con dietas especiales o en pacientes de pocos meses o semanas de vida que requieren ingestas repetidas.
Permite realizar cirugía sin ingreso de forma más ágil ya que el paciente deambula y está en un estado de conciencia mucho más rápido que utilizando sólo AG.
Inconvenientes de la anestesia combinada:
Tiene el riesgo de la anestesia general pero con el beneficio de que usamos una menor cantidad de medicación.
Tiene la desventaja de que hay que bloquear el globo ocular poniendo una infiltración intraorbitaria peri o retrobulbar.
Ventajas de la anestesia general:
En pacientes no colaboradores a los que hay que realizar una cirugía larga y complicada.
Inconvenientes de la anestesia general:
En pacientes con patología broncopulmonar en los que se hace difícil la extubación, lo cual retrasaría el tratamiento postural postquirúrgico requerido cuando se inyecta gas o aceite de silicona.
Al aumentar la incidencia de náuseas y vómitos postoperatorios, aumentan las maniobras de valsalva produciéndose una hiperpresión venosa dando lugar a un sangrado intraocular, sobretodo en pacientes diabéticos o con otras vasculopatías retinianas.
La ingesta de líquidos y sólidos es más tardía, lo cual podría descompensar el control de tratamiento de los pacientes diabéticos, lo que ello conlleva, a modificar sus pautas habituales de insulina. Contrariamente a lo que ocurre con la AL ya que el paciente no modifica su pauta de insulina y tampoco modifica su ingesta como ya se citó.
BIBLIOGRAFÍA