
Dres. Barrio Barrio J1, Mínguez Muro E2, Cristóbal Bescós JA3, Martínez Morales J1, Romano Ortega P2, Palomar Gómez A4
Hospital Clínico Universitario. Zaragoza.
(1) Licenciado en Medicina y Cirugía. Médico residente.
(2) Licenciado en Medicina y Cirugía. Médico adjunto. Oftalmología.
(3) Doctor en Medicina y Cirugía. Profesor asociado. Jefe de Sección. Oftalmología.
(4) Doctor en Medicina y Cirugía. Profesor titular. Jefe de Servicio. Oftalmología.
Introducción
La opacificación de la cápsula posterior después de la cirugía extracapsular del cristalino es la complicación que ensombrece con mayor frecuencia el pronóstico visual de los pacientes intervenidos de catarata. La incidencia se sitúa, según un metaanálisis de 90 estudios previamente publicados, entre el 0,7 y el 47,6% con una media ajustada del 19,7% (1).
Se admite que esta opacificación se debe a la migración y proliferación de las células epiteliales cristalinianas residuales de la zona anterior y ecuatorial. El traumatismo que supone para el cristalino la extracción extracapsular, provoca la liberación del sistema de inhibición por contacto entre las células y, por tanto, conduce a la proliferación celular acelerada (2,3).
Numerosos factores han sido relacionados con la incidencia de la opacificación capsular (4). Entre éstos se encuentra el material de fabricación de la lente y su diseño. Según algunos autores esta incidencia es menor tras la implantación de lentes de PMMA que con las de silicona (5-7) otros muestran lo contrario (8,9) y algunos obtienen tasas similares de opacificación entre ambos materiales (10).
Hemos realizado un estudio de la incidencia de opacificación de la cápsula posterior con tres modelos de lente implantadas en saco, de óptica y tamaños similares, que difieren en el material de fabricación y el diseño de los hápticos.
Material y métodos
Este estudio retrospectivo incluye a 126 ojos en los que se realizó una extracción extracapsular del cristalino con técnica de facofragmentación manual o facoemulsificación, entre enero de 1994 y septiembre de 1995. Se seleccionaron aquellos casos en los que se realizó una capsulotomía circular continua e implantación de LIO intrasacular de pequeño tamaño (menor o igual a 13 mm), todas las lentes eran de óptica biconvexa de 6 mm.
Se dividieron en tres grupos según el modelo de la lente implantada:
Grupo 1 (n=37): AA4203 (STAAR) de silicona (RMX-3) con hápticos compactos planos de 0° de angulación y longitud total de 10,5 mm
Grupo 2 (n=44): SI30NB (Allergan) de silicona (SLM-2UV) con hápticos en C modificada de prolene con 10° de angulación y longitud total de 13 mm.
Grupo 3 (n=45): B60 125 (Biotech) de PMMA(PERSPEX CQ.UV) con hápticos en C modificada con 6° de angulación y longitud total de 12,5 mm.
Todos los procedimientos quirúrgicos fueron realizados por dos cirujanos con una técnica similar. Tras anestesia retrobulbar, se practicó una incisión corneal de 3,2 mm, capsulorrexis, hidrodisección, hidrodelineación y facoemulsificación intrasacular. Se continuó con la ampliación de la incisión entre 3,5 y 6 mm según la lente a implantar, relleno del saco con viscoelástico, implante intrasacular de la LIO sin utilizar inyectores, lavado de cámara anterior, y cierre de la incisión con uno a tres puntos radiales de Nylon 10/0.
En los casos en los que se realizó facofragmentación manual el procedimiento inicial fue similar. Después, se prosiguió con la luxación del núcleo a cámara anterior, fragmentación con trisector, extracción de los fragmentos con cánula de cesta-punta y aspiración irrigación manual de los restos corticales.
Todos los pacientes recibieron el mismo tratamiento postoperatorio con colirio de polimixina, neomicina y prednisolona, durante dos meses.
Los pacientes fueron revisados entre los 17 y los 39 meses de la cirugía. Se comprobó, en la historia clínica, la agudeza visual en el momento del alta y otras incidencias significativas del postoperatorio. Se realizó una exploración oftalmológica completa de los pacientes. Tras la midriasis farmacológica, dos observadores examinaron mediante biomicroscopia la localización de la LIO y clasificaron la opacidad de la cápsula posterior en cuatro grados. Se realizó una valoración mixta, teniendo en cuenta tanto la intensidad de la opacidad como la disminución de la agudeza visual respecto al alta, quedando establecidos los siguientes grados:
- Grado 0: no opacificada.
- Grado 1: opacificación ligera; se incluyeron las opacidades centrales o paracentrales correspondientes a una fina capa de perlas de Elschnig o una ligera fibrosis, que no producían disminución de la agudeza visual o como máximo la disminuían en 1 línea.
- Grado 2: Opacificación moderada; opacidades centrales de mayor intensidad que las ligeras, que producían una disminución de la agudeza visual como máximo de 3 líneas.
- Grado 3; Opacificación severa; opacidades centrales producidas por un recubrimiento grueso de perlas de Elschnig o una fibrosis marcada, que producía una disminución de la agudeza visual de más de 3 líneas.
Los pacientes que en el momento del control tenían realizadas capsulotomías YAG, se clasificaron según la agudeza visual previa a ésta.
Los motivos de exclusión del estudio fueron la localización de la LIO en sulcus, complicaciones intraoperatorias, pacientes con patología ocular inflamatoria crónica, patología retiniana evolutiva o acontecida entre la cirugía y el momento del control que alterara la valoración de la agudeza visual en los casos de opacidades moderadas o severas.
La edad media global de los pacientes era de 65,66±10,77 años y el seguimiento medio de 28,53±6,86 meses, con un tiempo mínimo de 17 meses y máximo de 44. La distribución de estos datos por cada grupo se recoge en la tabla I. Existían diferencias significativas tanto en la edad de los pacientes de los grupos, como en el tiempo de seguimiento.

Para controlar los sesgos, producidos por estas diferencias, se realizó un análisis multivariante tipo regresión logística según el procedimiento "forward stepwise", del programa SPSS para MS Windows Release 6.0. Se consideraron significativos valores de p<0,05.
Resultados
La incidencia de los distintos grados de opacidad en cada grupo del estudio se representa en la figura 1.
Considerando las opacidades con relevancia clínica (es decir, la suma de moderadas y severas), éstas se produjeron en el 21,62% del grupo1, en el 18,18% del grupo 2, y en el 15,56% del grupo 3 (fig. 2).
Para el análisis de regresión logística se tomó como variable dependiente la opacidad, y se construyó el modelo multivariante según el procedimiento "forward stepwise". Tanto el seguimiento (p=0,0007), como la edad (p=0,0071) entraron en el modelo de regresión (tabla II). También el tipo de lente (p=0,0279) fue incluido en la ecuación final, considerando que la lente AA 4203 supone un factor de riesgo de mayor frecuencia de opacificación que la lente B60152 y la SI30NB. El tipo de intervención no fue incluido en la ecuación de regresión final, lo que implica que no es un factor significativo en este análisis.

Discusión
Existe en la literatura gran variabilidad respecto cuál es la incidencia real de la opacificación de la cápsula posterior. Esto es debido a los numerosos factores, algunos no bien comprendidos, que influyen en el desarrollo de la opacificación y especialmente a la dificultad de cuantificar objetivamente esta opacidad. Se han propuesto diversos métodos para medir el grado de opacificación pero hasta el momento ninguno ha sido universalmente aceptado. Algunos autores han utilizado fotografías mediante retroiluminación teniendo en cuenta la densidad de la opacificación y el área afectada (11), otros cuantificando el área opacificada con un sistema de análisis de imagen (12,13). En nuestro estudio hemos pretendido realizar una valoración mixta entre la opacidad objetivable mediante biomicroscopia y la pérdida de agudeza visual del paciente.
La mayoría de los estudios cuantifican la opacificación según el número de capsulotomías YAG. En ese sentido, quizá la incidencia encontrada en este trabajo pueda ser mayor que la descrita en otros, ya que no todos los pacientes valorados como opacidad clínicamente relevante eran candidatos de capsulotomía en el momento del estudio.
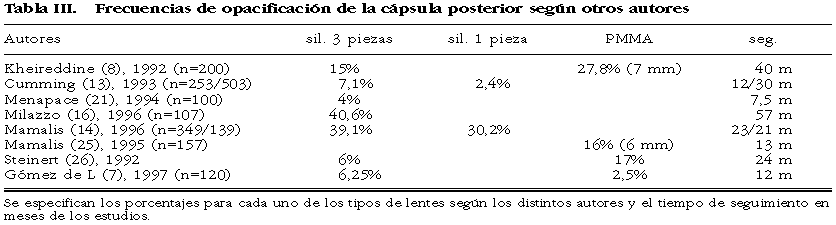
Según el material y el diseño empleado en la manufactura de las LIO se han publicado diferentes porcentajes de opacificación capsular (tabla III). Cumming (14) encuentra una incidencia superior en las lentes de silicona de 3 piezas (7,1%, a los 12 meses) que en las de una sola pieza (2,4%, a los 30 meses). Mamalis (15), no encuentra diferencias significativas entre estos mismos tipos de lentes, aunque la lente de tres piezas se opacifica con mayor frecuencia.
El mayor porcentaje de opacificaciones en nuestro estudio correspondió a la lente tipo Mazzocco de Staar. Estos resultados parecen significativos según el análisis de regresión logística, que tiene en cuenta el distinto tiempo de seguimiento y edad de los tres grupos. No obstante, pensamos que estas diferencias pueden deberse más al diseño de los hápticos de la lente y a su angulación, que al material con que está fabricada.
Algunos autores sostienen que la adhesión de las cápsulas es un factor protector para el desarrollo de opacidad; así, esta fusión supondría una barrera para las células que migran principalmente desde la zona ecuatorial y que no podrían invadir el área central de la cápsula (12). Las lentes con hápticos compactos planos no permiten la fusión capsular circunferencial, ya que las porciones de cápsula por encima y debajo de éstos no se adhieren, pudiendo suponer una vía de acceso de las células ecuatoriales a la zona central capsular (16) (figs. 3 y 4). Los 0° de angulación de los hápticos, y el pequeño tamaño de esta lente pueden provocar que la cápsula posterior no esté tensa y por tanto que exista un espacio retrolental que favorezca la migración de las células epiteliales. No obstante, Cumming (14) indica que la contracción del saco capsular favorece la flexión anterior de los hápticos y, de esta manera, forzaría el desplazamiento posterior de la óptica sobre la cápsula creando una firme aposición entre ambas superficies.
Aunque hemos realizado un análisis multivariante para eliminar los efectos del distinto seguimiento y edad entre los grupos, hemos de tomar los resultados de este estudio con cierta cautela. Por una parte, porque el seguimiento medio ha sido de 28 meses, y en algunos casos, de tan sólo 17, y algunos autores han comunicado la incidencia máxima de capsulotomías al cuarto año (17). Y por otra, porque al no ser un ensayo aleatorio, puede haber otros factores que influyan en los resultados y que no hemos tenido en cuenta; por ejemplo, la localización del límite de la capsulotomía anterior, considerada por algunos autores (18-21) como un factor determinante en el desarrollo de la opacidad de la cápsula posterior.
Respecto a este último punto, Ravalico (18) que estudia la influencia del tamaño de la capsulorrexis en la opacificación, apunta que no es suficiente la barrera protectora que se forma por la fusión capsular. Sostiene que hay una menor opacificación en los casos en los que el límite de la cápsula anterior está sobre la óptica de la lente; este efecto se explicaría por la tendencia a la transformación fibrosa del borde de la capsulorrexis, que ejercería una fuerza contráctil centrípeta, tensando la cápsula posterior y provocando una mayor adhesión a la óptica de la lente. Menapace (22) señala que en los casos en los que el límite de la capsulorrexis corre paralelo al borde de la óptica, la fibrosis que se produce a la largo de éste tiende a invadir la cápsula posterior; por eso considera que la capsulorrexis ideal debe ser 0,5 a 1 mm menor de la óptica. Hervás (21), indica que una forma de prevenir la opacificación por metaplasia fibrosa sería evitar que cualquier parte del borde de la capsulotomía entrara en contacto con la cápsula posterior.
Hemos encontrado en algunos de los pacientes con lentes SI30 y B 60125, que si la capsulorrexis no estaba bien centrada sobre la óptica, o existía una captura de la misma (fig. 5), la zona en la que estaban en contacto las cápsulas por fuera de la óptica era un posible lugar desde el que se iniciaba la opacificación (fig. 6). De hecho, una gran parte de las opacificaciones clasificadas como ligeras en este tipo de lentes correspondían a esta situación; por contraposición, las opacificaciones ligeras de la lente de Staar se debían en muchos casos al inicio de una monocapa de perlas de Elschnig desde los hápticos.
En definitiva, queda patente que los métodos quirúrgicos no consiguen eliminar las células residuales capsulares. Tampoco el interponer una barrera mecánica tipo anillo ha conseguido detener la proliferación y migración celular (2). Los esfuerzos en la prevención de la opacificación van encaminados en la actualidad hacia la investigación de sistemas de liberación sostenida de fármacos (23-25).
Resumen
Objetivo. Evaluar retrospectivamente la incidencia de la opacificación de la cápsula posterior en ojos en los que se implantó intrasacularmente tres tipos de lentes intraoculares de óptica y tamaño similares a lo largo de 28 meses.
Métodos. Se examinaron, para evaluar la incidencia de opacificación de la cápsula posterior, ciento veintiséis ojos, que habían sido intervenidos de cataratas con capsulorrexis e implante de uno de los siguientes tipos de lente: AA 4203 (Staar), SI 30NB (Allergan) o B60125 (Biotech). El grado de opacidad se clasificó en ligera, moderada y severa.
Resultados. Con un seguimiento medio de 23 meses en el grupo de la lente de Staar, de 31 en el grupo de la lente de Allergan y de 30 en la de Biotech, la incidencia de opacificación capsular relevante fue respectivamente de 21,62%, 18,18% y 15,56%. Los resultados del análisis estadístico concluyeron que tanto el tiempo de seguimiento, como la edad y el tipo de lente, estaban relacionados significativamente con la opacidad de la cápsula posterior.
Conclusión. Aunque la proporción de pacientes con opacidad de la cápsula posterior con lente intraocular de una pieza (Staar), fue superior a los otros dos grupos, estas diferencias parecen estar relacionadas más con el diseño de la lente que con el material de fabricación.
Palabras clave
Opacificación de la cápsula posterior, cirugía de la catarata por pequeña incisión, lente intraocular de PMMA, lente intraocular de silicona.
Summary
Objective. To retrospectively evaluate the incidence of posterior capsule opacification (PCO) in eyes receiving one of three types of capsular-bag-fixated intraocular lenses with similar optic and size over 28 months.
Methods. One hundred twenty-six eyes that had cataract extraction with a capsulorhexis and implantation of one of the next three kinds of intraocular lens: AA4203 (Staar), SI 30NB (Allergan) or B60125 (Biotech), were evaluated to assess the incidence of PCO. The opacity degree was clasificated as slight, moderate and severe.
Results. With an average follow-up of 23 months in the Staar group, 31 in the Allergan IOL group and 30 in the Biotech group, the incidence of PCO was 21.62%, 18.18% and 15.56%, respectively. These differences were statistically significant and related to time of follow-up, age of the patients and IOL type.
Conclusion. Although the proportion of patients with a one-piece silicone IOL (Staar) was higher than the other two groups this diference appears to be related to the lens design rather than the material of manufacture.
Key words
Posterior capsule opacification, small incision cataract surgery, PMMA IOL, silicone IOL.
Bibliografía