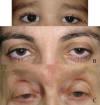
Fig. 1. Ptosis aponeuróticas. A: Leve izquierda (izda.); B: Moderada bilateral; C: Grave bilateral.
COMUNICACIÓN SOLICITADA
MATEOS SÁNCHEZ E1, ARRUABARRENA SÁNCHEZ C2, ALBANDEA JIMÉNEZ A3, ALONSO FORMENTO N3, KASBO B
41
Jefe de Sección de la Unidad de Párpados, Órbita y Dacriología. Hospital Ramón y Cajal. Madrid.INTRODUCCIÓN
Denominamos ptosis palpebral a la posición anormalmente baja del párpado superior (PS). El margen del párpado superior normal, en su zona central y con la mirada en posición primaria, se sitúa 1-2 mm por debajo del limbo esclerocorneal. El descenso del párpado se traduce en un estrechamiento de la hendidura palpebral que, según el grado, puede llegar a ocluir el eje visual.
Las ptosis se clasifican, según su etiología, en: miogénicas, aponeuróticas, neurogénicas, traumáticas y mecánicas.
En esta comunicación vamos a centrarnos en las ptosis aponeuróticas que son aquellas que se producen por desinserción, adelgazamiento o dehiscencia de la aponeurosis del músculo elevador del párpado superior (EPS), en su contacto con la placa tarsal. En la ptosis aponeurótica el músculo elevador se encuentra bien desarrollado, con capacidad para contraerse y relajarse normalmente; el defecto está solamente en la aponeurosis. Ocurre lo contrario en las ptosis miogénicas que se deben a un defecto en el desarrollo de dicho músculo, por lo que este es incapaz de relajarse y de contraerse de forma adecuada.
EPIDEMIOLOGÍA
En nuestra experiencia la ptosis aponeurótica es la forma más frecuente de todas las ptosis palpebrales, siendo entre ellas las aponeuróticas adquiridas las que más atención generan en la práctica clínica diaria (1). En otras series la colocan ligeramente por detrás de las miogénicas (2).
En los últimos 5 años hemos operado más de 500 pacientes con ptosis palpebral; de éstas el 75% son de origen aponeurótico, el 20% de origen miogénico y el resto incluye las neurogénicas, mecánicas y traumáticas. Prácticamente todos los pacientes con ptosis aponeurótica la padecían en ambos lados y la cirugía fue realizada bilateralmente en el mismo acto quirúrgico.
El aumento de la esperanza de vida, la expansión de las relaciones sociales, el culto a la belleza, y el mejor conocimiento y desarrollo de la técnica quirúrgica ha dado lugar a un gran incremento de la demanda en el tratamiento de esta patología.
CLASIFICACIÓN
Las Ptosis se clasifican por una parte según el grado y por otra según la etiología.
Según el GRADO (3):
Leves cuando el PS se sitúa 2 mm por debajo de su posición normal.
Moderadas cuando el párpado desciende 3-4 mm.
Graves cuando el descenso es mayor de 4 mm, pudiendo llegar a ocluir la pupila (fig. 1).

Fig. 1. Ptosis aponeuróticas. A: Leve izquierda (izda.); B: Moderada bilateral;
C: Grave bilateral.
Según su ETIOLOGÍA (tabla 1):
Miogénica.
Aponeurótica.
Neurogénicas.
Mecánicas.
Traumáticas.

Trataremos exclusivamente las ptosis aponeuróticas porque, además de ser las más frecuentes, presentan un gran interés médico y social.
Las ptosis aponeuróticas se clasifican a su vez en:
1) Aponeuróticas involutivas.
2) Aponeuróticas congénitas.
3) De portadores de lentes de contacto.
4) De frotadores crónicos.
5) Aponeurótica familiar tardíamente adquirida.
6) Del síndrome de blefarocalasia.
7) De la orbitopatía tiroidea, las cavidades anoftálmicas, y los estados gravídicos, entre otros.
Dentro de todos estos subgrupos la más frecuente es la Aponeurótica Involutiva, seguida de la que aparece en portadores de lentes de contacto y frotadores crónicos (así lo hemos detectando a lo largo de nuestra trayectoria oftalmológica).
Aunque la ptosis aponeurótica congénita es una entidad que a priori puede parecer rara, en un estudio realizado en 340 pacientes menores de 16 años encontraban un 5% de ptosis de etiología aponeurótica (4). Nuestra experiencia también confirma estos datos.
ETIOPATOGENIA
La ptosis aponeurótica se debe a una alteración en la unión entre la aponeurosis del EPS y la placa tarsal. En los casos adquiridos, la aponeurosis se debilita, se alarga y adelgaza dando lugar a la desinserción parcial o total de la misma en su unión con el tarso.
En los últimos años se ha evidenciado la importancia del músculo de Müller en la posición del EPS. Hay datos que confirman que se puede mantener una apertura palpebral normal a pesar de existir una desinserción casi completa de la aponeurosis del EPS siempre que el músculo de Müller esté intacto y funcione correctamente; pero con el tiempo la desinserción del EPS causa un debilitamiento del Müller y aparece la ptosis (5). Existe teóricamente un mecanismo tónico involuntario de contracción del EPS que mantiene la apertura del PS. Según esta teoría el músculo de Müller actuaría como un huso muscular del EPS, el estiramiento del Müller al descender el PS activaría la contracción del EPS manteniendo la apertura (6). Así en los primeros estadios de la desinserción de la aponeurosis la apertura palpebral se mantiene mientras está intacto el Müller. La ptosis del PS aparece cuando por efecto del alargamiento mantenido el músculo de Müller pierde no sólo su acción elevadora del PS mediada por la vía simpática, sino también su actividad como huso muscular del EPS.
El debilitamiento de la aponeurosis ocurre de forma fisiológica, en las personas de edad avanzada, generalmente a partir de los 60 años, como causa de envejecimiento. Son habitualmente bilaterales, moderadas o graves y se denominan ptosis aponeuróticas involutivas; son las formas más frecuentes (fig. 2). Otros pacientes en la edad media de la vida, alrededor de los 40 años, presentan ptosis aponeuróticas de características similares a las involutivas: se cree que se debe a factores predisponentes heredados que hacen que la ptosis se presente de forma precoz en el tiempo, son las ptosis hereditarias tardíamente adquiridas. En estos casos siempre se encuentran varios miembros de la familia afectados (fig. 3).
![]()
Fig. 2. Ptosis involutiva en paciente mayor de 80 años.
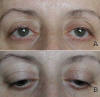
Fig. 3. A: Ptosis hereditaria tardíamente adquirida bilateral leve; B: Surcos
elevados y dermatocalasia.
El síndrome de blefarocalasia es una alteración infrecuente de etiología no bien conocida que cursa con episodios repetidos de inflamación palpebral muy llamativos y de corta duración. Se presenta en la adolescencia y con el paso de los años va disminuyendo la frecuencia de los episodios. Da lugar a una atrofia grave de las estructuras palpebrales, piel delgada y telangiectásica, desinserción de los cantos y de la aponeurosis, con ptosis y prolapso de la glándula lagrimal. Son ptosis muy graves y difíciles de tratar. El edema o inflamación intenso y mantenido de forma crónica del PS es el responsable de tanta y tan grave alteración. Afortunadamente este síndrome es poco frecuente (fig. 4).
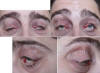
Fig. 4. Síndrome de Blefarocalasia. A: Ptosis muy grave. Atrofia generalizada,
piel fina y telangiectásica, desinserción de los cuatro cantos; B: A pesar de
contraer fuertemente el músculo (m) frontal sólo consigue dejar libre el eje
visual izdo.; C y D: Vistas laterales.
En las embarazadas que presentan retención de líquido y en la orbitopatía tiroidea con inflamación palpebral mantenida puede aparecer también una ptosis aponeurótica. Las cavidades anoftálmicas presentan con frecuencia ptosis por disminución del volumen y pérdida de soporte del párpado. Además en estos casos se suma el proceso inflamatorio que acompañó a la causa que ha dado lugar a la pérdida del globo ocular (fig. 5).
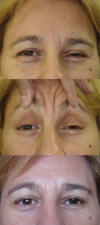
Fig. 5. A: Ptosis izda. leve en cavidad anoftálmica; B: Siempre el surco está
más alto; C: Postoperatorio.
Hay un grupo muy importante de ptosis aponeuróticas que se deben a irritación física de los párpados, (7) como es el caso de los frotadores crónicos, de los usuarios de lentes de contacto y de algunos pacientes que han sufrido cirugía del segmento anterior. El frotamiento de los PS puede realizarse en cualquier momento del día y por causas diversas: al despertarse por las mañanas, con el llanto, con el picor ocular (conjuntivitis alérgicas, dermatitis atópicas y ojo seco), al desmaquillarse o simplemente por costumbre. Nosotros observamos en consulta muchos pacientes que se frotan violentamente los ojos de forma rutinaria y sin ningún respeto a las estructuras palpebrales y al globo. Ellos solos se provocan la aparición de ptosis, y dermatocalasia (fig. 6).

Fig. 6. Paciente joven frotadora crónica. Presenta ptosis y dermatocalasia.
Los usuarios de lentes de contacto, sobre todo con las rígidas, presentan también mayor frecuencia de frotamiento y tracciones palpebrales durante la colocación y retirada de las lentes y aumento de la fricción del PS con la superficie del globo. El grado de ptosis en este grupo de pacientes se relaciona con la duración del uso de las lentes de contacto y se presenta en pacientes relativamente jóvenes (fig. 7). La cirugía del segmento anterior presenta una incidencia de ptosis entre el 1 y el 6,7% (8), se ha descrito en cirugía de catarata, queratoplastia, cirugía filtrante (no sólo por la agresión del blefarostato sino también en relación con ampollas de filtración redundantes) y con cirugía refractiva corneal (9).
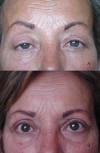
Fig. 7. Portadora de lentes de contacto rígidas. A: Ptosis y elevación de las
cejas; B: Después de la cirugía se ha normalizado la altura de los párpados y
las cejas.
Las ptosis aponeuróticas congénitas están descritas desde 1979, Anderson et al (10) en una serie de 46 párpados ptósicos congénitos que fueron explorados quirúrgicamente encontraron 3 casos de desinserción de la aponeurosis que se corrigieron satisfactoriamente con cirugía de reinserción de la misma. Se ha descrito una alteración en el desarrollo mesodérmico que daría lugar a un fallo en la colocación distal de la aponeurosis en la placa tarsal (11).
Detectamos frecuentemente esta desinserción congénita en niños; ya la sospechamos clínicamente en la consulta y más tarde la comprobamos en el momento de la cirugía. Creemos que el porcentaje de niños afectados de desinserción congénita supera los descritos en los estudios publicados (fig. 8).
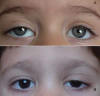
Fig. 8. Ptosis aponeuróticas congénitas. A: En lado derecho; B: En lado izdo.
Hace poco tiempo, al hacer una revisión sobre el efecto que puede causar en los párpados el hecho de frotarse de forma mantenida, encontramos en la red vídeos de ecografías tridimensionales donde perfectamente se aprecia cómo un feto se frota insistentemente el párpado derecho (12). Este dato puede justificar también que en el momento del nacimiento ya presenten la desinserción o estiramiento de la aponeurosis, y que la caída del párpado con frecuencia sea mayor en el lado temporal. No es infrecuente detectar ptosis oblicuas (figs. 9 y 10).

Fig. 9. Ptosis congénitas aponeuróticas oblicuas. Siempre mayor en lado
temporal.

Fig. 10. Ptosis oblicua antes y después de la cirugía. A: Mayor en lado
temporal; B: Surco más alto; C: Buena función del m. elevador; D:
Postoperatorio, surco a la misma altura que el derecho; E: Altura de párpados
superiores simétricas.
También existen casos de ptosis aponeuróticas infantiles adquiridas que se relacionan con el frotamiento excesivo de los parpados con el llanto, o con sensación de sueño.
CLÍNICA
El aspecto del paciente que presenta una ptosis aponeurótica es variado y generalmente inconfundible pero no siempre acuden a la consulta refiriendo que la padecen.
Los casos leves y algunos moderados, cuando son bilaterales, pueden pasar desapercibidos tanto para el médico como para el paciente ya que, al ser la función del EPS generalmente muy buena, el paciente puede compensarla incluso de forma involuntaria (fig. 11).
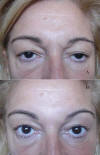
Fig. 11. Ptosis bilateral. La paciente desconocía su patología; B: Gesto
habitual, compensaba la ptosis contrayendo las cejas.
La ptosis unilateral es más difícil que pase inadvertida por la asimetría que provoca.
Cuando la ptosis es grave el paciente acude a la consulta solicitando el tratamiento sin demora, pues los síntomas son muy molestos: además del deterioro físico se produce reducción del campo visual superior, cefaleas por contracción forzada y mantenida del músculo frontal, cervicalgias porque compensan la ptosis elevando el mentón, e imposibilidad de realizar la lectura de forma prolongada (fig. 12). Otras veces elevan los párpados con los dedos y en alguna ocasión llegan a utilizar una tira de esparadrapo para sujetar las cejas (fig. 13).
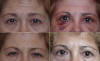
Fig. 12. A: Durante muchos años los analgésicos no calmaron sus cefaleas. Surcos
de la frente muy pronunciados; B: Ptosis bilateral al relajar la frente; C:
Postoperatorio inmediato; D: Postoperatorio tardío. Han desaparecido las
cefaleas.
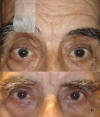
Fig. 13. A: Ptosis que el paciente corrige con un esparadrapo traccionando de
párpado y ceja; B: Tras la cirugía.
Ocasionalmente la queja de los pacientes es solamente estética, la ptosis da aspecto de aburrido, cansado, triste (fig. 14). Muchas veces nos encontramos con ptosis exageradas que contraen fuertemente el músculo frontal intentando dejar el eje visual libre, que llevan varios años de evolución y que no se habían decidido a operar por miedo porque creen que no podrán cerrar los ojos después de la cirugía (fig. 15).

Fig. 14. Aspecto cansado y triste secundario a ptosis.
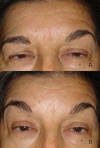
Fig. 15. A: Ptosis que ocluye el eje visual; B: Contracción muy forzada para
despejar el campo visual.
Alguna vez pueden no referir nada, solamente se presentan con la expresión que delata la ptosis (fig. 16).
![]()
Fig. 16. Aponeurótica infantil. A: Manteniendo este gesto disimula muy bien la
ptosis; B: Ptosis manifiesta al relajar la frente.
No es raro ver una retracción palpebral en el lado sano enmascarando la ptosis del párpado contralateral (Ley de Hering) (fig. 17).
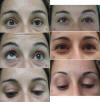
Fig. 17. A: Retracción derecha, ptosis izda.; B: Portadora de prótesis ocular
que limita la elevación del globo pero no la elevación del párpado; C: Surco
izdo. más alto; D: Al día siguiente a la cirugía del izdo. muestra ligera
inflamación; E: Un mes más tarde; F: Se ha normalizado también el surco izdo.
Otras veces el paciente refiere que se le cierran los ojos pero lo único que padecen es un exceso llamativo de piel que cubre los párpados e incluso las pestañas. Estos casos solamente requieren la realización de una blefaroplastia. En ellos la altura del surco palpebral es normal (fig. 18).
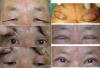
Fig. 18. Dermatocalasia en paciente oriental. Surco palpebral normal, no padece
ptosis. Corrección con una amplia blefaroplastia.
DIAGNÓSTICO
El diagnóstico de sospecha comienza ya en el momento de saludar al paciente y mirarle a los ojos, sin haber comenzado aún la exploración, porque muestran principalmente cuatro signos que les caracteriza a todos: La ptosis, el surco palpebral elevado, los pliegues de la frente muy marcados y las cejas más arqueadas. Es patente en personas mayores, pero también en niños.
El diagnóstico definitivo de la ptosis es clínico y se realiza por la exploración física detallada y por la anamnesis. Debemos interesarnos por la edad y la forma de comienzo. Muchos casos se presentan en el nacimiento pero la mayoría aparecen a lo largo de la vida. Los antecedentes que nos refiere el paciente son muy importantes pero debemos solicitar fotografías antiguas que nos serán de gran ayuda (para determinar la evolución).
Para valorar correctamente una ptosis es necesario conocer:
A. Los ojos con párpados normales
Para ello recordaremos brevemente algunos pequeños detalles anatómicos que nos parecen muy importantes:
1. La hendidura palpebral: espacio comprendido entre ambos párpados, tiene una altura central de aproximadamente 9-11 mm en la mujer y de 7-8 mm en el hombre. Su longitud alcanza los 30 mm.
2. El borde o margen del PS se encuentra 1-1,5 mm por debajo del limbo esclerocorneal superior.
3. El borde o margen del párpado inferior se sitúa tangente al limbo esclerocorneal a las VI horas.
4. La distancia margen-reflejo1 (DMR 1) es la distancia entre el reflejo luminoso de la linterna de exploración proyectado en la córnea en posición primaria de la mirada (PPM), y el borde palpebral superior. En condiciones normales es mayor de 3 mm (3-4 mm).
5. La distancia margen-reflejo 2 (DMR 2) es la distancia entre el reflejo luminoso de la linterna y el borde palpebral inferior y es de 5 mm.
6. El surco palpebral: situado normalmente a 10 mm del borde libre del PS. Este surco está formado por las fibras de la aponeurosis que, antes de llegar a insertarse en el tercio inferior de la cara anterior del tarso, emiten pequeñas ramificaciones que atraviesan el músculo orbicular insertándose en éste y en la dermis pretarsal. En la raza oriental el surco se encuentra muy cerca del margen palpebral, a unos 3 mm, porque la inserción de las fibras de la aponeurosis en la piel es muy baja.
Por su configuración curvilínea, la región nasal y temporal del surco están 2 y 1 mm respectivamente por debajo de la zona central.
7. El pliegue palpebral: en las personas jóvenes se identifica con el surco y no se aprecia en la infraversión; en las de edad media o avanzada se hace más intenso como consecuencia de la dermatocalasia y se hace manifiesto incluso en mirada extrema hacia abajo. Recordemos que la piel del párpado es la más fina que posee el ser humano y la dermis es muy escasa por lo que con el paso de los años se produce un adelgazamiento de la unión dermo-epidérmica y cambios importantes en el colágeno y elastina, lo que motiva una laxitud y exceso de piel con la aparición de los pliegues y arrugas.
8. El canto externo: normalmente queda 2 mm por encima del canto interno, lo que facilita la eliminación de la lágrima por el sistema excretor, y añade belleza al ojo (fig. 19 A, B y C).
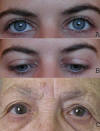
Fig. 19. Ojos con párpados normales, A y B: en persona joven; C: Paciente de
edad avanzada. No padece ptosis, solamente dermatocalasia por cambios
involutivos normales.
B. La exploración de los ojos que presentan ptosis aponeurótica
1. Disminución de la hendidura palpebral, uni o bilateral.
2. Descenso de uno o de ambos PS en PPM, por debajo de su posición normal.
3. Disminución de la DMR1. Las ptosis aponeuróticas involutivas suelen ser llamativas y aunque generalmente son bilaterales pueden presentarse de forma asimétrica.
4. El párpado se encuentra elongado verticalmente y adelgazado y a través de él pueden trasparentarse las estructuras del globo ocular.
5. El surco palpebral se encuentra elevado como consecuencia de la pérdida de la inserción de la aponeurosis en el tarso. En las ptosis involutivas graves el surco llega a perderse pues la aponeurosis se desplaza en exceso hacia la órbita, y la grasa orbitaria se atrofia, apareciendo lo que se ha dado en llamar «surco cadavérico». Este calificativo no es de nuestro agrado, pues puede herir la sensibilidad del paciente cuando escuchan nuestros comentarios con los médicos en formación. Nosotros preferimos denominarlo: «surco profundo» (fig. 20).
![]()
Fig. 20. A: Ptosis llamativa; B: Surcos altos y profundos, rebordes orbitarios
muy marcados, cejas arqueadas; C: Aspecto después de la cirugía.
6. El pliegue generalmente es visible, tanto en PPM, como en infraversión.
7. La función del EPS se encuentra conservada (fig. 21), lo que la distingue de las ptosis miogénicas en las que la elevación es defectuosa por dificultad de contracción del EPS. En la mirada arriba la ptosis aponeurótica mejora ya que el reflejo involuntario de contracción del músculo elevador se mantiene, mientras que en la ptosis miogénica congénita este reflejo se encuentra alterado y en la mirada arriba el párpado se eleva menos de lo normal (14).
![]()
Fig. 21. A: Los párpados parecen muy largos; B: Buena función de la elevación;
C: Descienden en exceso.
Cuando la aponeurosis está muy retraída hacia la órbita la función del elevador puede parecer mala, de una parte por la misma desinserción y de otra porque al ser la ptosis muy exagerada y ocluir el eje visual el paciente es incapaz de seguir la luz de la linterna en la exploración (fig. 22).
![]()
Fig. 22. A: Estado depresivo y cefaleas por ptosis; B: durante muchos años
padece dificultad para abrir los ojos; C: postoperatorio inmediato; D:
postoperatorio tardío.
La función del EPS se mide como la excursión que realiza el borde del PS desde la mirada inferior extrema hasta la elevación completa y en condiciones normales es de 15 mm. A efectos prácticos de cara a la cirugía se define como una función excelente si el PPS se desplaza 13 mm o más, muy buena si el desplazamiento es de 10-12 mm, buena si está entre 7 y 9 mm, mala de 4 a 6 mm y nula cuando es inferior a 4 mm. Es muy importante en estos casos hacer la valoración de los pacientes bloqueando la acción del músculo frontal, ya que en ocasiones la tracción del frontal enmascara ptosis leves o altera la valoración de la función del elevador (fig. 23).
![]()
Fig. 23. A y B: Medida de la función del músculo elevador. En este caso es
excelente.
En los niños con ptosis aponeuróticas congénitas hay que determinar si cubren el eje pupilar por la posibilidad de causar ambliopía. La ambliopía aquí es menos frecuente que en la miogénica, porque en estos niños el grado de ptosis es menor y la función del elevador buena.
8. En la mirada abajo el párpado ptósico desciende más que un párpado sano, al contrario que en las ptosis miogénicas congénitas en las que el párpado en la mirada abajo se queda rezagado. El mal desarrollo del EPS en estas últimas se traduce tanto en dificultad para contraerse como para relajarse.
9. El canto externo es de aspecto laxo y muchas veces lo encontramos desinsertado y descendido. Por este mismo motivo puede asociarse entropión o ectropión (fig. 24).
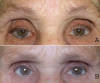
Fig. 24. Ptosis aponeurótica bilateral y entropión párpado inferior del ojo
derecho.
Al valorar la ptosis es muy importante determinar en los casos que parecen ser unilaterales lo que llamamos el ojo director, para evaluar que ocurriría si se realiza cirugía sobre un único párpado. Los párpados mantienen unos movimientos simétricos ya que los dos músculos elevadores funcionan como dos músculos yunta y cumplen la ley de Hering, de tal forma que el ojo dominante o director determina la cantidad de estímulo recibido. Así, cuando el ojo dominante presenta una ptosis latente el contralateral se encuentra retraído; si es una ptosis manifiesta el contralateral puede presentar una ptosis latente; y si el dominante está retraído el contralateral puede presentar una ptosis. Si sólo se corrige el párpado que parece ptósico, es posible que al disminuir el tono inervacional, tras la cirugía, el párpado contralateral descienda. Para intentar prevenir este fenómeno se explora a los pacientes elevándole el párpado que va a ser intervenido y mirando si con ello desciende el párpado contralateral (fig. 25). En este caso deben operarse los dos párpados. Hay un estudio que dice que esta prueba no tiene buena correlación con los resultados postoperatorios (15), por ello recomendamos que en aquellos casos que se vaya a realizar cirugía unilateral se informe de la posibilidad de que en el postoperatorio aparezca una ptosis del párpado contralateral.

Fig. 25. A: Sospecha de ptosis bilateral, no detectada por los padres, ceja
izda. más alta; B: Ptosis manifiesta en ojo izdo. dominante; C: Ptosis latente
derecha.
Dedicar el tiempo necesario para realizar una buena exploración nos permite llegar a un diagnóstico correcto, sin confundirlas con las miopáticas; ahorrando así realizar pruebas complementarias neurológicas, de imagen o de laboratorio, que son molestas, caras y, en estos casos, innecesarias.
Recogeremos en la historia clínica una tabla resumen con las medidas más importantes (tabla 2). También aconsejamos recoger documentación gráfica de cada paciente, imprescindible realizar al menos un dibujo esquemático de la situación de los párpados y siempre realizar fotografías, en las posiciones diagnósticas. Cualquier detalle de los párpados será de gran valor. Estudiar las fotografías antes y después de la cirugía aporta muchas enseñanzas. Nosotros hacemos y guardamos fotografías de todos y cada uno de los pacientes que se van a operar. Volvemos a realizar fotos en el postoperatorio inmediato, una o dos más a lo largo del primer mes y, por último, en el momento del alta.

TRATAMIENTO
El tratamiento de las ptosis aponeuróticas es quirúrgico y siempre realizamos la cirugía con microscopio. Preferimos la anestesia local siempre que la edad del paciente lo permita, porque así podemos localizar fácilmente la aponeurosis, aunque se encuentre muy retraída hacia la órbita, y ajustar, de manera más fiable la altura y simetría palpebral. Cuando la ptosis es bilateral corregimos los dos párpados en el mismo acto quirúrgico. Recalcamos que en la ptosis aponeurótica no debe realizarse ningún tipo de resección, como mucho podemos realizar un avance de la aponeurosis, en el momento de insertarla, de no más de 5-6 mm si además de desinsertada se encuentra elongada
Contamos con dos tipos de cirugía: A) Reinserción de la aponeurosis en el tarso por vía anterior y B) Resección en bloque de la conjuntiva y del músculo de Müller (Conjuntivo-Müllerectomía).
Técnica de Reinserción de la aponeurosis
La técnica quirúrgica no presenta dificultades si se conocen bien los planos anatómicos, pues se trata solamente de reinsertar la aponeurosis en la cara anterior del tarso, llevándola a su posición original. Nunca aquí debemos resecar la aponeurosis porque de lo contrario conseguiríamos una hipercorrección.
Utilizamos una infiltración anestésica con una mezcla de lidocaína al 2% con adrenalina al 1:100.000 y bupivacaína al 0,5%. Evitaremos la adrenalina en pacientes con enfermedad coronaria o enfermedad de Graves.
Los pasos que seguimos son:
1. Marcado del surco palpebral con un rotulador dermográfico con el paciente sentado y dirigiendo la mirada ligeramente hacia abajo. En ptosis unilaterales se marca a la misma altura que en el lado opuesto. Si la ptosis es bilateral marcamos en la zona central a 8-9 mm del borde palpebral en la mujer y a 6-7 mm en el hombre, y seguimos la línea curva normal del surco.
2. Si además de la ptosis también presentan dermatocalasia: valoramos toda la piel redundante y la marcamos.
3. Infiltración anestésica en piel, procurando evitar el orbicular para no crear hematoma.
4. Colocación de protector de globo.
5. Incisión en piel y orbicular a lo largo de la zona marcada en el surco, utilizando un terminal de bisturí eléctrico con punta de colorado (fig. 26). Si además presentan dermatocalasia (muy frecuente en ptosis involutiva), realizamos una blefaroplastia en la zona diseñada previamente (fig. 27).
![]()
Fig. 26. Incisión de piel y orbicular, con punta de Colorado, a todo lo largo de
la línea marcada.
![]()
Fig. 27. Incisión para blefaroplastia.
6. Resección de piel y orbicular con cuidado para no lesionar el septum orbitario (fig. 28).
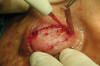
Fig. 28. Se reseca la piel y el orbicular incluidos en la zona marcada,
traccionando hacia arriba para no lesionar el septum orbitario.
7. Resección de bolsas grasas orbitarias si se encuentran herniadas, teniendo cuidado de coagular los vasos para prevenir el sangrado.
8. Debajo del orbicular encontramos el septum orbitario con la grasa preaponeurótica que se hará visible al presionar ligeramente el globo (fig. 29).
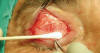
Fig. 29. Septum orbitario y grasa preaponeurótica; detrás se trasparenta la
aponeurosis que como se encuentra desinsertada y retraída, permite visualizar el
m. de Müller con la arcada vascular periférica.
9. Disección de las fibras del septum que se fusionan a la aponeurosis. Rechazamos el septum junto con la grasa preaponeurótica hacia el reborde orbitario, con un retractor de Desmarres.
10. Inmediatamente debajo se encuentra la aponeurosis que se muestra como una banda de color nacarado que la hace inconfundible. Como está desinsertada la encontramos siempre separada del tarso, y desplazada hacia arriba dejando visible al músculo de Müller, rojo y con la arcada vascular periférica sobre él (fig. 30). Debajo del Müller y bien adherida, se encuentra la conjuntiva palpebral a través de la cual podemos observar cómo se trasparenta la córnea.
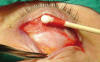
Fig. 30. Al rechazar el septum se expone la banda marcada de la aponeurosis. Se
observa la gran distancia que la separa del tarso.
11. La aponeurosis se desplaza arriba y abajo con los movimientos del globo; podremos reconocerla fácilmente pidiendo al paciente que mueva el globo hacia esas posiciones. Cuando se encuentra muy desinsertada y retraída hacia la órbita es más difícil su localización, de ahí la importancia de la anestesia local para que podamos solicitar la colaboración del paciente.
12. Generalmente nos encontramos con aponeurosis muy finas, y en ocasiones deshilachadas e infiltradas de grasa (las de origen miogénico tienen la aponeurosis engrosadas y fibrosas). Podemos también encontrar grasa debajo de la aponeurosis (fig. 31). Otras veces se encuentran menos debilitadas.
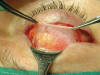
Fig. 31. Aponeurosis traccionada con pinzas. Es fina y está infiltrada de grasa.
Se han descrito estas diferencias en el grosor en las ptosis congénitas y en las aponeuróticas medidas con biomicroscopía ultrasónica, siendo la aponeurosis en estas últimas siempre más delgada (15).
13. Disección cuidadosa de la aponeurosis teniendo cuidado de no dañar la arcada vascular periférica, pues sangra efusivamente y resta belleza a la cirugía.
14. Liberar la aponeurosis de sus alerones laterales, tanto en el lado temporal como en el nasal. El cuerno temporal es más denso y puede provocar una retracción del párpado muy antiestética si no se debilita (fig. 32).
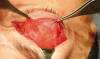
Fig. 32. Aponeurosis disecada y preparada para ser anclada en el tarso.
15. Exponemos la cara anterior del tarso separando de él el orbicular (fig. 33).
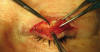
Fig. 33. Sutura a 2-3 mm del borde superior de la cara anterior del tarso.
16. Colocamos en el tarso una sutura central con doble aguja a 2-3 mm de su borde superior y anclamos la aponeurosis (sutura no reabsorbible de 6/0, tipo dacrón). Realizamos con el punto una lazada de prueba y, si la ptosis es bilateral, a la vez en los dos párpados. Incorporamos al paciente para comprobar la altura, contorno y simetría. Personalmente pensamos que éste es un momento que no tiene demasiado valor, pues el aumento de volumen de la infiltración anestésica, la inflamación peroperatoria y el hematoma que acompaña alteran la realidad. Solamente es válido esta medición para detectar la hipercorrección. Si todo nos parece correcto terminamos la cirugía suturando con ese solo punto si la ptosis era leve o añadiendo un punto más y en ocasiones dos cuando el párpado es grande o la aponeurosis está más retraída o debilitada (fig. 34). Personalmente pensamos que éste es un momento que no tiene demasiado valor, pues el aumento de volumen de la infiltración anestésica, la inflamación peroperatoria y el hematoma que acompaña alteran la realidad. Solamente es válido esta medición para detectar la hipercorrección. Es la experiencia la que aporta mucho valor en la decisión (fig. 35). No colocamos suturas ajustables, no tienen mucho sentido porque los primeros días los tejidos continúan inflamados.
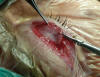
Fig. 34. Anclando aponeurosis al tarso.
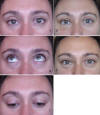
Fig. 35. A: Ptosis derecha leve; B: Excelente función; C: Surco más alto; D: Una
semana después de la cirugía, antes de retirar los puntos; E: Un mes más tarde.
17. La piel la suturamos con 7/0 y nunca colocamos punto de Frost porque el lagoftalmos aquí (al no haber sido resecada la aponeurosis) es mínimo y pasajero.
Técnica de Conjuntivo-Müllerectomía
En los casos leves se puede realizar una Conjuntivo-Müllerectomía o resección en bloque de la conjuntiva y el músculo de Müller (16), es una técnica sencilla y válida para corregir ptosis de 1-2 m y en casos de hiporrección tras una cirugía previa. Está indicada en pacientes con respuesta positiva a la prueba de la fenilefrina La fenilefrina al 10% administrada de forma tópica además del efecto en la midriasis pupilar, activa la contracción del músculo de Müller de forma máxima. Si con la fenilefrina el PS se eleva a una posición normal se realizará una resección en bloque de 8 mm de músculo de Müller y conjuntiva, si con fenilefrina persiste hipocorregido se reseca 9 ó 10 mm y si se hipercorrige solo 6 ó 7 mm.
Se evierte el PS ayudándose de un retractor de Desmarres y se coloca un punto de seda 5/0 a nivel de la línea gris del borde palpebral para mantener la tracción del PS. Se inyecta anestésico subconjuntival, creando un plano de separación entre el músculo de Müller y el EPS. Se mide con un compás la mitad de la longitud de la resección planeada desde el borde superior del tarso y con dos pinzas se cogen los extremos nasal y temporal de lámina posterior a esa altura, se fija la lámina posterior a resecar con un clamp de ptosis Putterman y con punta de Colorado se realiza un incisión a lo largo del tejido clampado. Posteriormente se sutura con un hilo reabsorbible de 6/0.
Personalmente no realizamos esta última técnica, porque sacrifica la arcada vascular periférica, buena parte de la conjuntiva con sus glándulas lacrimales accesorias, y bastante músculo de Müller; además de disminuir la profundidad del fondo de saco conjuntival. Por vía anterior conseguimos muy buenos resultados (fig. 36). En definitiva con la conjuntivo-Müllerectomía se pretende acercar la aponeurosis hacia el tarso, lo mismo que con la reinserción por vía anterior, pero con esta técnica se hace de forma reglada y respetando todas las estructuras.
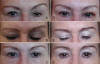
Fig. 36. A: Ptosis izda. B: Surco más elevado; C: Prueba positiva a la
fenilefrina; D: Postoperatorio inmediato; Cirugía por vía anterior; E: Ptosis
corregida; E: Surcos a la misma altura.
COMPLICACIONES
En general las complicaciones son raras.
Cuanto más cuidada sea la técnica quirúrgica y meticulosa la coagulación intraoperatoria, menores serán las complicaciones.
La inflamación excesiva y el hematoma en párpados con aponeurosis previamente debilitadas pueden causar el fracaso de la cirugía. Es útil pautar frío local las primeras 48 horas para disminuir la inflamación postquirúrgica (fig. 37).
En los primeros días tras la cirugía, pueden presentar un leve lagoftalmos sobre todo cuando encontramos la aponeurosis muy retraída hacia la órbita y con poca elasticidad. Es bien tolerado cuando la secreción lagrimal es normal. Generalmente es de corta duración. Se puede tratar de forma conservadora con lubricantes.
Hipercorrecciones: Cuando al reinsertar la aponeurosis colocamos la sutura a varios milímetros de su extremo distal. Se consigue así un resultado de avance con resección, innecesaria en la mayoría de los casos (fig. 38).
Hipocorrecciones pasado el postoperatorio inmediato. Son menos frecuentes que en la cirugía de las ptosis miogénicas, pero pueden aparecer cuando la aponeurosis además de desinsertada se encuentra deshilachada o estirada (fig. 39).
Alteraciones del contorno palpebral cuando el cuerno lateral tracciona demasiado (fig. 40).
Asimetrías en el tamaño de las hendiduras palpebrales. Este resultado es constante cuando la ptosis es bilateral y el paciente insiste en ser operado solamente del lado de mayor ptosis (fig. 41).
La malposición de las pestañas es rara, el entropión puede aparecer si se ancla la aponeurosis en el borde superior del tarso en vez de en la cara anterior y el ectropión si el anclaje es muy bajo, ambas requieren una segunda cirugía.
![]()
Fig. 37. Hematoma posquirúrgico.
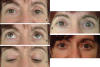
Fig. 38. A: Ptosis izda.; B: Buena función; C: Surco muy alto, bolsas grasas
nasales; D: Realizamos reinserción de la aponeurosis izda., resección de bolsas
grasas y blefaroplastia bilateral, resultando una hipercorrección.
Reintervención: retiramos los dos puntos de anclaje y los nuevos se anudan al
borde de la aponeurosis.
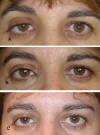
Fig. 39. A: Ptosis moderada desde el nacimiento. Ceja derecha más elevada; B: Ha
pasado una semana de la cirugía: Hipocorrección; C: Ha mejorado el surco y muy
poco la ptosis. Podemos observar cómo la ceja derecha está a la misma altura que
la izda.
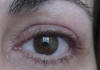
Fig. 40. Leve tracción del cuerno lateral.
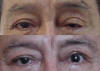
Fig. 41. A: Ptosis bilateral, mayor en lado izdo.; B: Por deseo del paciente se
realiza cirugía solamente en ese lado. Demasiada asimetría.
En nuestra casuística no hemos sufrido este tipo de complicaciones.
BIBLIOGRAFÍA
Mateos E. Ptosis palpebral: tipos, exploración y tratamiento quirúrgico. Ed Ergon, 2005.
Baggio E, Ruban JM, Boizard Y. Etiologc causes of ptosis about a serie of 484 cases. To a new classification? J Fr Ophtalmol. 2002 Dec; 25(10): 1015-20
Fisterer J. Ptosis: Causes, Presentation, and Mangement. Aesth Plast Surg 2003; 27: 193-204.
Konrad VL, Bunce C, nelson C, Collin JR. Aetiology and surgical treatment of childhood blepharoptosis. Br J Ophthalmol 2002; 86: 1282-1286.
Flowers RS. The art of eyelid and orbital aesthetics: multiracial surgical considerations. Clin Plast Surg 1987; 14: 693-721.
Matsuo K. Restoration of involuntary tonic contraction of the levator muscle in patients with aponeurotic blepharoptosis or Horner syndrome by aponeurotic advancement using the orbital septum. Scand J Plast Reconstr Surg Hand Surg. 2003; 37(2): 81-9.
Fujiwara T, Matsuo K, Kondoh S, Yuzurita S. Etiology and pathogenesis of aponeurotic blepharoptosis. ANN Plastic Surgery 2001; 46: 35.
Altieri M, Truscott E, Kingston AE et al. Ptosis secondary to anterior segment surgery and its repair in a two-year follow-up study. Ophthalmologica 2005; 219: 129-135.
Wasserman Bn, Bigler B, Nipper K. Unexpected outcomes associated with laser in situ Keratomileusis; ptosis, anisocoria and curing of exotropia. J cataract Refract Surg 2005; 31: 1238-1241.
Anderson RL, Gordy DD. Aponeurotic defects in congenital ptosis. Ophthalmology 1979 Aug; 86(8): 1493-500.
Martin PA, Rogers PA. Congenital aponeurotic ptosis. Aust N Z J Ophthalmol 1988 Nov; 16(4): 291-4.
www.layyous.com/ultrasound/fetalbehaviour.htm
Erb MH, Kersten RC, Yip CC, Hudak D, Kulwin DR, McCulley TJ. Effect of Unilateral Blepharoptosis Repair on Contralateral Eyelid Position. Ophthal Plast and Reconstr Surg 2004; 20: 418-422.
Hirasawa C, Matsuo. K, Kikuchi N, Osada Y , Shinohara H, Yuzuriha S. Upgaze eyelid position allows differentiation between congenital and aponeurotic blepharoptosis according to the neurophysiology of eyelid retraction. Ann Plast Surg 2006 Nov; 57(5): 529-34.
Hosal BM, Ayer NG, Zilelioglu G, Elhan AH. Utrasound biomicroscopy of the levator aponeurosis in congenital and aponeurotic blepharoptosis. Ophthal Plast Reconstr Surg. 2004 Jul; 20(4): 308-11.
Putterman AM, Fett DR. Müllers muscle in the treatment of upper eyelid ptosis: a ten-year study. Ophthal Surg 1986; 17: 354-60.