REVISIÓN ACTUALIZADA
Farmacología ocular durante la gestación y
la lactancia (II)GIL RUIZ MR1, ORTEGA USOBIAGA J2, GIL RUIZ MT3, CORTÉS VALDÉS C4
1 Doctora
en Medicina y Cirugía. Médico Adjunto del Servicio de Oftalmología. Hospital
Nuestra Señora del Prado. Talavera de la Reina (Toledo).
2 Doctor en Medicina y Cirugía. Especialista en Oftalmología. Clínica
Baviera - Instituto Oftalmológico Europeo. Bilbao (Bizkaia).
3 Doctora en Medicina y Cirugía. Jefa del Servicio de Análisis
Clínicos. Hospital Nuestra Señora del Prado. Talavera de la Reina (Toledo).
4 Doctor en Medicina y Cirugía. Jefe del Departamento de
Oftalmología. Hospital General Universitario «Gregorio Marañón». Madrid.
INTRODUCCIÓN
Un amplio porcentaje de los pacientes que acuden a la consulta de Oftalmología se encuentran dentro del rango de edad fértil. Por esta razón, el médico debe conocer ampliamente no sólo el impacto que el embarazo puede ejercer sobre la fisiología ocular y las enfermedades existentes previamente; además debe estar alerta sobre los niveles de seguridad de cada uno de los fármacos en la gestación y la lactancia. Sólo de esta manera se consiguen reducir al máximo los efectos secundarios que el tratamiento materno puede desarrollar sobre el feto en desarrollo o el neonato.
Como continuación a la primera parte de este artículo, se exponen los niveles de seguridad en la gestación y lactancia de los fármacos más comúnmente utilizados en el ámbito de la Oftalmología. Las letras A, B, C, D y X entre paréntesis indican las categorías de seguridad de los diferentes principios activos según el organismo de la FDA.
1. ANTIINFLAMATORIOS
Constituyen un conjunto heterogéneo de sustancias químicas que se dividen principalmente en tres subgrupos: antiinflamatorios esteroideos (corticoides), antiinflamatorios no esteroideos (AINE) e inmunomoduladores.
Esta riqueza farmacológica nos permite adecuar el tratamiento y personalizarlo a cada paciente –particularmente durante la gestación– ya que tenemos al alcance diversas estructuras químicas comercializadas con distintas propiedades, indicaciones y, por supuesto, diferente eficacia, tolerancia y vía de administración.
1.1. Corticoides
Los corticoides usados en Oftalmología se clasifican en función de su biodisponibilidad, lugar de acción y potencia intrínseca de la molécula en tres grupos: débiles, como la medrisona (no disponible en España como monocomponente); intermedios, como la cortisona, hidrocortisona, fluorometolona y deflazacort; y potentes, como la prednisona, prednisolona, dexametasona, triamcinolona, betametasona y rimexolona (1). Asimismo, la medroxiprogesterona es un progestágeno de baja potencia antiinflamatoria pero con actividad anticolagenasa (tabla 1).

La prednisona ha sido catalogada por la FDA como fármaco categoría B, el resto de los corticoides muestran nivel C, es decir, los estudios realizados en animales han demostrado efectos adversos en el feto, pero no hay estudios adecuados, ni bien controlados, en mujeres embarazadas; o bien no se han realizado estudios en animales, ni existen estudios adecuados y bien controlados en mujeres embarazadas. Estos medicamentos deben ser administrados solamente si el posible beneficio deseado justifica el riesgo potencial en el feto.
La dexametasona es compatible con el período de lactancia; por el contrario la triamcinolona, cortisona, hidrocortisona y deflazacort deben evitarse. En relación al resto de principios activos, el médico valorará si son rigurosamente necesarios.
La medroxiprogesterona está completamente contraindicada durante el embarazo y la lactancia, siendo fármaco categoría X.
1.2. Antiinflamatorios no esteroideos
En relación a los AINE, y según la FDA, debe prescindirse de estos fármacos durante el embarazo. En animales se ha observado que, cuando las cantidades administradas son lo suficientemente grandes como para producir efectos perjudiciales en la madre, disminuyen la velocidad de crecimiento y el peso del feto (3). Los más utilizados en Oftalmología son: diclofenaco (B), flurbiprofeno (D), indometacina (D), ketorolaco (C), pranoprofeno (B) e ibuprofeno (B/D) (tabla 2). Este último principio activo debe evitarse durante el primer y segundo trimestre del embarazo, a no ser que sea estrictamente necesario. Por el contrario, en el tercer trimestre está absolutamente contraindicado, al relacionarse con fetotoxicidad cardiopulmonar y disfunción renal fetal. Asimismo, puede exponer a la madre y al feto a prolongaciones del tiempo de hemorragia, efecto antiagregante e inhibición de las contracciones uterinas (2).
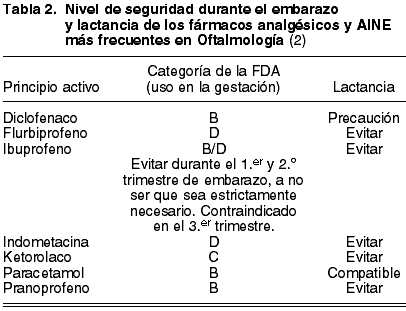
En conclusión, los AINE deberían ser administrados solamente si el posible beneficio deseado justifica el peligro para el feto. Es preferible sustituir, siempre que sea posible, el fármaco AINE por el paracetamol (B), analgésico seguro durante la gestación y compatible con la posibilidad de lactar.
El diclofenaco puede utilizarse con precaución durante el período de lactancia, el resto están prohibidos.
1.3. Inmunomoduladores
En relación a los fármacos inmunomoduladores utilizados comúnmente en Oftalmología, existen 4 grandes grupos: los inhibidores de las células T (ciclosporina A, tacrolimus), antimetabolitos (metotrexate, azatioprina, micofenolato de mofetilo), alquilantes (ciclofosfamida, clorambucilo) y terapias biológicas (tabla 3). Estos últimos, a su vez se subdividen en fármacos anti-factor de necrosis tumoral · (adalimumab, etanercept, infliximab) e inhibidores de la interleucina 2 (daclizumab) (4).

La ciclosporina A (C) es el fármaco inmunomodulador prescrito con mayor frecuencia en Oftalmología. No se ha estudiado si se excreta en leche materna tras su administración tópica, aunque sí se sabe que se elimina por la leche con el resto de formas de administración; a pesar de no detectarse concentraciones en sangre tras su administración tópica, no es aconsejable durante la lactancia (5).
En líneas generales, los fármacos inmunomoduladores no son convenientes durante el embarazo y lactancia, presentando la mayoría de ellos nivel D de seguridad según la FDA. Particularizando, el metotrexate muestra riesgo teratogénico y abortivo, aconsejándose recurrir a métodos anticonceptivos hasta 6 meses después de la última dosis en la mujer y 3 meses en el hombre. La azatioprina puede retrasar el crecimiento intrauterino y producir mutagenicidad o teratogenicidad, proponiéndose también la anticoncepción. El clorambucilo desarrolla infertilidad, incrementa el riesgo de leucemias y es teratógeno. Por último, en todas las terapias biológicas se recomienda evitar el embarazo y lactancia hasta 6 meses tras la finalización del tratamiento (5).
2. ANTIALÉRGICOS Y VASOCONSTRICTORES
Es bastante común para el oftalmólogo atender pacientes con sintomatología alérgica. El disconfort ocular que describen y las dificultades para poder llevar a cabo las actividades cotidianas con normalidad, hacen necesario tratar dichas manifestaciones, independientemente de que sean gestantes.
Ante la clínica alérgica se prescriben fármacos vasoconstrictores y antialérgicos. En el primer grupo destacan la fenilefrina (C), nafazolina (C), oximetazolina (B) y tetrizolina (C) (tabla 4).

Como principios activos antialérgicos existen: los antagonistas de los receptores de la histamina [clorfenamina (B), emedastina (B) y levocabastina (C)], inhibidores de la degranulación de los mastocitos (ácido espaglúmico (C), cromoglicato disódico (B), lodoxamida (B) y nedocromilo (B)) y fármacos multiacción (azelastina (C), epinastina (B), olopatadina (B) y ketotifeno (C)) (6).
Compatibles con la lactancia son la levocabastina, el cromoglicato disódico y el ketotifeno. Están prohibidos el ácido espaglúmico, la olopatadina, la fenilefrina y la tetrizolina. Los agentes químicos restantes se utilizarán tras valorar el oftalmólogo los beneficios (tabla 5).

3. HIPOTENSORES OCULARES
No existen ensayos clínicos referentes a los fármacos antiglaucomatosos en la gestación. En general, es preferible suspender temporalmente el tratamiento médico y vigilar estrechamente a la paciente, siempre y cuando el riesgo de progresión sea bajo (7).
Los prostanoides (latanoprost, travoprost, bimatoprost) están prohibidos; se han observado efectos teratógenos en animales y pueden estimular las contracciones uterinas (8). El tafluprost, recientemente comercializado, no presenta estudios suficientes por ahora para poder catalogar su seguridad en la gestación (tabla 6).

La brimonidina es el único hipotensor ocular con categoría B de seguridad según la FDA. El resto de agonistas a2-adrenérgicos (apraclonidina y clonidina) exhiben nivel C.
Los agonistas colinérgicos, con la pilocarpina como único representante antiglaucomatoso comercializado, presentan seguridad C.
Los b-bloqueantes (maleato de timolol, carteolol, levobunolol y betaxolol) muestran nivel C. A pesar de ello y extrapolando su experiencia por vía sistémica, existen numerosos estudios que dan soporte a su uso, basados en su indicación para el tratamiento de la hipertensión arterial o las arritmias durante el embarazo. Apoyándose en este argumento, la Sociedad Europea de Glaucoma propone a los b-bloqueantes como fármacos de primera elección en pacientes gestantes con riesgo de progresión elevado (7).
Los inhibidores de la anhidrasa carbónica (acetazolamida, brinzolamida y dorzolamida) también han sido clasificados por la FDA como C (tabla 6).
No obstante, los especialistas en Glaucoma recomiendan evitar en los últimos meses de embarazo la brimonidina, por el posible riesgo de depresión respiratoria en el recién nacido, y los b-bloqueantes, para reducir al máximo los potenciales riesgos derivados de los efectos sistémicos de la medicación en el neonato. Aunque no existe una evidencia clínica suficiente respecto a estos 2 hechos, la gravedad de las consecuencias aconseja ser prudente en su uso y recurrir a otras alternativas médicas, siempre que sea posible.
La Academia Americana de Pediatría ha aprobado la administración de b-bloqueantes e inhibidores de la anhidrasa carbónica en madres lactantes, aunque con cautela. Los agonistas a2-adrenérgicos deben evitarse, al estar contraindicados en la población pediátrica (8).
4. LÁGRIMAS ARTIFICIALES
El carácter dinámico de la película lagrimal y su composición compleja con variaciones interindividuales, hace que la reproducción de ésta en laboratorios sea prácticamente imposible, disponiendo realmente de sustitutos lagrimales. El componente mayoritario de las lágrimas artificiales es el agua, completando la formulación un principio activo y diversos elementos que estabilizan el pH y regulan la estabilidad de la lágrima (9). Por este motivo no existen efectos adversos descritos tras la utilización de tratamiento humectante, excepto los derivados de la alergia a alguno de sus componentes o conservantes.
No hay constancia de ninguna complicación referente a la prescripción de sustitutos lagrimales en embarazadas y madres lactantes; aún así, es preferible utilizar aquellas de las que existe más experiencia, ya que no se dispone de ensayos clínicos en este período de la vida.
Los principios activos más comunes en los lubricantes oculares son: carbómero (C), carmelosa (C), hipromelosa (C), parafina (C), lanolina (C), polivinil alcohol (C) y povidona (C). Del ácido hialurónico no existe experiencia suficiente durante la gestación, por lo que debe valorarse la relación riesgo-beneficio (tabla 7).

La carmelosa y el polivinil alcohol han resultado ser compatibles con la lactancia materna; el ácido hialurónico, carbómero, parafina y lanolina requieren prudencia en su uso; la hipromelosa y povidona deberían evitarse (tabla 7).
5. ANTIANGIOGÉNICOS
Los fármacos antiangiogénicos constituyen un conjunto de principios activos de gran actualidad. Son útiles en enfermedades oculares asociadas al factor de crecimiento del endotelio vascular, tales como la neovascularización coroidea y retiniana, el edema macular, procesos inflamatorios intraoculares, y neovascularización corneal e iridiana (10).
Algunos de ellos están aprobados por la FDA para usos diferentes al intraocular, como es el caso del bevacizumab o la triamcinolona intravítrea. Al ser utilizados como medicamento compasivo, no existen estudios aceptados por los organismos internacionales que avalen su seguridad y eficacia, mucho menos en gestantes (11). Mientras que la triamcinolona presenta categoría C, el bevacizumab está contraindicado. Respecto a éste último, no existen datos en embarazadas, y estudios animales han demostrado toxicidad reproductiva incluyendo malformaciones (tabla 8). Se sabe que las Inmunoglobulinas G (IgG) atraviesan la placenta, y es de suponer que inhiba la angiogénesis en el feto; por lo tanto, es esperable que provoque graves defectos natales si se administra en el embarazo (2).

Ranibizumab y pegaptanib sí han sido aprobados por la FDA para el tratamiento de la degeneración macular asociada a la edad de tipo exudativo, aunque tampoco han sido estudiados en embarazadas. El pegaptanib exhibe categoría C; el ranibizumab, aunque sus concentraciones sistémicas son bajas, debido a su mecanismo de acción debe considerarse como potencialmente teratogénico y embrio-fetotóxico (2). No existen datos en mujeres, ni estudios en animales. No deberá usarse en el embarazo salvo que el beneficio supere el riesgo para el feto (tabla 8).
El acetato de fluocinolona (C) como dispositivo intravítreo fue aceptado por la FDA en 2005 para el tratamiento del edema macular asociado a uveítis crónicas. Se elimina en la leche materna, por lo que, al igual que el resto de antiangiogénicos, están prohibidos en este período.
6. SUSTITUTIVOS VÍTREOS
En cirugía vítreo-retiniana es frecuente recurrir a sustitutivos vítreos para mantener la anatomía ocular. En la actualidad se dispone de líquidos perfluorocarbonados (perfluoro-n-octano, perfluorometildecalina, perfluorotributilamina, perfluorofenantreno), gases intraoculares no expansibles (aire, xenón), gases expansibles (hexafluoruro de azufre, perfluorometano, perfluoroetano, perfluoropropano) y silicona intraocular (polidimetilsilicona, fluorosilicona y siliconas pesadas) (12). No hay constancia de datos clínicos en embarazadas, ni en mujeres en período de lactancia, por lo que deberían evitarse en ambos casos, o al menos utilizarlos con precaución (tabla 9).

7. BIOADHESIVOS
Los bioadhesivos disponibles en la actualidad son los cianocrilatos, polímeros acrílicos y adhesivos biológicos. Estos últimos están compuestos por fibrinógeno, trombina y calcio (13). Al igual que en el grupo farmacológico anterior, no se dispone de experiencia durante el embarazo o lactancia (tabla 10).

8. TOXINA BOTULÍNICA
El principio activo es una exotoxina sintetizada por el Clostridium botulinum, una bacteria anaerobia esporulada grampositiva. Esta toxina es capaz de desarrollar una parálisis muscular flácida reversible (14).
Existen 2 serotipos; el A exhibe un nivel de seguridad C, mientras que con el serotipo B se desconocen riesgos potenciales para el ser humano, no siendo recomendable usarla en pacientes embarazadas, salvo estricta necesidad (2). Ambas son macromoléculas que en condiciones normales no lograrían atravesar la barrera hematoencefálica ni la placenta, pero al carecer de experiencia en gestantes y mujeres en período de lactancia, no se aconseja su uso (tabla 11).

9. VISCOELÁSTICOS
Necesarios en numerosos procedimientos quirúrgicos oftalmológicos, contienen una o más de las siguientes sustancias, en diferentes concentraciones: hialuronato sódico, condroitín sulfato e hidroxipropilmetilcelulosa (14). No se dispone en la actualidad de investigaciones acerca del uso de viscoelásticos en embarazadas o mujeres en lactancia, por lo que no se recomienda su utilización (tabla 12).

10. SUPLEMENTOS VITAMÍNICOS
En la actualidad existen comercializados diversos complejos vitamínicos que, como complemento a nuestra alimentación, constituyen un aporte equilibrado de nutrientes y antioxidantes. Estos suplementos incrementan los mecanismos defensivos del organismo frente a procesos oxidativos que constituyen un daño potencial para la función visual, como puede ser la radiación ultravioleta.
Los complejos vitamínicos contienen: carotenoides (luteína, zeaxantina, astaxantina); vitamina A (retinol), C (ácido ascórbico), E (d-a-tocoferol) y el grupo B (B1 o tiamina, B2 o riboflavina, B3 o niacina, B6 o piridoxina, B9 o ácido fólico y B12 o cianocobalamina); minerales (zinc, manganeso, selenio, cobre) y ácidos grasos esenciales omega-3 (tales como el DHA o docosahexaenoico y el EPA o eicosapentaenoico).
Las funciones de los suplementos vitamínicos son múltiples, tantas como componentes existen en su formulación. De este modo, los carotenoides son pigmentos localizados en la mácula con propiedades antioxidantes y protectores de los fotorreceptores; las vitaminas A, C y E regularizan numerosas reacciones metabólicas, retrasando el proceso de envejecimiento desencadenado por los radicales libres; el grupo B es necesario para el correcto funcionamiento del sistema nervioso y los ojos, al proveer al organismo de la energía necesaria para que se efectúen correctamente diversas reacciones metabólicas; los minerales forman parte del sistema antioxidante celular y, por último, los ácidos grasos son elementos imprescindibles en la retina (2).
Excepto el tocoferol que muestra un nivel de seguridad C fijo, el resto de vitaminas presentan grados diferentes de seguridad en función de la dosis administrada. Concretamente la vitamina A, puede llegar a mostrar categoría X al superar la dosis recomendada (tabla 13). Por ello, y dado que no existen estudios suficientes en pacientes embarazadas, se aconseja obtener estos principios activos en la gestación y la lactancia a través de una alimentación sana y equilibrada y, sólo en casos extremos, recurrir a los suplementos vitamínicos (2).

BIBLIOGRAFÍA
-
Gil MR, Cortés C. Farmacología de la Inflamación y Analgesia en Oftalmología. En: Cortés C, Arias A, Encinas JL, García J. LXXXIII Ponencia Oficial de la Sociedad Española de Oftalmología. Farmacología Ocular. Madrid: Industria Gráfica MAE SL; 2007: 163-177.
-
Vademecum Internacional. 50ª edición; Madrid: CMP Medicom; 2009.
-
Ministerio de Sanidad y Consumo. Información de medicamentos. Consejos al paciente. 11ª edición; Madrid: Einsa; 1994.
-
Díaz D, Benítez del Castillo JM, Arriola P. Corticoides sistémicos e inmunoterapia en oftalmología. En: García-Sánchez J, García-Feijoó J. Oftalmomecum 2009. Barcelona: Publicaciones Permanyer; 2009: 111-127.
-
Arriola P, Díaz D, Benítez del Castillo JM. Antiinflamatorios. Corticosteroides, antiinflamatorios no esteroideos, otros agentes moduladores de la inflamación. En: García-Sánchez J, García-Feijoó J. Oftalmomecum 2009. Barcelona: Publicaciones Permanyer; 2009: 51-63.
-
Gil MR, Cortés C. Antialérgicos y vasoconstrictores. En: García-Sánchez J, García-Feijoó J. Oftalmomecum 2009. Barcelona: Publicaciones Permanyer; 2009: 65-70.
-
European Glaucoma Society. Terminología y pautas para el glaucoma. 2.ª edición; Savona: Dogma; 2003.
-
Urcelay JL. Tratamiento médico antiglaucomatoso en mujeres gestantes y lactantes. En: Cortés C, Arias A, Encinas JL, García J. LXXXIII Ponencia Oficial de la Sociedad Española de Oftalmología. Farmacología Ocular. Madrid: Industria Gráfica MAE SL; 2007: 297-299.
-
Benítez del Castillo JM, Díaz D, Arriola P. Lágrimas artificiales. En: García-Sánchez J, García-Feijoó J. Oftalmomecum 2009. Barcelona: Publicaciones Permanyer; 2009: 81-87.
-
Bañuelos J, García MC, Gili P, Arias A. Antiangiogénicos. En: Cortés C, Arias A, Encinas JL, García J. LXXXIII Ponencia Oficial de la Sociedad Española de Oftalmología. Farmacología Ocular. Madrid: Industria Gráfica MAE SL; 2007: 301-324.
-
Bañuelos J, Gili P, Arias A. Antiangiogénicos. En: García-Sánchez J, García-Feijoó J. Oftalmomecum 2009. Barcelona: Publicaciones Permanyer; 2009: 89-96.
-
Encinas JL, Bañuelos J. Sustitutivos vítreos. En: Cortés C, Arias A, Encinas JL, García J. LXXXIII Ponencia Oficial de la Sociedad Española de Oftalmología. Farmacología Ocular. Madrid: Industria Gráfica MAE SL; 2007: 405-443.
-
Cortés C, Gil MR, Cortés I. Adhesivos en Oftalmología. En: Cortés C, Arias A, Encinas JL, García J. LXXXIII Ponencia Oficial de la Sociedad Española de Oftalmología. Farmacología Ocular. Madrid: Industria Gráfica MAE SL; 2007: 445-449.
-
Encinas JL, Gómez de Liaño R, Muñoz AM. Sustitutivos vítreos. Bioadhesivos. Toxina botulínica. Viscoelásticos. En: García-Sánchez J, García-Feijoó J. Oftalmomecum 2009. Barcelona: Publicaciones Permanyer; 2009: 97-110.