|
1. Introducción
Si bien el diagnóstico del retinoblastoma (RTB) utilizando estas técnicas
ya ha sido tratado de forma más resumida dentro de otro capítulo de este
libro, creemos que debemos profundizar más en el uso tanto de la tomografía
computada (TC) como de la resonancia magnética (RM) en el diagnóstico y el
control del tratamiento de esta entidad, ya que, si bien la terapéutica
quirúrgica sigue siendo fundamental, se están utilizando otras formas de
actuación sobre este tumor que requieren de rigurosos y frecuentes controles de
imagen con estas técnicas para poder decidir si dichas conductas terapéuticas
son eficaces o bien se debe recurrir a la cirugía.
Por ello, en este capítulo trataremos en mayor detalle las aplicaciones
diagnósticas de estos métodos de imagen, en especial en su utilidad en los
tratamientos previos a la enucleación que, lógicamente, debe ser la última
opción cuando fallen las demás.
2. Papel de TC y RM en el diagnóstico deL RETINOBLASTOMA
El primer paso a la hora de decidir el tratamiento más correcto para un RTB
es un diagnóstico lo más exacto y completo posible.
Aunque este diagnóstico inicial es fundamentalmente oftalmoscópico (1), no
por ello disminuye el papel de las técnicas de imagen, aunque su función
primordial no sea la detección primaria de la patología.
Los objetivos del diagnóstico por imagen en el RB (2) son los siguientes:
• confirmación del diagnóstico clínico
• realización de diagnóstico diferencial con otras entidades que causan
leucocoria y pueden simular esta patología (hiperplasia persistente de vítreo
primario, enfermedad de Coats, toxocariasis, hemorragia subretiniana organizada,
hamartoma de retina...)
• determinación del tamaño tumoral
• detección de la presencia de calcio
• valoración de la diseminación del tumor a coroides, esclera, nervio
óptico, grasa orbitaria
• valoración de la diseminación metastásica en el sistema nervioso
central (SNC)
• detección de RB trilateral
• control de respuesta al tratamiento.
Las técnicas de diagnóstico por imagen que muestran mayor utilidad en el
diagnóstico del RTB son la ultrasonografía (US), tomografía computarizada
(TC) y resonancia magnética (RM).
Tradicionalmente la US ha sido la más utilizada por su alta resolución para
ver lesiones de pequeño tamaño (2 mm según algunos autores) (3) y para
valorar calcificaciones (detectadas en un 90-95%, un 5-10% de los RB no muestran
calcio) (1,2), como por su inocuidad al no utilizar radiación ionizante y poder
ser empleada sin necesidad de anestesia.
Sin embargo, su uso se ha complementado (4) con otras técnicas conforme
éstas han resultado más accesibles y han progresado, aportando innovaciones
como la TC helicoidal que permite realizar exploraciones más rápidas, evitando
la anestesia en muchos casos, o las secuencias turbo de la RM que han disminuido
significativamente los tiempos de exploración.
No obstante aún no hay un criterio unánime con respecto a la indicación de
cada una de estas pruebas. Algunos autores propugnan la ecografía como método de elección (3)
para detectar calcificaciones incluso de un tamaño menor a 2 mm (1,2,5).
La RM muestra una significativa menor sensibilidad en la detección del
calcio que la TC o la US pero supera a estas dos técnicas en la valoración de
la extensión a coroides, n. óptico... la diseminación en el SNC y en el
diagnóstico diferencial con entidades que simulan al RTB (1-3,5,6).
En este contexto, la mayoría de los protocolos abogan por la US y el TC
orbitario como prueba de elección para confirmación del diagnóstico de RTB
(dada su sensibilidad para detectar calcio) y por la RM para valoración de su
extensión local y en el SNC, diagnóstico diferencial, así como para una
medición de tamaño previa a posibles tratamientos y controles sucesivos de
regresión de las tumoraciones. Lo ideal es usar las tres técnicas en principio
y controles sucesivos con US y RM.
3. Diagnóstico de RB mediante TC
El protocolo típico de TC orbitaria (figuras 1 y 2) consiste en cortes
contiguos de 3 cada 3 mm paralelos a la línea infraorbitomeatal (7). Algunos
autores recomiendan realizar estudios de alta resolución con cortes finos de
1,5 mm para detectar el tumor con mayor seguridad (1).
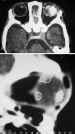
Figuras 1a y b. Retinoblastoma: 2 casos estudiados en TC. Buena
delimitación del componente cálcico con TC axial en 2 casos de RTB .
El estudio con contraste intravenoso aumenta el contraste en las estructuras
vasculares, delimitándolas mejor de la masa, y permite identificar la
extensión extraorbitaria.
Desde el año 1989, el desarrollo de la TC helicoidal o espiral, permite
estudiar un volumen orbitario más rápido con mayor resolución espacial, lo
que hace innecesaria en muchos casos la anestesia para realizar el estudio (7).
Además es posible realizar reconstrucciones en cualquier plano dentro del
volumen estudiado y reconstrucciones tridimensionales (5).
Más del 90% de los RTB muestran calcificación en TC, generalmente en la
región posterior del globo (5). Su aspecto es variable, única o múltiple,
finas o gruesas. Si el tumor es pequeño la calcificación es difícil de
identificar (7). Es rara la calcificación del componente extraocular del RTB;
la forma infiltrante difusa es rara y puede no tener calcio (1).
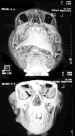
Figura 2. Reconstrucción tridimensional craneofacial para una mejor
valoración de asimetrías.
El RTB realza mínimamente en el estudio con contraste, no obstante puede
ayudar a identificar enfermedad retrobulbar e intracraneal aunque para ello es
más sensible la RM.
La TC también juega un papel decisivo en el estudio de extensión
pretratamiento para detectar metástasis hematógenas (óseas o linfáticas).
4. Diagnóstico de RTB mediante RM
La órbita ha sido una de las regiones (figuras 3 y 4) que más se ha
beneficiado de los avances técnicos experimentado por la RM. En un principio,
la resolución en este área era menor a la de otras técnicas (US y TC) debido
a su situación periférica y a la movilidad de su estructura más grande, el
globo ocular. Por ello se ha trabajado en encontrar soluciones técnicas para
paliar estas dificultades, y éstas han contribuido a aumentar de un modo
importante la sensibilidad de la RM en la órbita.
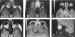
Figuras 3a, b, c, d, e y f. Retinoblastoma bilateral.
Secuencias potenciadas en T1 pre y post la administración de gadolínio, y
potenciadas en T2 (a, b, c). RM de control 11 meses después de finalizar el
tratamiento (d, e, f).
Marcada disminución de tamaño de las masas (d, e) respecto al primer
estudio (a, b), aunque con persistencia de captación de contraste.

Figuras 4a, b, c y d. Retinoblastoma en ojo derecho.
Secuencias potenciadas en T1 tras la administración de gadolínio (a) y
potenciada en T2 (b). RM de control 17 meses tras finalizar el tratamiento (c,
d).
Ausencia de captación tumoral de gadolínio (c) así como reducción del
componente cálcico (d) respecto a estudio basal potenciado en T2 (b).
Entre estos avances destaca la aparición de las secuencias rápidas (fast o
turbo). Son secuencias de similares características a las convencionales con
una importante reducción de tiempo en la adquisición de datos. Esto ha
disminuido el número de artefactos de movimiento y ha permitido mejorar la
imagen, al poder utilizar matrices de alta resolución manteniendo el tiempo de
exploración en unos límites aceptables.
Otro gran avance ha sido la aparición de antenas de superficie, que son
bobinas de exploración de pequeño diámetro que se colocan sobre la superficie
a estudiar, consiguiendo aproximar al máximo la zona de interés a la antena
receptora y eliminando el ruido que producen áreas cercanas a la órbita pero
fuera del campo de interés. De esta forma, se logra aumentar la relación
señal-ruido que es la que marca la calidad de la imagen y permite tanto
aumentar la matriz utilizada como disminuir el grosor del corte, parámetros que
permiten una mayor resolución del estudio.
Sin embargo, en el caso del RTB, existen algunas dificultades en el uso de
esta antena:
• La antena de superficie no permite explorar el vértice orbitario ni el
compartimento intracraneal, áreas de especial interés en la valoración de la
diseminación tumoral.
• Las secuencias largas (como las secuencias con potenciación T2),
especialmente útiles en el diagnóstico de RTB, son más susceptibles a
artefactos cuando se emplea esta antena en lugar de la de cráneo.
Por ello en el diagnóstico del RTB el uso de la antena de superficie está
más limitado que en el resto de la patología orbitaria, siendo necesario
combinar su uso con el de la antena de cráneo. Algunos autores recomiendan
utilizar directamente esta última (1).
Las secuencias empleadas en el diagnóstico del RTB en RM y sus
características son las siguientes:
• Secuencia spin eco potenciada en T1 (SET1) con tiempo de
repetición (TR) y tiempo de eco (TE) cortos. Es la secuencia que aporta
información anatómica. Los RTB muestran en esta secuencia un comportamiento
similar a otros tumores neuroectodérmicos, iso o levemente hiperintensos
respecto al vítreo. Este aumento de la intensidad de la señal parece
relacionarse con necrosis y hemorragia intratumoral, y a depósitos de
sustancias paramagnéticas asociadas a calcificaciones tumorales (1).
• Secuencia spin eco potenciada en T2 (SET2) con TR y TE largo. En
esta secuencia la señal del tumor es hipointensa respecto al vítreo, en
relación a los mismos factores responsables de la intensidad de señal en SET1,
así como a la alta celularidad de estos tumores con escasa proporción de agua.
Es este contenido hídrico, muy alto en otros tumores, el responsable del
típico brillo de las lesiones tumorales en esta secuencia. El comportamiento
contrario del RB es de gran ayuda para realizar el diagnóstico diferencial con
otras lesiones y poder cuantificar exactamente su tamaño diferenciándolo tanto
del líquido intraglobo como de otras lesiones que puedan asociarse
(desprendimiento de retina...).
• Secuencia SET1 con saturación de la grasa (fat sat) tras la
administración de gadolinio (Gl) intravenoso.
El grado de extensión tumoral se valora sobre todo tras la administración
de gadolinio intravenoso; los tejidos tumorales aumentan su señal de forma
clara. La valoración de este aumento de la señal se hace empleando secuencias
T1, con supresión de la señal de la grasa intraorbitaria, también
hiperintensa, que podría ser confundida con la señal del tumor. A esto se le
llama «saturar la grasa» y es imprescindible para las secuencias con
gadolinio.
• Secuencia eco de gradiente potenciada en T2. Su utilidad en esta
patología está actualmente en evaluación. Teóricamente son secuencias
especialmente susceptibles a la presencia de calcio y elementos paramagnéticos.
Su función sería aumentar la capacidad de la RM en la detección de calcio.
• Secuencias 3D. Esta modalidad de exploración permite la
adquisición de datos de un volumen determinado, sobre el que posteriormente se
puede actuar para conseguir la proyección deseada así como grosores de corte
muy pequeños (menos de 1 mm). Son muy útiles para valorar una estructura
concreta en toda su longitud como el nervio óptico, aunque su diferenciación
anatómica es peor que en las secuencias spin eco, y la proporción de
artefactos mayor.
5. Diagnóstico diferencial de RB con entidades simulantes
Tanto la TC como la RM son fundamentales para establecer el diagnóstico
diferencial con lesiones simulantes de RTB que también causan leucocoria.
TC
Dado que las calcificaciones de cualquiera de estas lesiones simulantes suele
ser inexistente antes de los tres años, a excepción del microftalmos y los
quistes colobomatosos (8), la presencia de calcio en una lesión es
prácticamente patognomónica de RTB.
RM
A partir de los tres años algunas de estas lesiones simulantes si pueden
mostrar componente cálcico como la retinopatía del prematuro, las drusas o la
toxocariasis. En estos casos, así como en los RTB no calcificados [5% de los
casos y en mayor proporción en el tipo difuso infiltrante (2)] es necesario
realizar el diagnóstico diferencial mediante RM (1-3). La captación de
gadolinio por parte del tumor así como la típica baja señal T2 con señal
levemente aumentada T1 son características que solo encontramos en RTB.
Además mediante RM se puede diferenciar claramente el componente sólido del
líquido. Esto resulta especialmente útil en el diagnóstico diferencial con la
enfermedad de Coats, y en el RTB asociado a desprendimiento de retina. La señal
de este fluido subretiniano, es marcadamente hiperintenso en la enfermedad de
Coats y es isointenso en el caso de RTB (3).
6. Diagnóstico de RB trilateral
Otra de las funciones principales del diagnóstico por imagen en el RTB es la
detección de tumores asociados de línea media, de la región pineal en el 75%
de los casos y supra o paraselares en el 25% (8).
Debido a su origen en restos neuroectodérmicos en el suelo del tercer
ventrículo (9) sus características de imagen son similares a las del RTB.
Dada la ausencia prácticamente completa de calcificaciones pineales antes de
los seis años (15 de 11) el hallazgo de las mismas resulta altamente sugestivo
de patología pineal. Por ello, un protocolo adecuado para el seguimiento de los
casos de RTB bilateral o unilateral e historia familiar sería la realización
de TC cada seis meses hasta los cuatro años, y en el caso de encontrar
calcificaciones, realizar RM con gadolinio para valorar el componente blando del
posible tumor pineal (9).
7. Papel de TC y RM en el control de la respuesta al tratamiento del RB
Una función primordial de las técnicas de imagen es la evaluación de la
respuesta a los distintos tratamientos del RB.
Enucleación e implantación de prótesis porosas de hidroxiapatita, Medpor o
Alúmina
Este tema ya ha sido tratado exhaustivamente en otros capítulos de este
libro por lo que únicamente remarcaremos que en estos casos, si bien la TC
puede ser útil y suficiente para valorar posibles complicaciones quirúrgicas,
la RMes la técnica más adecuada para la evaluación de la revascularización
que debe producirse en estas prótesis previamente a la colocación del
vástago. Su resolución en este campo es muy alta, con una eficacia global del
90%, según nuestras evaluaciones (11,12).
Evaluación de respuesta al tratamiento con quimioterapia
La utilización de un método de diagnóstico u otro en este campo viene dada
en muchos casos por la disponibilidad técnica y por el número de controles a
realizar. Algunos autores propugnan la US como método suficiente de seguimiento
(10), mientras que otros abogan por TC o RM para este propósito (9).
En nuestra experiencia, tras revisar los estudios de RM y TC de 31 niños con
RTB tratados con quimioterapia, la RM es el método más adecuado para la
valoración de la respuesta al tratamiento, ya que detecta con mayor
sensibilidad que la TC la presencia de tejido tumoral activo, diferenciandolo
del componente cálcico; también detecta mejor la existencia de hemorragia y el
desprendimiento de retina asociados. Ninguno de los dos métodos diagnósticos
(TC y RM) es eficaz para la valoración de invasión coroidea ni siembra
vítrea.
La RM también es más útil que la TC en la valoración cuantitativa de la
reducción del tamaño tumoral. No obstante el análisis cuantitativo debe ser
muy riguroso realizando las medidas en planos muy similares en todos los
estudios y de la misma forma.
Por ello, los controles de imagen deben ajustarse a un estricta seriación
para obtener planos y secuencias similares en todos los controles.
El protocolo más idóneo consistiría en la realización de:
— US.
— TC sin contraste para la detección de calcificaciones, preferible TC
helicoidal dada la posibilidad de realizar cortes muy finos y reconstrucciones.
— RM sin y con Gadolinio: Secuencias T1 axial sin G con saturación grasa,
T2 axial y coronal o sagital según se vea mejor, T1 con G, con saturación
grasa axial y coronal o sagitales según se vea mejor.
Los controles deben realizarse por lo menos cada seis meses (9), por lo que
la TC implicaría una elevada dosis de radiación sobre el cristalino. Por otra
parte, la RM tiene importantes ventajas en la estimación exacta del tamaño
tumoral así como de su componente retrobulbar sobre la US por lo que en nuestra
experiencia este método es el ideal para realizar estos controles semestrales
complementado con ecografías bimensuales.
BIBLIOGRAFÍA
- Som Peter M, Curtin Hugh D. Head and Neck Imaging. Third Edition. MOSBY.
1996; 1.009-1.183.
- Kaufman LM, Mafee MF, Song CD. Retinoblastoma and simulating lesions. Role
of CT, MR imaging and use of Gd-DTPA Contrast Enhancement. Radiologic clinics of
North America. Nov. 1998; 36, 6: 1.101-1.116.
- Beets-Tan RGH, Hendriks MJ, Ramos LMP, Tan KEWP. Retinoblastoma: CT and
MRI. Neuroradiology 1994; 36: 59-62.
- Harbour JW, Murray TG. Management of intraocular tumors. Part III. Retina
and Vitreous Surgery. In:Albert DM. Ophthalmic surgery: Principles and
techniques 1999; 51: 695-705.
- Pelak VS, Volpe NJ, Liu GT, Galetta SL. Neuroradiology in ophthalmology.
Ophthalmology clinics of North America. 1998; 11 (3): 339-347.
- Scott W. ATLAS. Magnetic Resonance Imaging of the Brain and Spine Second
edition. Lippincot-Raven, 1996; 1.007-1.092.
- Hansberger HR. Handbook of head and neck imaging. Second edition. Mosby,
1995; 301-338.
- Bagley LJ, Hurst RW, Zimmerman RA, Shields JA, Shields CL, De Potter P:
Imaging in the trilateral retinoblastoma syndrome. Neuroradiology 1996; 38:
166-170.
- Kiratli H, Bilgiç S, Özerdem U. Management of Massive Orbital Involvement
of Intraocular Retinoblastoma. Ophthalmology 1998; 105,2: 322-326.
- Shields CL, De Potter P, Himelstein BP, Shields JA, Meadows AT, Maris JM.
Chemoreduction in the Initial Management of Intraocular Retinoblastoma. Arch
Ophthalmology 1996; 114: 1.330-1.346.
- Doz F, Khelfaoui F, Mosen V. The role of chemotherapy in orbital
involvement of retinoblastoma. The experience at a single institution of the 33
patients. Cancer 1994; 74: 722-732.
|