|
La órbita es una maravilla arquitectónica, interrelacionada en su contenido
con gran cantidad de septos, vasos, nervios y músculos que sostienen al globo
ocular y lo protegen de agresiones externas. Tan solo tiene su talón de Aquiles
en su parte anterior y lateralmente para así conseguir un mejor campo de visión
lateral.
El abordaje quirúrgico de la órbita debe respetar la complejidad de su
anatomía si no queremos producir ceguera. De todo el mundo es conocido que en
la cirugía orbitaria, las indentaciones, tracciones, hemorragias y lesiones
ocupantes de espacio pueden producir una neuropatía óptica isquémica. Las
contusiones frontales, aparentemente inocuas son irrecuperables si no actuamos
con celeridad mediante punciones, megadosis de corticoides e incluso utilizando
la vía neuroquirúrgica. Situaciones tan banales como no desinsertar los
músculos, traccionarlos en nuestros abordajes transconjuntivales y transeptales
o con la ayuda de los maxilofaciales y neurocirujanos utilizando más
sofisticados accesos, resultan desproporcionados al producirse la pérdida de
visión permanente, pero tienen una justificación clara.
La cirugía con la ayuda del microscopio, tiene que ser asistida por
ayudantes que descompriman los separadores periódicamente. La grasa orbitaria
que nos resulta tan molesta impidiéndonos lazar, disecar o extraer con criodos
las tumoraciones sólidas o friables, produce en nuestros vecinos de unidades
craneofaciales (neurocirujanos, maxilofaciales u otorrinolaringólogos)
verdadera aversión. Los trayectos de los 7 músculos, sus fijaciones, poleas y
ligamentos exigen un equipo multidisciplinario en el que oftalmólogos
especializados en órbita se integren en la cirugía craneofacial y revisen periódicamente en estrecha colaboración con neuroradiólogos, oncólogos y
radioterapeutas la diversidad de esta patología infantil.
Mención aparte merece el Servicio de Anestesia Infantil, que desarrolla su
experiencia en una cirugía a veces muy corta en las biopsias o extirpaciones de
quistes dermoides y en otras con tiempos quirúrgicos de 12 ó 14 horas en el
curso de reconstrucciones tumorales y malformaciones.
Queremos comunicar en este capítulo la experiencia personal y las
complicaciones que hemos tenido en los últimos 11 años en el Hospital Infantil
La Paz, lo que hemos aprendido de nuestros jefes, amigos y maestros y aunque
«todo está en los libros», siempre hay pequeños conceptos que tamizar.
Conviene resaltar más intensamente las novedades y aportaciones que puedan ser
útiles a los lectores.
Anatomía quirúrgica
(1-18)
Paredes orbitarias
Las dos cavidades piriformes con su mayor apertura anterior, tienen en el
canal óptico su vértice. El paralelismo de las paredes mediales, contrasta con
los aproximadamente 45° de inclinación de las externas, que entre sí son
entre 90 y 100°.

Figura 1. Representación para imagen tridimensional del globo
ocular y la órbita en visión frontal y angulada.
El hueso tiene mucho grosor en los rebordes orbitarios y en el ápex. Por
otra parte es delgado en la lámina papirácea y en zonas del suelo.
La mitad posterior de la pared orbitaria lateral es adyacente a la fosa
craneal media y en su grosor limita la cantidad de hueso que puede ser resecado
en las orbitotomías laterales, dificultando el acceso al ápex orbitario. El
techo de la órbita es vecino a la fosa craneal anterior. Las paredes orbitarias
tienen siete huesos diferentes en su estuctura que nos obligan a relacionarlos y
estudiar su complejidad.
Periostio
Se separa facilmente de las paredes orbitarias, pero en los rebordes
anteriores, fisuras, suturas y en el foramen óptico esta firmemente fijado al
hueso.

Figura 2. Representación para imagen tridimensional de la
vascularización arterial orbitaria desde una visión lateral.
Cono muscular
Todos los músculos extraoculares excepto el oblicuo inferior, las membranas
y septos crean un embudo que termina en el agujero óptico. La mayoría de los
vasos y nervios entran en el cono lateralmente al nervio óptico.

Figura 3. Representación para imagen tridimensional de la vía
lagrimal.
Canal óptico
Su eje está a 36° de la línea media. Tiene 7-10 mm de longitud y en su lado
medial es adyacente al seno esfenoidal y a las celdas etmoidales posteriores.

Figura 4. Cortes anatómicos de las estructuras óseas y contenidos
de la cavidad orbitaria cedidos por los Dres. Costa Vila y Canals Imhor de la
LXX ponencia oficial de la Sociedad Española de Oftalmología «Cirugía
Básica de Anejos Oculares» (Pablo Zaragoza García), Tecnimedia Editorial.
1996.
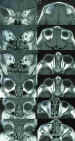
Figura 5. Cortes anatómicos de resonancia nuclear magnética donde
se aprecia el contenido orbitario.
Abordaje anterior
Es fundamental conservar y disecar las múltiples estructuras que nos
encontramos. Párpados, séptum orbitario, tróclea, vasos y nervios supra e
infraorbitarios y los trocleares, la glándula, el saco lagrimal y los
ligamentos palpebrales. El oblicuo inferior pasa cerca del saco y la glándula
lagrimal es dividida en dos por el cuerno lateral del elevador. Los ligamentos
de Whitnall, los fondos de saco conjuntivales y la tenon son de vital
importancia en la armónica conservación de la arquitectura anatómica.
La grasa orbitaria
Está dividida por los septos intermusculares en dos cavidades (intra y
extraconal) protegiendo, interrelacionando y soportando con esos tractos
fibrosos al globo ocular, nervio óptico y a la musculatura extrínseca. El
cirujano de órbita puede originar imbalances musculares, diplopías y
retracciones por alteración del tejido conectivo en sus aproximaciones al
contenido orbitario.
Finalmente las hendiduras esfenoidales e infraorbitarias, el anillo de Zinn,
los vasos y nervios intraorbitarios, las estructuras periorbitarias (senos
paranasales) y las tres fosas limítrofes que nos comunican con otras
especialidades, engloban el complejo abordaje quirúrgico de la patología en la
infancia que se complementa con su semiología, la exploración física y los
estudios neurorradiológicos complementarios.
ORBITOTOMÍAS EN LA INFANCIA
(4,11,18-21)
Hay cinco aproximaciones a la órbita de las cuales la vía anterior y la
lateral consideramos deben ser realizadas por el oftalmólogo. La transfrontal,
antral y etmoidal pertenecen a otras especialidades.

Figura 6. Diversos tipos de resecciones óseas que se usan en las
orbitotomías laterales.

Figura 7. Abordajes de entrada a la órbita. 1: Orbitotomía lateral
de Stallard-Wright. 2: Nueva orbitotomía lateral palpebral. 3: Orbitotomía con
cantotomía lateral. 4: Orbitotomía transcaruncular medial. 5: Orbitotomía de
Lynch. 6: Orbitotomía de párpado superior. 7:Orbitotomía superomedial
palpebral vertical. 8: Orbitotomía transconjuntival medial. 9: Orbitotomía
lateral con cantotomía anterior. 10:Orbitotomía subciliar inferior. 11:
Orbitotomía transconjuntival inferior. 12: Orbitotomía transconjuntival
lateral.
Como espacios quirúrgicos resaltamos igualmente otros cuatro:
• Subperióstico entre el hueso y la periórbita.
• Extraconal entre la periórbita y el cono muscular con sus fascias.
• Intraconal.
• Epiescleral entre la tenon y el globo ocular.
Orbitotomías anteriores
La resección del hueso es innecesaria por este método que penetra en la
órbita por tres vías:
Transconjuntival.
La usamos para lesiones superficiales próximas al
globo ocular y para las localizadas en la parte anterior del cono muscular.
Transeptal.
A través del séptum orbitario. Vale para tumores
circunscritos y permite la biopsia de masas infiltrantes, previa localización.
Subperióstica.
Limitada en el acceso de lesiones posteriores, permite
biopsias y drenaje de colecciones purulentas de la periórbita afectada por
contigüidad.
Orbitotomía lateral
La parte anterior de la pared lateral de la órbita se reseca y tiene en la
infancia muy pocas indicaciones por la facilidad de realizar orbitotomías
anteriores. Permite un acceso cómodo al espacio retrobulbar pero está limitada
en el ápex orbitario por la proximidad al espacio óseo de la fosa craneal
media.
Figura 8. Orbitotomía
transcraneal realizada por la unidad craneofacial del Hospital Infantil «La
Paz».
Orbitotomía transfrontal
La retracción del lóbulo frontal del cerebro, extirpación del techo de la
órbita, e incluso la apertura de la duramadre cerebral son procedimientos
neuroquirúrgicos que implican más riesgo que otras aproximaciones a la
órbita. Es, sin embargo, necesaria cuando la lesión invade las cavidades
craneal y orbitaria o hay que impedir a un glioma llegar al quiasma.
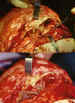
Figura 9. Orbitotomía transfrontal con liberación del techo de la
órbita y colocación de placas de titanio para reconstruir la cavidad.
Orbitotomía transantral y transetmoidal
Se usa en colaboración con los otorrinolaringólogos con visualización
endoscópica para biopsias, exploración y cirugía en las fracturas del suelo
de la órbita y drenajes de abcesos orbitarios. Tiene peor resolución en la
extirpación de lesiones sólidas intraconales. Utilizan la vía transnasal. Su
futuro en la descompresión del canal óptico, cada vez tiene mayor aceptación
en la literatura mundial.
Las aproximaciones mediales transcutáneas tipo Linch están anticuadas y son
preferibles las carunculares para llegar a mucoceles, tumores etmoidales y de
línea media ya que permiten un buen abordaje de la pared interna.
El hecho de que en la infancia no sea preciso realizar descompresiones
orbitarias en los hipertiroidismos al tener mínima afectación muscular y
proptosis, no minusvalora su utilización en adultos jóvenes con magníficos
resultados estéticos y funcionales.

Figura 10. Diversos tipos de orbitotomías anteriores con
extirpación de masas orbitarias.
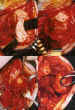
Figura 11. Orbitotomía lateral con resección del hueso orbitario y
extirpación de la masa tumoral intraconal.
TÉCNICAS QUIRÚRGICAS
(18-33)
Orbitomías anteriores
Se usa anestesia general con hipotensión inducida y microscopio quirúrgico
con iluminación coaxial.
Incisión transconjuntival
Suele acompañarse de desinserción de algún músculo en las zonas
necesarias para una buena exposición. Es preferible hacerlo ya que hay peligro
de isquemia por tracción excesiva. Se pueden alcanzar los espacios
epiesclerales, centrales y periféricos.
La ruta medial permite descomprimir el nervio óptico. Si se desinserta el
recto medial y se asocia a una orbitotomía lateral con descompresión de la
pared ósea se puede abordar el ápex orbitario con más facilidad.
La ruta inferior ha reemplazado a la transcutánea para exponer tumores del
suelo de la órbita y tratamiento de las fracturas del suelo y de la pared
medial. Se consigue un mejor abordaje si la incisión en el fórnix se acompaña
de cantotomía lateral y cantolisis.
La ruta caruncular con disección posterior al saco lagrimal permite el
acceso a la pared medial a través del espacio subperióstico. Esta incisión
tiene la ventaja de que consigue mejores resultados estéticos que la
tradicional incisión de Lynch o frontoetmoidal. Asimismo, si se asocia con una
incisión transconjuntival inferior, es muy cómoda para fracturas mediales,
descompresiones y drenaje de abcesos subperiorbitarios.
Incisión transeptal
Se utiliza la vía transcutánea. La piel de los párpados y el músculo
orbicular se abren con una incisión paralela y dentro del reborde orbitario en
la zona donde está la tumoración. La incisión del septo expone la grasa
orbitaria y abre el espacio entre los músculos y el periostio. Algunas veces se
usa la vía coronal para el abordaje de lesiones orbitarias superiores con la
disculpa de producir menos cicatriz. Sin embargo la alopecia cuando los niños
se hacen hombres puede resultar más desfigurante. Si hay que extirpar hueso y
reconstruir alguna pared tambien usamos esta vía neuroquirúrgica y luego la
transeptal.
La ruta transeptal en el párpado inferior utiliza la vía transcutánea
subciliar cuya disección por debajo del orbicular permite un fácil abordaje.
Tiene el problema de cortar el drenaje linfático y causar linfoedema
persistente postoperatorio si realizamos algún corte vertical.
La incisión de Lynch, inicialmente transcutánea, se convierte en transeptal
posteriormente. No es práctica al tener que cortar el tendón cantal interno y
deja mucha cicatriz.
La incisión vertical en el párpado superior y tercio interno, permite la
ampliación transconjuntival para remover tumores intraconales superomediales.
Incisión subperióstica
En el momento actual es preferible iniciar las incisiones en los párpados
superiores que realizar las antiguas a través de las cejas o 4 mm por encima
del reborde orbitario. La disección superior en el plano fascial postorbicular,
permite el acceso al reborde orbitario superior y el plano subperióstico evita
el prolapso de la grasa orbitaria anterior. Las incisiones coronales tienen los
mismos inconvenientes al llegar al abordaje superióstico que explicamos
anteriormente.
En el párpado inferior se utiliza la vía subcutanea infraciliar y abordamos
por debajo del orbicular el espacio del reborde donde se incide la periórbita.
Las incisiones cutáneas en el párpado inferior dejan más cicatriz.
Apertura del perióstio: La tróclea dificulta la entrada en el cuadrante
nasal superior. Debe ser desinsertada, cortando un pequeño trozo del hueso
orbitario con un cincel.
Incisión del periostio sobre el tumor: Al palparse la masa se expone
mediante una incisión sagital. Los rectos o el elevador necesitan una
retracción cuidadosa para poder penetrar en el cono muscular. La lesión puede
ser disecada y escindida, podemos tomar biopsias en otros casos y se pueden
drenar los abcesos.
Orbitotomía lateral
En niños, al ser las órbitas menos profundas podemos obtener buenos
abordajes sin necesidad de realizarla. Se puede desplazar el globo ocular con
más facilidad hacia la zona nasal previa desinserción del recto externo.
Paradójicamente se practican en abordajes mediales cuando al liberar el recto
interno no tenemos suficiente campo quirúrgico y la resección ósea temporal
permite llegar muy posteriormente a esa zona de gran compromiso. Las incisiones
antiguas se hacían en la ceja y se liberaba la región orbitaria temporal
superior. Al llegar a la altura del arco zigomático se extendían
horizontalmente sobre éste, con una extensión de 3 cm. Las cicatrices que
dejaban determinaron su sustitución por incisiones curvadas a traves del
párpado superior e incluso por cantotomías ampliadas.
Estas nuevas vías descritas en la figura 7 permiten, igualmente y mediante
abordaje subcutaneo, exponer la pared orbitaria lateral y la porción anterior
del arco zigomático con desplazamiento del músculo temporal.
El periostio se incinde a 2 mm y paralelo al margen lateral de la órbita. La
incisión se extiende hacia atrás para descubrir el techo de la órbita por
encima y el borde superior del arco zigomático por debajo.
En la órbita se libera y desperiostiza toda la parte interna de la pared
lateral. El ligamento palpebral lateral debe ser desprendido en el mismo acto
quirúrgico. Las incisiones horizontales y de la pared externa permiten la
resección del bloque óseo zigomático temporal.
Resección ósea: La fosa media craneal limita esta resección de 1,5 a 2,5
cm del reborde orbitario externo con lo que acorta el campo de abordaje en la
infancia. Las modernas fresas oscilantes han desplazado a las antiguas Stryker
que removían los pilares y el margen lateral de la órbita. Se hacen cortes
horizontales en el córner temporal y en el nivel superior del arco zigomático
tras haber hecho previamente los agujeros para su fijación posterior. Es
fundamental usar un retractor por dentro de la órbita para proteger la
periórbita y el globo ocular al realizar los cortes. Se completan con una
incisión vertical a 10 mm por detrás del reborde orbitario externo. Si es
necesario se recorta con gubias mas pared lateral hasta que el progresivo
engrosamiento nos indique que comenzamos a aproximarnos a la fosa craneal media
en el ala mayor del esfenoides.
Abordaje al tumor: El periostio orbitario se abre horizontalmente a nivel del
recto lateral, que desinsertado se intenta colocar en el cono muscular lateral a
la tumoración si ésta es encapsulada. Los tumores pueden ser prolapsados a
veces en la incisión ejerciendo presión sobre los párpados. Un criodo o
alguno de los modernos forceps de fijación que se utilizan en cirugías
endoscópicas permiten una tracción firme de los tumores encapsulados. En el
caso de hemangiomas, una lazada alrededor de la lesión permite descomprimir y
traccionar al mismo tiempo al removerlo.
Visualizando con microscopio de luz coaxial, los tumores encapsulados deben
ser disecados intentando proteger el nervio óptico y los vasos sanguíneos del
espacio retrobulbar. La disección debe ser hecha con hemostasia escrupulosa.
En los tumores infiltrativos la cirugía se limita a biopsias o escisión
parcial para descomprimir seguido de otras medidas terapeúticas más o menos
paliativas.
Solemos dejar drenajes colocados en la piel y que alcanzan los tejidos
orbitarios profundos. El periostio lo cerramos sin demasiada estanqueidad para
permitir descomprimir las hemorragias postoperatorias. El hueso se recoloca y
sutura con seda de 4(0), o con placas y tornillos de titanio si precisamos más
fijación.
Los antiguos alambres de acero que se utilizaban producen artefactos en los
TC.
Los corticosteroides suelen administrarse por vía intravenosa al inicio de
la operación y durante varios días en el postoperatorio. Si puede haber
compromiso de los senos paranasales se recomienda administrar antibióticos
antes y después de la operación. La antibioterapia profiláctica no tiene
sentido.
COMPLICACIONES DE LAS
ORBITOTOMÍAS (34-41)
• Pérdida o disminución de la visión. Por excesiva tracción del globo
ocular o del nervio óptico, contusión o hemorragia.
• Hemorragias. Si se producen en el espacio retrobulbar pueden dañar el
nervio óptico por aumento de la presión orbitaria. Hemostasia meticulosa y
drenaje postoperatorio disminuyen esta complicación. Vigilar el dolor
postoperatorio y el defecto pupilar aferente para evacuar el hematoma.
• Oclusión vascular retiniana por manipulación de estructuras cerca del
ápex orbitario.
• Atrofia óptica si se daña el nervio o se presenta una neuropatía
isquémica al manipularlo.
• Maculopatía por lesión de vasos ciliares.
• Ptosis. Por daño en el elevador, excesiva compresión con los
separadores por los ayudantes o hematomas orbitarios.
• Diplopía. Por daño de músculos, principalmente por traciones excesivas
o disecciones demasiado agresivas. En tumores infiltrativos, reintervenciones y
cápsulas muy fibrosas.
• Queratopatía neuroparalítica.
• Cambios pupilares.
• Hemorragia vítrea.
• Desprendimiento de retina.
• Hipoestesia periorbitaria y craneal.
• Queratitis seca.
• Infección.
• Exposición y perforación de la duramadre en las ventanas óseas que
realizamos o en las malformaciones congénitas quísticas o coristomatosas.
• Meningitis.
• Pseudomeningocele.
• Trombosis del seno cavernoso.
En general las complicaciones se reducen si realizamos una buena evaluación
preoperatoria y elegimos una vía de abordaje apropiada. La exposición de la
tumoración, cuidadosa manipulación de los tejidos y perfecta hemostasis. Las
relaciones interdisciplinarias con neurorradiólogos, maxilofaciales,
neurocirujanos, neurofisiólogos y otorrinolaringólogos deben ser fluidas.
TÉCNICAS ESPECIALES EN LA ÓRBITA
Biopsia por aspiración con aguja
(42-44)
La usamos en casos especiales, bajo control ecográfico o de TC. Sospechas de
reactivación, metástasis ojos ciegos con tumores del nervio óptico,
pseudotumores o tumores de contigüidad de senos y/o línea media. No obtenemos
buenos resultados en lesiones fibrosas porque es muy difícil aspirar células
de ellas. Tiene más utilidad en lesiones linfoproliferativas, aunque se
precisan pruebas complementarias de inmunohistoquímica.

Figura 12. La biopsia por aspiración mientras se realiza el TAC
helicoidal permite obtener muestras que los citólogos procesan inmediatamente.
Se usa una aguja de 4 cm y 22-23 G en una jeringa incorporada a una pistola
especial de aspiración mecánica. Se utiliza la vía transconjuntival,
transcutánea y septal. Celularidad o pequeños bloques de tejido son aspirados
de la lesión. Es indispensable contar con un citólogo experimentado ya que
pueden producise falsos positivos que obligan a planteamientos quirúrgicos más
agresivos o causan daños irrecuperables.
Endoscopia orbitaria
(45-47)
Puede ser la técnica del futuro. Hay pocas referencias en la literatura y
existe precaución en la inyección de gases en la órbita por la compresión
que pueden producir. El desarrollo experimental en animales y el inicio de su
utilización cuando el ojo es amaurótico predicen un gran campo para estas
técnicas que están consiguiendo un gran éxito en otras especialidades. La
investigación con nuevos gases e incluso con líquidos de diversa viscosidad y
la utilización de contrastes para una mejor definición es un nuevo campo y muy
interesante.
Exenteración orbitaria
(48-51)
El objetivo de una exenteración es extirpar todo el contenido orbitario con
amputación del ápex en un solo bloque requiriendo que la zona esté recubierta
por el periostio. En su forma completa incluye los párpados. Por los especiales
anclajes de la membrana periorbitaria algunas veces y en casos extremos se
incinde en las paredes óseas con cortes profundos en las hendiduras orbitarias.
Es necesaria la coagulación de los pedículos vasculares en el agujero óptico
y en las dos hendiduras.

Figura 13. Exenteración orbitaria mediante abordaje subperióstico
con desinserción del ápex orbitario mediante asa de alambre.
Se intenta conseguir la exéresis completa de un tumor maligno orbitario que
no puede ser tratado con extirpación local, quimioterapia o radiación. Es
preciso realizar estudios histológicos intraoperatorios. Si el hueso está
afectado, debe ser resecado y cuando hay extensión en el cráneo o en los senos
paranasales se hacen extirpaciones más radicales con la unidad craneofacial.
Figura 14. La exenteración es una técnica de vigencia actual,
aunque las indicaciones están más restringidas.
Si la lesión es una metástasis y no puede ser excindida completamente, se
contraindica la operación a menos que los radioterapeutas precisen utilizarla
como ayuda para la radiación.
Aunque cada vez son menos las indicaciones, no existe en la literatura
ningún trabajo que la deseche en contraposición con la creencia de algunos
oftalmólogos en nuestro país de ser casi una aberración.
Cuando el tumor esta separado del septum y hay menos riesgo de recurrencia,
los párpados pueden ser preservados y la cavidad se puede rellenar con una
trasposición del músculo temporal o con implantes expandibles de silicona.

Figura 15. Las prótesis orbitarias permiten una reconstrucción
estética integrada en el macizo craneofacial.
Estos últimos se colocan intraorbitariamente con un reservorio
retroauricular que se comunica a través de una osteotomía a 7-8 mm del margen
orbitario y pared lateral en su concavidad posterior, justo debajo del músculo
temporal en su porción anterior. Cada 5 meses y bajo control con TC helicoidal
se rellena el reservorio, para así permitir un desarrollo armónico de la
órbita.
Si no se injerta piel, la granulación de la cavidad orbitaria retrasa su
epitelización en varios meses.
En niños exenterados y radiados, la afectación ósea da con la granulación
imágenes de proliferación y crecimiento en el vértice de la órbita que
confunden a los neuroradiólogos y dan citologías y biopsias negativas.
Asimismo la remodelación del macizo craneofacial con el crecimiento produce un
aplanamiento de la cavidad orbitaria con prolapso de tejidos fibrosos y
vascularizados provenientes de las hendiduras esfenoidales, esfenomaxilares y
canal óptico. Estas proliferaciones nos mantienen expectantes al ver que se
conforma un nuevo ápex orbitario pese a que juraríamos que habíamos realizado
una extirpación radical.
Descompresión de la órbita
(7,12,17-21,26-28, 35-38,51-56)
En la infancia el exoftalmos distiroideo no precisa operaciones
descompresivas por exposición de la córnea o afectación del nervio óptico.
Tampoco es preciso usar corticoides o megadosis.

Figura 16. Los implantes de silicona con reservorio retroauriculares
permiten el desarrollo de la cavidad orbitaria mediante inyecciones repetidas de
suero fisiológico bajo control de TAC helicoidal.
Como resumen en adultos jóvenes la estética palpebral y la extirpación de
la grasa orbitaria son el primer paso terapeútico quirúrgico. Como segunda
posibilidad, las descompresiones mediales e inferiores permiten a los músculos
edematosos expandirse en los espacios periorbitarios disminuyendo la tracción
sobre el nervio óptico y su vascularización.
En las malformaciones congénitas, angiofibromas y displasias fibrosas sí se
realizan, pero son casos complejos que manejamos en la Unidad Craneofacial.

Figura 17. La orbitotomía transconjuntival con desinserción
muscular permite el acceso al espacio retrobulbar y nervio óptico.
La vía endoscópica transnasal tiene un gran futuro en las descompresiones
de la pared medial y la penetración en el seno maxilar por esa misma vía
consigue la observación, apertura y recolocación de las fracturas en el suelo
de la órbita.
Igualmente en las fenestraciones de las vainas de los nervios ópticos en los
casos de pseudotumor cerebri, podría ser la técnica de elección. Para el
abordaje del canal óptico intraorbitario y cirugía de fragmentos óseos
todavía hay mucho camino que recorrer.

Figura 18. La contusión frontal produce una neuropatía óptica
traumática con pérdida irreversible de visión pese a tratamiento con
megadosis de corticoides o descompresión del canal óptico orbitario por la
unidad craneofacial. Llamamos la atención de esta patología en golpes inocuos
sobre el reborde orbitario superior.
Recientemente se aboga en las fracturas con un gran componente restrictivo de
los rectos inferiores cambiar la apertura del suelo por la pared lateral para
evitar el atrapamiento de los músculos en el seno maxilar.

Figura 19. La orbitotomía transeptal permite la reducción de las
fracturas del suelo de la órbita y el abordaje al espacio intraconal en la zona
de la glándula lagrimal.
Las pérdidas de visión que suceden en la infancia por neuropatía óptica
traumática tras manejo quirúrgico o contusión frontal son un tema
controvertido. No tratar megadosis de corticoides o descompresión quirúrgica
del canal óptico siguen siendo las tres alternativas. El aparente éxito en los
estudios americanos de heridas agudas traumáticas de médula espinal usando
corticoides lleva su utilización a la órbita, aunque no están todavía
reflejadas en la literatura. Se precisan estudios randomizados para confirmar
las posibilidades futuras. Igualmente la inclusión de otorrinolaringólogos y
neurocirujanos expertos dentro de las unidades craneofaciales permite la
apertura del canal óptico por sus vías respectivas.

Figura 20 Los traumatismos en la órbita pueden desestructurar ésta
con fragmentos óseos que se enclavan en el globo ocular. Son urgencias
inmediatas quirúrgicas.
La vigilancia del desarrollo de la neuropatía, los corticoides a altas dosis
y la actuación quirúrgica dentro de los cinco primeros días del traumatismo
son descritos en la literatura como éxitos aislados y sin contigüidad ya que
incluso hay recuperaciones visuales sin ningún tipo de tratamiento.
BIBLIOGRAFÍA
- Henderson JW. Orbital tumors. Philadelphia. Philadelphia. WB Saunders.
1973; 1: 11-24.
- Lloyd GAS. Radiology of the Orbit. Saunders. 1975; 1: 1-29.
- Wolff´s E. Anatomy of the eye and orbit. London H K Lewis. 1976.
- Dorrell ED. Surgery of the eye. London Blackwell S P. 1978; 10: 175-178.
- Koornneef L. Sectional anathomy of the orbit Amsterdam.Aeolus Press. 1981.
- Perez Moreiras J. Patología Orbitaria. Exploración clínica,diagnóstico
y cirugía. LXII Ponencia de la Sociedad Española de Oftalmología. Barcelona
Comercial Pujades. 1986; 1: 9-22.
- Rootman J ed. Disease of the orbit: A multidisciplinary approach.
Philadelphia. Lippincott 1988. Chapter 8.
- Shields JA. Diagnosis and management of orbital tumours. Philadelphia W B
Saunders Company 1989; 1: 3-14.
- Snell RS, Lemp MA. Clinical anatomy of the eye. London Blackwell S P.
1989; 3: 52-68.
- Costa Vila, Canals Imhor M. Anatomía quirúrgica de la órbita y anejos
oculares. En: Zaragoza P. Cirugía básica de anejos oculares. LXX Ponencia
Oficial de la Sociedad Española de Oftalmología. Madrid. Tecnimedia Editorial.
1996; 1: 35-100.
- Spaetz GL, Katz LJ, Parker KW. Current therapy in ophtalmic surgery.
Toronto B.C. Decker Inc. 1989.
- Moore A, Blazer J. In: Taylor D. Paediatric Ophthalmology. Orbital
disease in children. Oxford. England Blackwell SC. 1990; 22(1): 208-212.
- Galán Terraza A. Orbita. En: Gil-Gibernau JJ. Oftalmología en la
infancia. Clínica, diagnóstico y tratamiento. Barcelona Scriba SA. 1991; 10:
221-223.
- Osttler HB. Disease of the external eye and adnexa A test and Atlas.
Baltimore, Maryland, William & Wilkins. 1993; 7: 313-359.
- Gil-Gibernau JJ. Tratado de Oftalmología Pediátrica. Barcelona
Comercial Pujades. 1997; 10: 221-224.
- Junceda J, Hernandez LC, Sainz Ayala A, et al. Anatomía radiológica de
la órbita y globo ocular.Madrid. IM & C 1992; 10: 221-224.
- Lyons C, Rootman J. In: Taylor D. Paediatric Ophthalmology. Orbital
disease in children. Oxford England Blackwell Sciance 1997; 27: 302-308.
- Albert DM, Ophthalmic Surgery. Principles and Techniques. Blackwell
Sciance. Oxford. England 1999; 5: 1.432-1.648.
- Shields JA, Bakewell B, Augsburger JT, et al. Space ocuping orbital
masses in children. A review of 250 consecutive biopsies. Ophthalmology 1986;
93: 379-384.
- Bullock JD, Goldberg SH, Rakes SM. Orbital tumors in children. Ophthal
Plast Reconstr Surg. 1989; 5: 13-16.
- Bullock JD. Orbital tumours in childhood. Ophthalmology 1986; 933:
384-387.
- Kennerdell JS, Maroon JC, Celin SE. The posterior inferior orbitotomy.
Ophthalmic Plast Reconstr Surg 1998; 14(4): 277- 280.
- Arai H, Sato K, Katsuta T, Rothon A. Lateral aproach to intraorbital
lesions: anatomic and surgical considerations. Neurosurgery 1996; 39(6):
1.157-1.163.
- Shorr N, Baylis HI, Goldberg RA, Perry JD. Transcaruncular approach to
the medial orbit and orbital apex. Ophthalmology 2000; 107(8): 1.459-1.463.
- Rueda Franco F, Marhx Bracho A. Tumores orbitarios en niños.Su abordaje
quirúrgico transcraneal. Gac Méd Méx 1998; 134(5): 529-536.
- Goldberg RA, Steinsapir KD. Extracranial optic canal decompression:
indications and technique. Ophthal Plast Reconstr Surg 1996; 12: 163-170.
- Lee AG, Patrinely JR, Edmond JC. Optic nerve sheat descompresion in
pediatric pseudotumor cerebri.Ophthalmic Sur Lasers 1998; 29: 5 14-517.
- Snyder BJ, Hanieh A, Trott JA, David DJ. Transcranial correction of
orbital neurofibromatosis. Plast Reconstr Surg 1998; 102(3): 633-642.
- Sherman RP, Rootman J, La Pointe JS. Orbital dermoids:clinical
presentation and management. Br J Ophthalmol 1984; 68: 642-652.
- BartlleT T , Lin KY, Katowitz J. The surgical management of orbitofacial
dermoids in the pediatric patients. Plast Reconstr Surg 1993; 91: 1.208-1.215.
- Archer DB, Gordon DS, Maguire CJF, et al. Ophthalmic aspects of
craniosinostosis Trans Ophthalmol Soc UK 1974; 94: 172-196.
- Aldave AJ, Shields CL, Shields JA. Surgical excision of selected
amblyogenic periorbital capillary hemangiomas. Ophthalmic Surg Lasers 1999;
30(9): 754-757.
- Alper M, Gurler T, Bilkay U, et al. Intraorbital osteoma and surgical
strategy. J Craniofac Surg 1998; 9: 464-467.
- Yee RD, Cogan DG, Thorp R, et al. Optic nerve compression due to
aneurysmal bone cyst. Arch Ophthalmol 1997; 95: 2.176-2.179.
- Dufier JL, Vinurel MC, Renier D et al. Les complications
ophthalmologiques des craniofaciostenoses. A propos de 244 obsevations. J Fr
Ophthalmol 1986; 9: 273-280.
- Oh AK, Kim S, Wang KC, et al. Complications of pediatric craniofacial
surgery in the Orient: analysis of 10 year experience. J Craniofac Surg 1997; 8:
340-351.
- Wong GB, Kakulis EG, Mulliken JB. Analisis of fronto-orbital advancement
for Apert, Crouzon, Pfeifer and Saethre-Chotzen syndromes. Plast Reconstr Surg
2000; 105(7): 14-23.
- Guyuron B, Schlechhter B. Pseudomeningocele as a complication of teratoma
resection and aseptic meningitis following craniofacial reconstruction: a case
report. J Craniofac Surg 1990; 1(4): 179-181.
- Neuman D, Isemberg SJ, Rosembaum AL, et al. Ultrasonographically guided
injection of corticosteroids for the treatment of retroseptal capillary
hemangiomas in infants. JAAPOS 1997; 1(1): 34-70.
- Taylor W, Moseley I. Visual loss in retrobulbar cavernous haemangiomas
investigated by computed tomography. Neuroradiology 1994; 36: 166-168.
- Sankrithi UM, Li Puma JJ. Clinical innaparent meningitis complicating
periorbital cellulitis. Pediatr Emerg Care 1991; 7(1): 28-29.
- Kaw IT, Cuesta RA: Nodular fasciitis of the orbit diagnosed by fine
needle aspiration ciytology. A case report. Acta Cytol 1993; 37: 957-960.
- Galera-Ruiz H, Gomez-Angel D, Vazquez-Ramirez FJ, Sanguino-Fabre JC,
Salazar Fernandez E, Gonzalez-Hachero J. Fine needle aspiration in the
preoperative diagnosis of melanotic neuroectodermal tumor of infancy. Journal of
Laringology and Otology 1999; 113: 581-584.
- Yakulis R, Dawson RR, Wang SE, Kennerdell JS. Fine needle aspiration
diagnosis of orbital plasmacytoma with amyloidosis. A case report. Acta Cytol
1995; 39(1): 104-110.
- Kuppersmith DB, Alford EL, Patrinely JR, et al. Combined
transconjunctival-intranasal endoscopic approach to the optic canal in traumatic
optic neuropathy. Laryngoscope 1997; 107: 311-315.
- Luxemberg W, Stammmberger H, Jebeles JA, et al. Endoscopic optic nerve
decompression: the Graz experience. Laryngoscope 1998; 108: 873-882.
- Kountakis SE, Maillard AA, El -Harazi SM, et al. Endoscopic optic nerve
decompression for traumatic blindness. Otolaryngol Head Neck Surg 2.000; 123:
34-37.
- Lucarelli MJ, Gausas RE, Lemke BN. Exenteration. In: Albert DM,Ophthalmic
Surgery. Principles and Techniques. Blackwell Sciance. Oxford. England 1999;
5(95): 1.553-1.565.
- Levin PS, Dutton JJ. A 20 year series of orbital exenteration. American J
Ophthalmology 1991; 112(15): 496-501.
- Lee YH, Kim HC, Lee JS, ParkWJ. Surgical reconstruction of the contracted
orbit. Plas Reconstr Surg 1999; 103(4): 1.129-1.136.
- Fountain TR, Goldelberg S, Murphree AL. Orbital development after
enucleation in early chilhood. Ophthalmic Plas Reconstr Surg 1999; 15(1): 32-36.
- Papay FA, Morales L, Flaharty P, et al. Optic nerve decompression in
craneal base fibrous dysplasia. J Craniofac Surg 1995; 6: 5-14.
- Seiff SR. Optic nerve decompression in fibrous dysplasia: Indications,
efficacy, and safety. Plast Reconstr Surg 1997; 100: 1.611-1.612.
- Haertstein ME, Grove AS, Woong JJ, et al. The multidisciplinary
management of psammomatoid ossifying fibroma of the orbit. Ophthalmology 1998;
105: 591-595.
- Harris GJ, Garcia GH, Logany SC, Mhurphy ML. Correlation of preoperative
computed tomography and postoperative ocular motility in orbital blowout
fractures. Ophthalmic Plas Reconstr Surg 2000; 16(3): 179-187.
- Levin LA, Beck RW, Joseph MP, et al. The treatment of traumatic optic
neuropathy. Ophthalmology 1999; 106: 1.268-1.277.
|