|
INTRODUCCIÓN
Las aplicaciones de los métodos
de imagen a la cirugía orbitaria, al igual que a otras áreas quirúrgicas,
han experimentado un cambio total debido a los grandes avances tecnológicos
de los últimos tiempos. La ecografía o ultrasonografía (US), con las
aportaciones del Doppler y la imagen tridimensional (todavía no de uso
clínico habitual), ha hecho de esta prueba el mejor medio de despistaje
en el estudio de la patología del globo ocular. También la angiografía
digital, donde la mejora de los materiales ha disminuido de forma
significativa la morbimortalidad, ha podido ampliar sus indicaciones, en
especial en los tratamientos endovasculares.
Pero es, sobre todo, en
el campo de la tomografía computada (TC) y resonancia magnética (RM),
donde se han producido los cambios más significativos, que han
permitido al neurorradiólogo, no sólo mejorar su capacidad diagnóstica,
sino aportar información de gran ayuda en la planificación de cirugías
complejas e incluso al mismo acto quirúrgico. Desde que en 1972
Hounsfield realizara el primer estudio cerebral con un tomógrafo
experimental a la actualidad, la evolución de la TC ha sido
vertiginosa. El último gran avance en este campo, la TC helicoidal ha
dado una nueva dimensión a esta técnica. Combinando el movimiento de
rotación del tubo y el de traslación de la mesa a través del mismo,
se crea un movimiento en hélice o espiral que permite una adquisición
volumétrica de datos similar a la que se realiza en RM. Esto consigue,
por una parte, disminuir de forma muy importante los tiempos de
exploración (30 segundos para la realización del estudio completo) y
la dosis de radiación y, por otra, hacer reconstrucciones en distintos
planos con sólo una mínima pérdida de calidad respecto a la proyección
basal (figura 1).
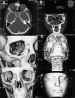
Figuras 1a, b, c, d, e y f. Imagen axial (a) en técnica espiral con
reconstrucciones biplanares coronal (b), y de superficie de estructuras óseas
(c, d, e) y de piel (f). Se observa fractura de la lámina papirácea (a) con
hundimiento del suelo (b) y con esquirla ósea. En las reconstrucciones
tridimensionales de superficie puede valorarse su repercusión estética.
La RM también ha
avanzado mucho técnicamente y la órbita ha sido una de las regiones
que más se ha beneficiado de estos avances. En un principio, la
resolución en este área era menor a la de otras técnicas debido a su
situación periférica y a la movilidad de su estructura más grande, el
globo ocular. Además, tanto la US como la TC tenían una capacidad
diagnóstica especialmente alta en este área. Por ello se ha trabajado
en encontrar soluciones para paliar estas dificultades. Entre estos
avances destaca la aparición de las secuencias rápidas (fast o turbo),
de similares características a las convencionales pero con una
importante reducción de tiempo en la adquisición de datos. Estas
secuencias han disminuido el número de artefactos de movimiento y han
permitido mejorar la imagen, al poder utilizar matrices de alta resolución
manteniendo el tiempo de exploración en unos límites aceptables. Otro
gran avance ha sido la aparición de antenas de superficie, que son
bobinas de exploración de pequeño diámetro que se colocan sobre la
superficie a estudiar, consiguiendo aproximar al máximo la zona de
interés a la antena receptora y eliminando el ruido que producen áreas
cercanas a la órbita pero fuera del campo de interés. De esta forma,
se logra aumentar la relación señal-ruido que es la que marca la
calidad de la imagen. Existen algunas dificultades en el uso de esta
antena: no permite explorar el vértice orbitario ni el compartimento
intracraneal, áreas de especial interés en la valoración de la
diseminación tumoral. Además las secuencias largas (como las
secuencias con potenciación T2) son más susceptibles de artefactos
cuando se utiliza.
Es importante reseñar
que en el Hospital Infantil La Paz, y dentro de la población pediátrica
hay dos factores especialmente importantes que debemos considerar a
la hora de decidir cuál es el método diagnóstico más adecuado para
cada caso:
— La necesidad de sedación
en gran parte de los pacientes. Por ello, hay que utilizar, a igual
rendimiento, el más rápido posible, que puede evitar la necesidad de
largas anestesias.
— La radiación.
Según la Comisión Internacional de protección radiológica (CIPR), la
mayor esperanza de vida de los niños da lugar a una mayor manifestación
potencial de los efectos tardíos de la radiación, como la carcinogénesis.
Por tanto, la utilización de todas los recursos que permitan optimizar
la prueba disminuyendo la dosis de radiación deben ser especialmente
utilizadas en ellos, incluso a expensas de perder cierto grado de
resolución. Todo esto debe realizarse manteniendo lógicamente la
capacidad diagnóstica de la prueba.
Teniendo en cuenta estas
consideraciones, la elección se basará en las ventajas y desventajas
de cada técnica, adaptándose a las circunstancias concretas de cada
caso (disponibilidades de aparataje, edad del niño, urgencia de la
prueba, etc.).
En este capítulo, además
de hacer una revisión del diagnóstico neurorradiológico en las
patologías orbitarias infantiles frecuentemente quirúrgicas a la luz
de la evolución de las técnicas de diagnóstico por imagen,
incidiremos especialmente en sus nuevas aplicaciones para planificación
y guía quirúrgica.
DIAGNÓSTICO NEURORRADIOLÓGICO
DE LA PATOLOGÍA ORBITARIA DE TRATAMIENTO QUIRÚRGICO HABITUAL
Tumores del globo ocular:
retinoblastoma
El retinoblastoma (RTB)
es el tumor intraocular más frecuente en la infancia, diagnosticándose
con mayor frecuencia entre un año y medio y dos de edad. Puede ser uni
o bilateral (1/3 de los casos). El diagnóstico inicial suele ser
oftalmoscópico. Las técnicas de imagen son imprescindibles para
detectar la patología en aquellos casos que se presenten con leucocoria
(60% de los pacientes según Kaufman) (1) y en todos los casos
necesarias para confirmar el diagnóstico clínico y realizar un diagnóstico
diferencial, ya que aportan datos sobre las características del
proceso, extensión orbitaria y al SNC, así como sobre la respuesta al
tratamiento (2).
La ultrasonografía
(US) debe ser la técnica inicial tras la exploración oftalmológica.
Se trata de una técnica ampliamente disponible e inocua tanto por no
emplear radiaciones ionizantes como por realizarse sin sedación del
paciente.
La fiabilidad diagnóstica
de la US es alta ya que detecta masas únicas o múltiples de pequeño
tamaño (menores de 2 mm), heterogéneas, con calcificación (detectada
con esta técnica hasta en un 85-90% de los casos), y desprendimiento de
retina.
El uso del Doppler es
capaz de detectar vasos en los tumores no calcificados y ayuda en el
diagnóstico diferencial en casos de RTB atípicos.
La US dadas las ventajas
referidas es muy útil para realizar controles evolutivos de respuesta
al tratamiento, según el tamaño y el grado de calcificación y
vascularización (3).
Más del 90% de los RTB
muestran calcificación en tomografía computada (TC),
generalmente en la porción posterior del globo (4). Su aspecto es
variable, única o múltiple, finas o gruesas. Si el tumor es pequeño
la calcificación puede ser difícil de identificar (5). La TC permite
hacer cortes seriados de 1,5 a 3 mm de espesor o estudiar un volumen
orbitario mediante técnica helicoidal. En el estudio con contraste
intravenoso el realce tumoral es mínimo o moderado, no obstante puede
ayudar a identificar enfermedad retrobulbar e intracraneal aunque para
ello es más sensible la resonancia magnética (figuras 2a y 2b).

Figuras 2a, b y c. Retinoblastomas bilaterales calcificados.
Imágenes axiales mediante TC (a, b) y secuencia potenciada en T2 de RM. El
calcio se define mejor en el estudio de TC.
La resonancia magnética
(RM) muestra menor sensibilidad en la detección de calcio que la US o
la TC, sin embargo supera a estas dos técnicas en la valoración de
extensión local, diseminación al SNC y en el diagnóstico diferencial
con entidades que simulan al RTB (1) (figura 2c). El tumor aparece iso o
levemente hiperintenso respecto al vítreo en secuencia eco de espín
potenciada en T1 (SET1) en relación a hemorragia intratumoral y al depósito
de sustancias paramagnéticas asociadas a calcificaciones tumorales (6)
(figura 3). En secuencia eco de espín potenciada en T2 (SET2) la señal
del tumor es hipointensa respecto al vítreo. El grado de extensión
local se valora tras la administración de gadolinio intravenoso
mediante secuencias SET1 con saturación de la grasa. Aunque el realce
tumoral es variable, siempre ha de realizarse estudio con contraste ya
que ayuda a identificar enfermedad retrobulbar (4).
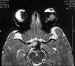
Figura 3. Secuencia axial potenciada en T2 de retinoblastoma
bilateral con hemorragia vítrea asociada en el lado izquierdo.
Los protocolos de imagen
en el diagnóstico del RTB deben incluir la búsqueda de tumores
asociados de línea media, de la región pineal en el 75% de los casos y
supra o paraselares en el 25% (RTB trilateral) (7).
Tanto la TC como la RM
son fundamentales para establecer el diagnóstico diferencial con
lesiones simulantes de RTB entre ellas la enfermedad de Coat o
teleangiectasia retiniana, meduloepitelioma, osteoma coroideo, etc. (1).
Las técnicas de imagen y
en especial la RM juegan un papel primordial en el control de la
respuesta al tratamiento. Tras la enucleación e implantación de prótesis
porosas de hidroxiapatita, Medpor o Alumina la RM permite valorar la
revascularización previa a la colocación del vástago con una eficacia
global de un 90% (2).
Aunque algunos autores
propugnan la US como método de seguimiento, en nuestra experiencia,
tras revisar los estudios de RM y TC de 31 niños con RTB tratado con
quimioterapia, la RM es el método más adecuado para evaluar la
respuesta al tratamiento. Es posible valorar la reducción del tamaño
tumoral, la presencia de tejido tumoral activo, así como la asociación
con hemorragia y desprendimiento de retina. La valoración cuantitativa
de la reducción tumoral ha de ser rigurosa, realizando las medidas en
planos y secuencias similares en todos los controles.
El protocolo más idóneo
en el diagnóstico de RTB consistiría en la realización de:
— US.
— TC sin contraste para
la detección de calcificaciones, si fuese posible mediante técnica
helicoidal.
— RM sin y con Gadolínio,
empleando técnica de saturación grasa.
Los controles deben
realizarse por lo menos cada seis meses con RM complementado con ecografías
bimensuales (2).
Tumores orbitarios
El estudio por imagen es
esencial en el diagnóstico de masas orbitarias. La TC y la RM confirman
la presencia de lesión, definen su localización y extensión
periorbitaria o intracraneal. El diagnóstico definitivo se realizará
por biopsia.
Algunos autores plantean
el dilema de cual de las dos técnicas se debe usar y en que orden. Como
regla general recomiendan la RM como 1ª en procesos neuro-oftálmicos,
lesiones del nervio óptico, así como en lesiones orbitarias en las que
se sospeche extensión intracraneal. La TC se acepta como modalidad de
elección en otros procesos orbitarios dado que permite valorar las
estructuras óseas orbitarias con una buena delimitación de tejidos
blandos. En casos complicados ambas técnicas deben ser realizadas
complementándose la una a la otra (8).
Los tipos de tumores
orbitarios encontrados en la población pediátrica por orden de
frecuencia son quistes, lesiones vasculares, tumores del nervio ópticos
y meninges, masas inflamatorias, lesiones óseas y fibroquísticas y
rabdomiosarcoma (9). Las lesiones vasculares son tratadas específicamente
más adelante en un apartado distinto, dada su complejidad.
Quistes dermoides y
epidermoides
Los quistes dermoides y
epidermoides son lesiones benignas del desarrollo y representan el tipo
más frecuente de masa orbitaria en niños. Se suelen diagnosticar en la
primera década de la vida especialmente cuando son superficiales o
subconjuntivales (8). La localización más frecuente de los quistes
dermoides es el cuadrante superotemporal junto a la sutura frontozigomática,
debido a que su origen está en relación con el secuestro de epidermis
en las suturas durante el desarrollo orbitario. La TC muestra una
lesión quística de pared fina y lisa con un centro de baja atenuación.
Los quistes dermoides, dependiendo de su contenido, pueden mostrar
densidad grasa, niveles líquido-líquido y calcio. El realce con
contraste suele ser nulo o leve en la pared. Pueden causar remodelación
o erosión ósea. En RM los quistes dermoides aparecen como
lesiones redondeadas u ovales con intensidad de señal variable
dependiendo de su contenido. Son de modo característica hipointensos
con respecto a la grasa en imágenes T1 e hiperintensos en T2, aunque
pueden tener áreas con intensidad de señal idéntica a la grasa en
todas las secuencias. Los niveles grasa-líquido son patognomónicos
(10). Los quistes epidermoides no suelen contener grasa, su intensidad
de señal es similar a la del líquido excepto en aquellos con
componente hemorrágico o proteináceo intralesional hiperintensos en imágenes
T1.
Tumores del nervio óptico
y meninges
• Glioma del nervio
óptico:
El glioma del nervio óptico
o astrocitoma pilocítico juvenil es un tumor benigno, de lento
crecimiento, que se asocia con frecuencia a neurofibromatosis en
especial cuando es bilateral.
La TC muestra un
aumento de grosor liso y fusiforme del nervio óptico aunque también
puede verse tortuoso dependiendo del patrón de crecimiento del tumor. A
diferencia con el meningioma la calcificación es rara. Suelen mostrar
un realce con contraste moderado y uniforme. Si el tumor se ex tiende al
canal óptico la imagen en ventana de hueso muestra ampliación y
remodelación del canal.
Como ya se comentó
anteriormente en este capítulo, la RM es la técnica de elección
en el diagnóstico del glioma del nervio óptico para determinar su
extensión intracanalicular, quiasmática e intracra neal profunda, sin
artefactos en la imagen por estructuras óseas circundantes. La
intensidad de señal suele ser similar a la de la sustancia blanca
cerebral tanto en secuencias T1 como T2. El realce con gadolínio puede
ser moderado o intenso (figura 4).

Figuras 4a, b y c. Glioma del nervio óptico. Secuencia axial
potenciada en T1 tras la administración de Gadolínio (a, b) que muestra el
tumor del nervio óptico derecho que no llega al quiasma. Una reconstrucción
biplanar (c) logra delimitar mejor la extensión tumoral así como su componente
quístico.
• Meningioma:
El meningioma de la vaina
del nervio óptico o del ala del esfenoides con extensión a la órbita
es menos frecuente en niños aunque también es posible encontrarlo. Se
observa un engrosamiento fusiforme con márgenes irregulares, puede
presentar calcificación en TC y realza con contraste. La RM muestra el
tumor que suele ser isointenso con respecto al nervio en T1 y T2, con
intensa captación de contraste alrededor del nervio óptico
hipointenso.
Lesiones óseas y fibroquísticas
La lesión más frecuente
en este grupo es la displasia fibrosa que puede afectar cualquier hueso
de la órbita. Los estudios de imagen muestran un engrosamiento difuso
con aumento de la densidad en TC e intensidad de señal variable en RM.
Otras lesiones menos frecuentes son las lesiones fibro-óseas benignas,
y lesiones malignas como el osteosarcoma y el sarcoma de Ewing.
Rabdomiosarcoma (RMS)
El rabdomiosarcoma es el
tumor maligno más frecuente en la infancia, representa el 4-8% de las
masas orbitarias biopsiadas según la serie de Shields y cols. (11).
El diagnóstico debe ser
precoz ya que un tratamiento precoz con quimio y radioterapia mejora
dramáticamente la supervivencia. La TC y la RM juegan un importante
papel en la evaluación preoperatoria y en el estadiaje.
Suele presentarse en niños
de 7-8 años de edad con proptosis unilateral progresiva de evolución rápida.
La localización más frecuente es el cuadrante superonasal aunque puede
afectar a más de uno. El tumor es indistinguible del cono muscular que
se encuentra desplazado o englobado en la lesión aunque la mayoría de
los tumores se desarrollan independientes del cono a partir, de células
mesenquimales indiferenciadas (12). Puede extenderse fuera de la órbita
y con menor frecuencia dar metástasis hematógenas a pulmón, hígado y
cerebro.
La TC muestra una
lesión isodensa con el músculo normal, homogénea, de márgenes bien
definidos.
El tamaño es variable,
menor o similar al globo ocular mostrando éste desplazamiento o
deformación posterior aunque no suele estar invadido (12).
La captación de
contraste es leve-moderada y homogénea.
Los tumores grandes
suelen tener márgenes peor definidos y al estar en contacto con los márgenes
óseos orbitarios pueden adelgazar o erosionarlos e invadir estructuras
vecinas como la glándula lacrimal o el nervio óptico (figura 5).

Figuras 5a y b. Rabdomiosarcoma orbitario izquierdo. Secuencia
potenciada en T1 con gadolínio y saturación grasa (a) y potenciada en T2 (b).
El tumor impronta el globo ocular y el cono muscular.
La RM muestra una
masa de intensidad de señal similar al músculo o al cerebro en T1,
hiperintensa en T2. La intensidad de señal puede variar si el tumor
presenta áreas de hemorragia focal. El realce con contraste paramagnético
es moderado-marcado.
La RM demuestra la
extensión del tumor a senos paranasales (seno etmoidal) así como al
compartimento intracraneal a través de la fisura orbitaria inferior.
Hay autores que defienden
la superioridad de la RM como modalidad de imagen en el diagnóstico del
RMS para detectar, evaluar extensión debido a su mejor resolución de
contraste y a su capacidad multiplanar (13). Además es muy útil en el
diagnóstico diferencial con otras lesiones orbitarias que causan
proptosis y que por su intensidad de señal característica permiten
hacer un diagnóstico más específico. Este es el caso de lesiones quísticas
benignas, lesiones hemorrágicas (hematoma subperióstico) o
lipomatosas, lesiones óseas o condrogénicas (14).
El diagnóstico
diferencial con lesiones inflamatorias (poco frecuentes en esta edad) así
como con otros tumores orbitarios (leucemia, linfoma, hemangioma,
linfangioma, granuloma eosinófilo) (figura 6), tumores de nervio periférico
(el más frecuente el neurofibroma) (figura 7) puede ser más dificil ya
que pueden presentar una intensidad de señal similar al RMS. En algunos
casos es preciso diagnóstico histológico (15).

Figuras 6a y b. Granuloma eosinófilo que destruye el techo
orbitario izquierdo e invade el parénquima cerebral. Secuencias de RM
potenciadas en T1 con Gadolínio coronal (a) y sagital (b).
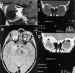
Figuras 7a, b, c y d. Neurinoma extraconal. Secuencia sagital T1 (a)
y axial DP que muestra la lesión de localización extraconal. Las
reconstrucciones coronales en ventana ósea (c) y parenquimatosa (d) de TC
helicoidal permiten ver la lesión pue produce remodelación ósea, hallazgo
típico de las lesiones de lento crecimiento.
Las técnicas de imagen
también juegan un importante papel en la detección de masa residual y
recurrencia tumoral. Para ello es preciso realizar TC o RM tras
completar el tratamiento, estudios que servirán de base para comparar
con estudios de control y así detectar de forma precoz recaídas (14).
Metástasis
Las lesiones secundarias
o metastásicas representan menos de la mitad de las lesiones orbitarias
malignas en niños (9).
El tumor más frecuente
es el RTB ocular con invasión local orbitaria.
Los tumores que con mayor
frecuencia metastatizan en la órbita en niños son el neuroblastoma y
el sarcoma de Ewing. La TC y la RM muestran una lesión focal o
infiltrativa.
Las leucemias tambien
pueden afectar a la órbita siendo los cloromas una de las causas de
exoftalmos (figura 8).

Figuras 8a, b y c. Cloromas. TC axial con contraste intravenoso
yodado que muestra tres lesiones en rama mandibular izquierda (a), pared
orbitaria inferolateral derecha (b), y la de mayor tamaño en pared orbitaria
lateral izquierda. Las 3 corresponden a cloromas.
Tumores orbitarios
vasculares infantiles
Papel de las distintas técnicas
de imagen
En la infancia, los
tumores vasculares ocupan estadísticamente el segundo puesto en
frecuencia, después de los tumores quísticos (9,16). Las series de
Belmekki, Kodsi y Cotton, (9,16,17), coinciden en que suponen del 18-20%
del total de los tumores orbitarios infantiles, incluyendo primarios y
secundarios. Dada la complejidad de su diagnóstico diferencial, hemos
preferido tratarlos de forma separada del resto de los tumores
orbitarios.
Las nuevas técnicas de
imagen han adquirido un papel muy importante en la caracterización de
estas lesiones y son fundamentales, en las decisiones terapéuticas, en
el control evolutivo de las mismas, y en caso de que sea necesaria la
cirugía en la planificación del abordaje quirúrgico. La información
es fundamental cuando las lesiones son profundas y no revelan su carácter
vascular en el examen clínico.
Todas las técnicas de
imagen pueden ser útiles en el diagnostico de las lesiones orbitarias
vasculares: placa simple, US, tomografía computada (TC) y resonancia
magnética (RM). Sólo en casos de diagnóstico dudoso o cuando se
plantee un tratamiento endovascular, hay que recurrir a la arteriografía.
La venografía orbitaria era muy utilizada hasta hace unos años, pero
con la aparición de las nuevas técnicas (TC y RM), ha caído en desuso
y sólo se utiliza en contadas ocasiones (18).
En la radiología simple,
que aporta muy poca información, podemos ver remodelación ósea
orbitaria, agrandamiento del agujero óptico o de la hendidura
esfenoidal, e incluso calcificaciones en las varices o en los
hemangiomas cavernosos, pero estos dos hallazgos (alteraciones óseas y
calcificaciones), se ven mejor en la TC que, además, nos proporciona
información sobre otras estructuras del contenido orbitario.
La US es una técnica
accesible, fácil de realizar y puede ser muy útil como estudio inicial
para descartar otras patologías orbitarias y sobre todo intraoculares.
Con US analizamos la naturaleza de la lesión y se puede diferenciar
claramente entre tumores quísticos y sólidos, también en los procesos
vasculares (19,20), con la introducción del Doppler pulsado y del
Doppler color, podemos ver la vascularización tumoral y medir la
velocidad del flujo de los vasos que la componen. Como es una prueba dinámica,
en las varices se puede distinguir si la lesión es depresible y si
cambia con las maniobras de Valsalva o con los cambios posturales.
Los tumores orbitarios
generalmente son hiperecogénicos, aunque pueden presentar en su
interior áreas quísticas o hemorrágicas, que se manifiestan como
zonas hipoecoicas. Cuando hay flebolitos, se pueden ver las
calcificaciones.
Cuando la US es normal no
es necesario realizar más pruebas si no hay discordancia clínica, pero
cuando es dudoso o patológico, debemos continuar con TC o RM.
La TC tiene mayor poder
de resolución que los ultrasonidos, por lo que se pueden delimitar
mejor las lesiones, su morfología, sitio de origen y grado de afectación
de las estructuras que los rodean, se diferencia muy bien la grasa
orbitaria de los músculos, nervio orbitario y contenido ocular, en
cambio para la valoración intraocular es superior la US.
Los procesos vasculares
son casi siempre masas de alto valor de atenuación con gran captación
tras la introducción de contraste intravenoso, ésta puede ser homogénea
o heterogénea pero con frecuencia muy intensa.
La RM permite obtener imágenes
en varios planos diferentes sin necesidad de movilizar al paciente,
tiene gran capacidad de discriminación de tejidos blandos y supera a la
TC ampliamente en la valoración de la relación del proceso tumoral con
las estructuras adyacentes. Esto es especialmente cierto cuando hay
extensión intracraneal; en estos casos es la única técnica capaz de
valorar el proceso con seguridad, pues es una prueba muy segura
detectando la existencia de hemorragia y la presencia de vasos patológicos.
Únicamente el calcio se ve peor que en la TC, por lo que, para asegurar
un diagnóstico correcto, a veces hay que realizar las dos técnicas (TC
y RM), ya que muchos procesos se presentan con imágenes poco específicas.
Diagnóstico diferencial
de los tumores vasculares orbitarios
Los tumores vasculares
orbitarios más frecuentes en la infancia, ya hemos dicho que son el
hemangioma capilar (figura 9) y el linfangioma (figuras 10 y 11), pero
también, aunque son más raros, se pueden ver los hemangio-pericitomas
y los hemangiomas cavernosos. La varíz orbitaria, es una malformación
venosa generalmente congénita que se manifiesta con frecuencia en las
primeras décadas de la vida y es la principal causa de hemorragias
orbitarias. Hay otras entidades mucho menos frecuentes en la infancia
como la malformación arteriovenosa y la fístula carótido-cavernosa
que producen aumento de tamaño de las venas orbitarias (17).
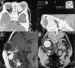
Figuras 9a, b, c y d. Hemangioma capilar. TC axial con adquisición
helicoidal (a) con reconstrucción sagital (b). RM en secuencias sagital T1 y
coronal T2 (c, d). Masa intra-extraconal hipercaptante con imágenes de vacío
correspondientes a pequeños vasos en la RM (a).
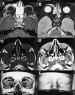
Figuras 10a, b, c, d, e y f. Típica localización de linfangioma
orbitario en la región cantomeatal. Secuencias potenciada en T1 con gadolínio
(a) y en T2 (b) en las que no se observa afectación retrobulbar. TC axial en
ventana ósea (c) y parenquimatosa (d) con reconstrucción tridimensional ósea
(e) y de piel (f) muestran asimetría de párpado inferior y ausencia de
afectación ósea.

Figuras 11a y b. Linfangioma: Secuencias coronal (a) y axial (b)
potenciadas en T2 que muestran la lesión interconal multilobulada que brilla en
T1 y T2.
Los tumores vasculares
con frecuencia están presentes en el nacimiento o se manifiestan en los
primeros 5 años de vida (16), es el hemangioma cavernoso el que aparece
mas tardíamente. En algunas series, hay predominio del sexo masculino,
en cambio en la revisión de Kodsi (9), afecta por igual a ambos sexos.
Todos ellos tienen muchas
características en común y muchas veces las imágenes radiológicas
son inespecíficas, por eso su diagnóstico resulta complicado y por lo
tanto habrá que tener en cuenta multiples factores como son: edad de
aparición, localizacion, velocidad de crecimiento y presentación
radiológica, para con todos estos datos intentar llegar a un diagnóstico
lo más preciso posible.
El crecimiento de estas
lesiones es lento excepto el del hemangioma capilar que crece rápidamente
durante los 6-10 meses de vida a partir de los cuales involuciona
progresivamente (18). El linfangioma que es de crecimiento lento, puede
aumentar de tamaño bruscamente por sufrir hemorragia, esta misma
complicación también es frecuente en las varices (21).
La localización más
frecuente de los procesos vasculares orbitarios es extraconal, excepto
el hemangioma cavernoso, que es intraconal, y los linfangiomas y las
varices (figura 12) que son mixtas, de situación intra y extraconal. El
hemangioma capilar puede extenderse al interior del cráneo a través de
la fisura orbitaria inferior, el canal óptico, o el techo de la órbita.
(6).
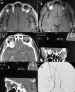
Figuras 12a, b, c, d, e y f. Variz de la vena oftálmica superior.
Secuencia axial potenciada en T1 pre y post administración de gadolínio (a,
b). Corte axial con contraste yodado a nivel de la lesión (c) con
reconstrucciones biplanares coronales (d) y sagitales (e). Angiografía venosa
de la lesión (f). Se observa lesión en región teórica de la vena oftálmica
superior que capta contraste marcadamente, y en la angiografía venosa (f) se
observa el teñido correspondiente a la variz.
Con US las malformaciones
venosas son anecoicas, pero pueden ser heterogéneas si la variz esta
parcialmente trombosada. El registro Doppler es de flujo venoso
cambiando con la maniobra de Valsalva. La fístula arteriovenosa produce
dilatación de la vena oftálmica superior, hay inversión del flujo
venoso normal que, además, presenta registro arterializado (6,22).
Los tumores vasculares
son masas homogé neas, bien o mal delimitadas pero casi siempre
hipoecoicas con vascularización muy evidente, algunos pueden tener
componentes quísticos como los linfangiomas. El único proceso con
características ecográficas típicas que permite un diagnóstico
bastante seguro, es el hemangioma cavernoso, que es intraconal, muy bien
delimitado con respecto a la grasa orbitaria con aspecto ecográfico en
«panal de miel» (22). La presencia de calcio no es muy frecuente,
aparece en primer lugar en las varices y con menor frecuencia en los
hemangiomas cavernosos, la imagen será de pequeños nódulos hiperecogénicos
con sombra acústica posterior.
En la TC suelen tener
valor de atenuación alto y captan contraste de forma intensa y homogénea,
la excepción es el linfangioma que es más heterogéneo (quístico) y
que puede mostrar captación de contraste leve y heterogénea.
Como en todas las pruebas
el mejor delimitado es el hemangioma cavernoso que tiene forma
redondeada u oval y límites muy nítidos, en cambio el hemangioma
capilar y el hemangiopericitoma, también tienen bordes nítidos, pero más
irregulares o multilobulados. El linfangioma y el hemangiopericitoma
maligno, están mal delimitados, son difusos, no están encapsulados y
pueden infiltrar estructuras adyacentes. Las varices tienen límites nítidos
y su forma puede ser lobulada o serpiginosa.
El diagnóstico
diferencial de los tumores vasculares, por sus características, siempre
hay que hacerlo con lesiones muy vascularizadas, que también capten
mucho contraste. Las bien delimitadas como el hemangioma cavernoso, hay
que diferenciarlas de los meningiomas y schwanomas. Las peor
delimitadas, como el hemangiopericitoma, linfangioma o hemangioma
capilar, se pueden parecer a entidades menos frecuentes como
angioleiomiomas, hemangioendoteliomas malignos (angiosarcomas) y mención
especial merece el pseudotumor que puede ser muy parecido en infiltración,
mala delimitación, erosión ósea, etc., pero en este, generalmente, la
captación de contrate no es tan intensa. (6,19).
En RM el hemangioma
capilar y el hemangiopericitoma, son muy similares: ambos son tumores
muy vascularizados con abundantes vasos en su interior, que se mostrarán
hipointensos en T1 y T2 por el vacío de señal debido al flujo sanguíneo
en su interior. La masa del hemangioma capilar es hiperintensa en T1 y
T2 con respecto a la sustancia gris cerebral y el hemangiopericitoma,
suele ser isointenso en T1 y T2, aunque en ocasiones, también puede
mostrarse hiperintenso en ambas secuencias (19,23).
El linfangioma tiene señal
similar al hemangioma capilar con hiperseñal en T1 y T2, pero tiene
cavidades quísticas en su interior y hemorragias en diferentes estadíos
de evolución que lo hace bastante característico ya que la señal es más
heterogénea aunque el predominio sea hiperintenso.
El hemangioma cavernoso
es iso o hipointenso en T1 e hiperintenso en T2, ésto es bastante
inespecífico pero si introducimos contraste intravenoso y realizamos
adquisiciones precoces, la captación será heterogénea con más
intensidad en la periferia del tumor y en las adquisiciones tardías, la
captación se vuelve homogénea e intensa (23).
En las varices orbitarias
la señal es muy variable, dependiendo de si la varíz está permeable
en su interior (la señal será hipo en T1 y T2), si está trombosada
(hiperintensidad en T1 y T2) o si está parcialmente trombosada (se
mezclarán ambas señales).
La RM tiene la ventaja en
el diagnóstico de los procesos vasculares (fístula carótido
cavernosa, malformación arteriovenosa o varices) de que, además de
mostrar los vasos anormales intraorbitarios, nos permite ver el
contenido intracraneal y poder descartar si la lesión orbitaria es
primaria o secundaria, o si (como puede ocurrir en las anomalías
venoso-linfáticas), coexisten simultáneamente la lesión orbitaria y
la intracraneal (23,24).
Traumatismo orbitario
La radiología es de gran
ayuda en la valoración de los traumatismos orbitarios, aunque hasta
hace poco su diagnóstico se basaba principalmente en la radiología
simple, con lo cual se obtenía abundante información sólo sobre las líneas
de fractura, pero ahora con la introducción de la US, tomografía
computada y de la resonancia magnética, se ha mejorado mucho en la
valoración de las partes blandas.
Sigue habiendo muchos
centros en los que se sigue considerando la placa simple como la primera
exploración radiológica, si esta resulta normal y la clínica no es
sugestiva de fractura, no se realiza ninguna prueba radiológica más
(25).
Si la placa simple es
patológica o dudosa, se debe recurrir siempre a hacer una TC que ha
revolucionado el diagnóstico de estos traumatismos porque delimita bien
las lesiones óseas pero, además, permite ver las partes blandas
orbitarias y su relación con los senos paranasales, especialmente útil
en las fracturas de la pared medial (figura 1). Con la nueva generación
de TC helicoidal se pueden hacer adquisiciones de cortes muy finos en
tiempos muy cortos que permite hacer reconstrucciones sagitales,
coronales y 3D sin necesidad de movilizar al paciente (figura 1). En
nuestra experiencia la calidad de las reconstrucciones, a pesar de ser
aceptable no se puede comparar con las adquisiciones directas y sólo
sirven para descartar lineas de fractura evidentes o luxaciones pero no
tienen nitidez para valoración fina de lesiones pequeñas, por lo tanto
siempre que las condiciones del enfermo lo permitan, haremos
adquisiciones directas (figura 13) y en caso contrario recurriremos a
las reconstrucciones. Con la TC se ve el contenido orbitario herniado en
el seno maxilar (grasa o músculo) y esto nos permite anticiparnos a las
complicaciones como enoftalmos o diplopía. Con la TC se pueden valorar
simultáneamente las lesiones asociadas intracraneales o faciales (26).

Figuras 13a y b. Doble fractura orbitaria. Cortes coronales
secuenciales mediante TC. Doble línea de fractura de la pared lateral (a) y del
suelo (b), con esquirlas óseas que afectan a los músculos del cono.
Resulta imprescindible en
la valoración del canal óptico cuando haya neuropatía traumática
para valorar el tratamiento a seguir (27-29).
La TC resulta muy útil
en la evolución del traumatismo y en el seguimiento posquirúrgico de
la reparación de la fractura, bien sea la fijación con Teflón o metálica.
(19). Hay que valorar con mucho cuidado los estudios radiológicos en
especial la TC para poder evitar con el tratamiento adecuado, las
secuelas postraumáticas (30).
La principal indicación
para realizar RM, son las fracturas del techo orbitario, con ella se
pueden realizar adquisiciones multiplanares directas sin necesidad de
recurrir a las reconstrucciones. Con TC se valora muy bien el hueso,
pero no se puede distinguir un hematoma orbitario de una herniación
cerebral intraorbitaria, con la RM estas dos patologías se diferencian
sin dificultad (25).
Aunque la RM parecería
el procedimiento más indicado, la exploración de elección ante un
traumatismo orbitario es la TC, porque la RM esta contraindicada siempre
que haya duda de la existencia de un cuerpo extraño metálico. El
cuerpo extraño ferromagnético se movería al ser introducido en el
campo magnético y aumentaría el daño ocular u orbitario. La TC como
hemos dicho delimita mejor que la RM, las lesiones óseas y da muy buena
delimitación de las partes blandas (29).
Cuando se sospecha la
existencia de cuerpo extraño metálico hay autores (22) que sugieren la
US como primera exploración, aunque debido a las condiciones del
paciente, no siempre resulta fácil la realización de esta prueba. Se
dice que la radiología en manos expertas, detecta los cuerpos extraños
intraoculares en el 95% de los casos y en el 70% cuando están fuera del
globo ocular (22). La TC, con cortes finos y contiguos, puede detectar
cuerpos extraños metálicos desde 0,06 mm, cuando el material del que
están formados es madera o plástico, este poder de detección es
menor, y por lo tanto en estos casos sería conveniente recurrir a la
ecografia.
Por lo tanto la exploración
indicada ante un traumatismo orbitario, sería la TC, después de la
radiología simple. La RM quedaría como segunda exploración para casos
dudosos, sobre todo en fracturas del techo de la órbita. La ecografia
se debe hacer ante la sospecha de lesión ocular, sobre todo si puede
haber cuerpos extraños intraoculares no metálicos difíciles de
detectar con las otras técnicas.
NUEVAS APLICACIONES DE LA
NEURORRADIOLOGÍA DE LA CIRUGÍA ORBITARIA
Los importantes avances
ya mencionados en las técnicas de imagen no sólo han mejorado la
sensibilidad y especificidad diagnóstica en este campo sino que, además,
están permitiendo nuevas aplicaciones en la planificación previa a la
cirugía e incluso en el mismo acto quirúrgico, que comentaremos
brevemente en este apartado.
A. Técnicas de imagen
aplicadas a la planificación quirúrgica
Reconstrucciones de
imagen
El sofisticado desarrollo
de computadores conectados a los diferentes métodos de imagen (TC, RM,
US), las llamadas estaciones de trabajo, han permitido procesar y
reconvertir las imágenes obtenidas mediante una o varias de estas técnicas
y así conseguir otras tri o bidimensionales de las estructuras a
estudio. Además, permiten trabajar en esa imagen simulando la cirugía
planificada, decidiendo el procedimiento más seguro y sobre todo,
comprobar el resultado de esa intervención viendo las imágenes
obtenidas tras la simulación quirúrgica (31).
Las posibilidades y tipos
de reconstrucción a realizar por estas estaciones de trabajo son múltiples:
Reconstrucciones planares:
reconstruyen bidimensionalmente superficies planas o curvas que sigan
estructuras de interés (figura 1b).
Reconstrucciones 3D:
reconstrucciones en los tres planos del espacio obteniendo imágenes
tridimensionales (figuras 1c, 1d, 1e y 1f). Estos pueden ser:
• De superficie:
reconstruyen una imagen tridimensional de un tejido específico, es
decir, eligiendo una única densidad, como por ejemplo el hueso. Nos
permitirá ver la superficie del cráneo pero no su interior.
• De la superficie y
por transparencia, de algún elemento interior, eligiendo dos
densidades.
• Reconstrucciones
tridimensionales de una estructura determinada, sea cual sea su
localización, y de una densidad que en general es la máxima, como en
el caso del contraste intravenoso. Así se obtienen las reconstrucciones
de estructuras vasculares.
La técnica de imagen
utilizada para realizar estos procesos es variable. En el caso de la órbita,
la elegida suele ser la TC debido a su mejor resolución para evaluación
de estructuras óseas así como su mayor capacidad para detectar
posibles fragmentos, calcificaciones o cuerpos extraños. Aunque la RM
puede tener superior resolución en partes blandas, la falta de
referencias óseas la hace menos útil en esta área.
Se está trabajando en la
fusión de imágenes de distintas técnicas lo cual resultaría ideal
para obtener la máxima resolución de cada tejido, sí bien en regiones
como la órbita todavía no esta muy perfeccionado. La experiencia con
estaciones de trabajo ha demostrado numerosas ventajas, entre las que
destacan (31-33): mejor comprensión de la extensión de las patologías,
en especial de estructuras complejas en las que la extrapolación de
planos axiales es más complicada; mediciones de distancias, ángulos y
volúmenes; ensayos quirúrgicos teóricos; más exactitud en la
construcción de la prótesis; planificaciones quirúrgicas en las que
participan varias especialidades, para realizar una intervención más
integrada y con mejor coordinación entre los distintos equipos quirúrgicos.
Estas ventajas tienen
especial aplicación en el campo de la cirugía orbitaria infantil,
donde las reparaciones quirúrgicas óseas pueden impedir complicaciones
a largo plazo como el enoftalmos. Estudios realizados también mediante
mediciones volumétricas en caso de enoftalmos han demostrado que el único
elemento orbitario cuya proporción varia en estas órbitas respecto a
las normales es el hueso, cuyo volumen aumenta, mientras que la grasa, músculo
y globo ocular mantienen su volumen normal. Esto implicaría que
resecciones adecuadas en cantidad y localización de parte del hueso
orbitario permitirían la anteriorización del globo y la desaparición
del enoftalmos. Tanto en este tipo de cirugía orbitaria como en las
displasias y disóstosis óseas, las planificaciones mediante TC pueden
ser de gran utilidad (34).
Programas de simulación
quirúrgica: técnica de imagen en espejo.
Esta es una de las aplicaciones más prometedoras de la manipulación de
imagen, especialmente útil en cirugías que implican reconstrucciones
faciales importantes. Mediante esta técnica se logra una imagen virtual
del resultado ideal de la intervención, y, a partir de la misma,
realizar las resecciones adecuadas y los moldes con las medidas precisas
para las prótesis que deban colocarse. El procedimiento se llama
producción de imagen en espejo (35). Requiere de los siguientes pasos:
una adquisición de imágenes siguiendo un método riguroso de colocación
del paciente (ninguna rotación de la cabeza, ni sobre eje axial ni
vertical, no angulación del gantry, adquisición volumétrica...); una
revisión exhaustiva de las imágenes para evaluar exactamente la línea
media de cada una de ellas, cosa no siempre sencilla por las
deformidades naturales del paciente; mediante técnicas de sustracción
digital se logra eliminar la parte a intervenir y sustituirla por la
imagen en espejo (o algo modificada según las necesidades) del lado
contralateral sano.
Se pueden, a partir de
estas imágenes, reconstruir modelos que permiten luego conseguir moldes
para utilizarse en la cirugía.
Esta técnica, sin
embargo, no está todavía introducida de forma habitual en la práctica
diaria debido, no sólo a su coste (software especifico, etc.), sino a
las dificultades técnicas que a veces implica la realización de la
prueba (la colocación exacta del paciente es difícil en muchas
ocasiones) y la laboriosidad del postproceso de la imagen, con el
consiguiente gasto de tiempo médico. Todo el procedimiento debe, además,
garantizar un grado de resolución máxima para que el error sea prácticamente
inexistente en las mediciones y las prótesis encajen correctamente.
Mediciones tumorales para
diseño de placas radioactivas de actuación local. Otra
de las grandes utilidades del postproceso de imagen es la capacidad de
medir distancias a veces desde cualquier ángulo y proyección que nos
permiten elegir las placas radioactivas del tamaño más adecuado y
colocarlos en la posición idónea.
En este sentido, la
realización de secuencias de RM potenciadas en T1 con gadolinio y
matrices de alta resolución resulta muy útil, en nuestra experiencia,
para evaluar el resto activo de los retinoblastomas, diferenciándolo
del componente cálcico y medir exactamente su localización y tamaño
(figura 14).

Figuras 14a y b. Resto tumoral activo de retinoblastoma que se
diferencia en secuencia T1 con gadolínio del componente óseo, para realizar
mediciones previa a la colocación de la placa radioactiva.
Control del intervalo
quirúrgico en los casos de tratamientos quirúrgicos en varios tiempos:
implantes porosos. Las
técnicas de imagen pueden ser muy útiles a la hora de decidir el
momento de las distintas fases en tratamientos con varias cirugías. Es
el caso de la colocación de prótesis oculares porosas de
hidroxiapatita (HA) o MEDPOR, La RM permite un control de la
revascularización que se produce en la prótesis y que es necesaria
para una correcta implantación del vástago en el que se anclará la prótesis
externa.
La sección de Oftalmología
infantil y la sección de Neurorradiología del Hospital Universitario
La Paz, hemos realizado un estudio prospectivo mediante RM para valorar
la existencia o no de revascularización en función del grado de
captación de Gd en 39 niños (20 niñas y 19 niños) sometidos a
enucleación o evisceración uni o bilateralmente y de edades
comprendidas entre los 3 meses y los 2 años por diferentes patolo gías
de base, colocando en 10 casos prótesis de MEDPOR y en 29 niños prótesis
de hidroxiapatita (en un caso de forma bilateral). Se realizaron
secuencias potenciadas en T1, con saturación grasa y reconstrucciones
axiales y sagitales de 3 mm con matriz de alta resolución antes y después
de la administración de gadolinio. La RM nos permitió evaluar
diferentes parámetros como el grado de captación (sinónimo de
revascularización del implante), la forma de captación (homogénea o
heterogénea), el lugar de comienzo (anterior o posterior), la
existencia o no de captación extraprótesis como índice de infección
periprótesis y la presencia o no de líneas que sugieran fisuras o
alteraciones intrínsecas de la prótesis. Estos parámetros fueron
comparados con la evolución y el estado de la prótesis en el acto quirúrgico
de la colocación del vástago, evaluando el grado de correlación entre
los hallazgos en la RM y los datos clínicos y quirúrgicos (figura 15).

Figuras 15a, b, c y d. Secuencias T1 con gadolínio intravenoso y
saturación grasa de prótesis porosas. Captación completa de la prótesis en
(a). Falta la vascularización anterior en la prótesis (b, c). Línea de
fractura de la prótesis (d).
Los resultados de nuestro
estudio muestran una forma de vascularización bastante constante,
empezando por el polo posterior, con un patrón homogéneo, y quedando
la parte anterior como última zona para vascularizar. Esto podría
explicar la aparición de exposiciones anteriores y malas implantaciones
de vástagos en los casos de prótesis sin buena vascularización
anterior. Por ello, es especialmente importante que sea prácticamente
completa antes de la colocación del vástago, o, por lo menos, la de la
región anterior. Respecto al tiempo de esta revascularización,
nuestros resultados coinciden con los referidos en la literatura, siendo
necesario casi un año en el caso de las prótesis HA para lograr un
75-80 por ciento y un tiempo algo menor para las prótesis MEDPOR. Son
llamativas las diferencias en la sensibilidad de la RM para las prótesis
de MEDPOR y las de HA, significativamente menor en la primera. Hay que
tener en cuenta, sin embargo, varios hechos a la hora de evaluar estos
resultados como el escaso número de prótesis de MEDPOR estudiadas con
RM por el momento (solo diez) y el hecho de que en todos los casos en
los que ha existido una mala correlación clínico-radiológica el
recubrimiento era de esclera. Quizá este tipo de recubrimiento
dificulta la valoración de la captación. También puede ser que el
MEDPOR pueda dar lugar a más variabilidad en la forma de captación. De
hecho, el patrón y la forma de evolución de la captación son menos
constantes en el MEDPOR que en la HA.
En conclusión, y de
acuerdo con otros trabajos, la RM es un método útil y de alta
fiabilidad en el control de las prótesis sobre todo de HA. Asimismo, la
RM es especialmente útil para la detección de complicaciones en ambos
tipos de prótesis (36-39).
B. Aplicación de técnicas
de imagen como guía para procedimientos quirurgicos
A. En cirugías complejas
Si bien las técnicas de
imagen han logrado una gran precisión en el diagnóstico y la
planificación quirúrgica de las lesiones craneofaciales, todavía la
correlación entre esa imagen conseguida o planificada y la situación
real de la lesión en el campo quirúrgico seguía siendo un proceso
mental que el cirujano debía de realizar. También se ha intentado
facilitar y agilizar este proceso. Para ello se ha desarrollado una
estación de trabajo, aunque de características y funcionamiento algo
diferente a los nombrados previamente, que permite la visualización
directa y en tiempo real de la región que se está interviniendo
mediante imágenes, ya sea de TC, RM o US.
Esta estación de trabajo
tiene las mismas posibilidades de reconstrucción que las otras, pero su
ubicación es en el quirófano donde, por un complicado sistema de
reconocimiento de coordenadas, son capaces de correlacionar las imágenes
realizadas previamente de la región a intervenir, con la situación
exacta de esa región en la mesa del quirófano. De esta forma, mediante
un puntero que el cirujano puede usar directamente, o bien conectar a
los distintos instrumentos quirúrgicos, él sabe su situación exacta
en cada momento en las imágenes del computador, y ve más claramente en
el lecho quirúrgico las estructuras cercanas, la distancia a la lesión
y si la resección es más o menos completa. Las primeras estaciones de
este tipo se han utilizado sobre todo en neurocirugía con el nombre de
navegadores.
Dentro del campo de la
cirugía orbitaria también se está empezando a utilizar esta tecnología.
En este sentido, es destacable la experiencia llevada a cabo en la
Universidad de Aachen por un equipo multidisciplinario con la técnica
CASS (Computed assisted Surgery). En su experiencia, de 21 casos, se ha
conseguido acortar significativamente el tiempo quirúrgico, teniendo en
todo momento la situación exacta del cirujano en la órbita marcada en
las imágenes y, por tanto, una más clara visión de conjunto, de los
posibles obstáculos al objetivo de la cirugía (40-42). En otros
centros se han llevado a cabo experiencias similares (43).
Las indicaciones
fundamentales según su experiencia para esta técnica serían las
siguientes:
• Tumores retrobulbares
profundos de pequeño tamaño.
• Biopsias en especial
por vía intranasal.
• Descompresiones del
nervio óptico.
• Extracción de
cuerpos extraños o fragmentos óseos.
• Sangrados severos que
impiden ver el campo quirúrgico.
En todos estos casos la técnica
utilizada para las imágenes basales es la TC, ya que es la que mejor
visualiza el hueso, como ya hemos comentado, y este es un punto de
referencia fundamental en la cirugía orbitaria.
No obstante lo
prometedoras que parecen ser estas experiencias, nunca debe olvidarse
que son una mera ayuda para el cirujano y que nunca deben sustituir su
visión espacial y su orientación en el campo quirúrgico, tanto más
cuando la casuística todavía es pequeña con esta técnica, en
especial en el campo de la órbita, y que debemos esperar series mas
largas para mejor evaluación de los posibles errores y problemas que
conlleve (movilización de estructuras al exponerlas en el campo quirúrgico
que aumentan el posible margen de error en la correlación de
coordenadas, etc...).
En cuanto a la realización
del estudio basal de imágenes, éste ha de tener unas características
técnicas muy concretas para ser compatibles con cada estación de
trabajo concreta. En general en estos estudios debe:
• realizarse cortes
continuos sin distancia entre ellos
• cortes de 1 mm
preferentemente y nunca mas de 3 mm
• pixel cuadrados de
512x512
• FOV circular o
cuadrado y fijo a lo largo de todo el estudio
• Proyección axial.
Estas condiciones
aconsejan el uso de tomógrafos helicoidales para la realización de
estos estudios, ya que:
• consiguen mejor
calidad de reconstrucción
• se utiliza menor
dosis de radiación
• el estudio es más rápido
por lo que en especial en el caso de los niños puede ahorrar el uso de
sedación.
B. En procedimientos mínimamente
invasivos
Finalmente, no podemos
dejar de hacer mención en este apartado de la utilidad de las técnicas
de imagen como guía y control de procedimientos mínimamente invasivos,
como toma de biopsias, o hinchado de prótesis retrobulbares para
corregir o evitar enoftalmos. En estos casos la TC suele ser la técnica
de elección por su mayor resolución, aunque en muchos casos, la US
puede ser suficiente y resulta más barata, accesible e inocua que la TC
(figura 16).
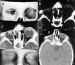
Figuras 16a, b, c, d, e y f. Prótesis de silicona intraorbitaria
que se ha ido expandiendo progresivamente (a, b, c) con control de TC en tres
tiempos. En las reconstrucciones de superficie óseas (d) y de piel (e) se
observa la asimetría orbitaria que trata de corregirse.
BIBLIOGRAFÍA
- Kaufman LM, Mafee MF,
Song CD. Retinoblastoma and simulating lesions. Role of CT, MR imagin
and use of Gd-DTPA Contrast Enhancement. Radiologic clinics of North
America. NOV. 1998, 36, 6: 1101-1116.
- Capeans C. Actualización
en tumores intraoculares. Tecnimedia. 1999, pág 179-186.
- Kingston JE,
Hungerford JL, Madreperla SA, Plowman PN. Results of Combined
Chemoterapy and Radiotherapy for Advenced Intraocular Retinoblastoma.
Arc Ophthalmol 1996; 114: 1339-43.
- Pelak VS, Volpe NJ,
Liu GT, Galetta SL. Neuroradiology in ophtalmology. Ophthalmology
clinics of North America. 1998; 11 (3): 339-347.
- Hansberger HR.
Handbook of head and neck imaging. Second edition. Mosby, 1995; 301-338.
- Som Peter M, Curtin
Hugh D. Head and Neck Imaging. Third Edition. MOSBY. 1996, pág.
1009-1183.
- Bagley LJ, Hurst RW,
Zimmerman RA, Shields CL, De Potter P. Imaging in the trilateral
retinoblastoma syndrome. Neuroradiology 1996; 38: 166-170.
- Buerger D, Biesman B.
Orbital imaging. Ophthalmology clinics of North America 1998; vol 11,
num 3: 381-410.
- Kodsi S, Shetlar D,
Campbell J, Garrity J, Bartley G. A review of 340 orbital tumors in
children during a 60-year period. Am Journal oh Ophthalmology 1994; 117:
177-182.
- Scott W. Atlas:
Magnetic Resonance Imaging of tha Brain and Spine. Second edition.
Lippincot-Raven, 1996; 1007-1092.
- Shields JA, Bakewell
B, Augsburger JJ et al. Space occupying orbital masses in children. A
review of 250 consecutives biopsies. Ophthalmology 1986; 93: 379-384.
- Sohaib SA, Moseley y,
Wrigth JE. Orbital Rhabdomyosarcoma-the radiological characteristics.
Clinical Radiology 1998; 53, 357-362.
- Lee JH, Lee MS, Lee
BH, et al. Rhabdomyosarcoma of the head and neck in adults: MR and CT
findings. AJNR Am J Neuroradiol 1996; 17: 1923-1928.
- Mafee M, Pai E,
Philip B. Rhabdomyosarcoma of the orbit. Radiologic clinics of North
America 1998; 36.6: 1215-1227.
- Yousem DM, Lexa JL,
Bilaniuk LT, et al. Rhabdomyosarcomas in the head and neck: MR imaging
evaluation. Radiology 1990; 177: 683-686.
- Belmekki BM, El
Bakkali M, Abdellah H. Epidemiologie des processus orbitaires chez l’
enfant. A propos de 54 cas. J. Fr.Ophtalmol. 1999; 22 (3), 394-398.
- Cotton J B,
Ligeon-Ligeonnet P, Ranchin B. Exophtalmie de l’ enfant par
neoformation vasculaire orbitaire. Arch Pediatr. 1994; 1: 1111-1114.
- Tan WS, Wilbur AC,
Mafee MF. The role of neuroradiologist in vascular disorders involving
the orbit Radiologic Clinics of North America. 1987; 25 (4) 849-861.
- Newton TH, Bilaniuk
LT. Radiology of the eye and orbit 1ª ed. Raven Press. 1990; cap 5, 6,
7, 1-84, 1-20, 1-26.
- Edmar A, Boumahni B,
Piyaralys. Hemangiome capillaire orbitaire profond chez un nourrisson.
Lettre à la redaction. Arch Pediatr 1997; 4, 896-904.
- Wright JE, Sullivan
TJ, Garnen A. Orbital venous anomalies. Ophthalmology 1997; 104 (6),
905-913.
- Berges O, Torrent M.
Echographie de l’ oeil et de l’orbite. 1ª ed. Vigot. 1986 cap. 6
pag. 101-31, cap. 7 pag. 133-139.
- Bilaniuk LT. Orbital
vascular lesions. Role of imaging. Radiologic Clinics of North America.
1999, 37 (1), 169-183.
- Katz SE, Rootman J,
Vangueeravong S. Combined venous lymphatic malformations of the orbit
(so-called lymphangiomas). Ophtalmology 1998; 105 (1), 176-184.
- Koh JY, Della Rocca
RC, Maher EA. Orbital fractures. Diagnosis and management. In Albert,
ed. Ophtalmic Surgery: Principles and techniques, Vol. Two, London,
Blackwell Science Inc., 1995; 90: 1459-1507.
- Mixter RC, Carson LV,
Hardy S. Orbital aspects of craniofacial surgery. In Albert, ed.
Ophtalmic Surgery: Principles and techniques, Vol. Two, London,
Blackwell Science Inc.,1999; 94: 1537-1552.
- Levin LA, Beck RW,
Joseph MP. The treatment of traumatic optic neuropathy ophthalmology.
1999; 106: 1268-1277.
- Harris GJ, Garcia GJ,
Logan SC. Orbital Blow-out fractures: correlation of preoperative
computed tomography and postoperative ocular motility. Trans Am
Ophthalmol. 1998; 96: 329-347.
- Seiff SR, Carter SR.
Optic canal decompression. In Albert, ed. Ophtalmic Surgery: Principles
and techniques, Vol. Two, London, Blackwell Science Inc., 1995; 93:
1529-1536.
- Meyer CH, Groos N,
Sabatier H. Séquelles á long terme des fractures du plancher de
l’orbite opérées. Stomatol. Chir. Maxillofac. 1998; 99, (3) 149-154.
- Zonneveld FW,
Vaandrager TM, Van der Meulen JH. Three dimensional imaging in
congenital disorders involving the orbit. Rad Clinicals of North
America. 1998; 36: 1261-1277.
- Eppley BL, Sadove AM.
Computer- generated patient models for reconstruccion of cranial and
facial deformities. J Craniofac Surgery. 1998; Nov, 9(6): 548-56.
- Altobell DE, Kitinis
R, Mulliten JB. Computer- assisted three-dimensional planning in
craniofacial surgery. Plast Reconstr Surg. 1993; Sep 92(4): 576-85.
- Bite Uldis, Jackson
IT, Forbes GS et al. Orbital Volume Measurements in Enophthalmos using
three-dimensional CT Imaging. Plastic and reconstructive Surgery 1995;
75: 502-508.
- Fukuta F, Jackson IT,
Mc Ewan CM et al. Three- dimensional imaging in craniofacial surgery: a
review of the role mirror image production. Eur J Plast Surg. 1990; 13:
209-217.
- Karesh JW, Dresner
SC. «High-density porous polyethylene (MEDPOR) as a succesful
anophothalmic socket implant». Ophthalmology 1994; 101: 1688-95.
- Flanders AE, De
Potter P, Rao VM, Tom BM, Shields CL, Shields JA. MRI of orbital
hydroxyapatite implants. Neuroradiology 1996; 38: 273-277.
- Jamell GA, Hollsten
DA, Hawes MJ, Griffin DJ, Klingensmith WC, White WL, Spirnak J. Magnetic
resonance imaging versus bone scan for assessment of vascularization of
hydroxyapatite orbital implant. Ophthalm Plast Reconstr Surg 1996; 12:
127-130.
- Jordan DR, Ells A,
Brownstein S, Munro SM, Grahovac SZ, Raymond F, Gilberg SM, Allen LH.
Vicryl-mesh wrap for the implantation of hydroxyapatite orbital
implants: an animal model. Can J Ophthalmol 1995; 30: 241-246.
- Korves B, Klimek L,
Mosges R. Surgical decompression in endocrine orbitopathy a
three-dimensional locating device greater safety. ORL J Otorhinolaryngol
Relat Spec. 1996; 58(1): 46-50.
- Klimek L, Wenzel M,
Mosges R. Computed assisted orbital Surgery. Ophthalmic Surgery. 1993;
24(6): 411-416
- Klimek L, Mosges R,
Laborde G et al. Computed-assisted image-guided surgery in pediatric
skull-base procedures. J Pediatric Skull-base procedures. J Pediatr
Surg. 1995; 30(12): 1673-6.
- Sandeman DR, Gill SS.
The impact interactive image guided surgery: The Bristol experience with
the IgG/Elekta viewing wand. Acta Neurochir Suppl (wien) 1995; 64:
54-58.
|