|
La proximidad de las estructuras intracraneales con la órbita, unido a la
alta frecuencia de síntomas oculares en los pacientes neuroquirúrgicos, obliga
a los especialistas en neurocirugía a estar familiarizados con la anatomía (1)
y la patología orbitaria.
Hoy día, las patologías orbitarias de mayor interés neuroquirúrgico
pediátrico, están constituidas por: las lesiones ocupantes de espacio, ya
sean, originadas dentro de la orbita o en su vecindad, las lesiones traumáticas
cráneo-orbitarias, la patología malformativa y otras entidades que provocan un
deterioro de la función del nervio óptico en el contexto de hipertensión
endocraneal. El abordaje actual de estas lesiones requiere, muchas veces, una
colaboración estrecha de varias especialidades.
PATOLOGÍA OCUPANTE DE ESPACIO INTRAORBITARIA
Existen muchos tipos de tumores orbitarios, que pueden clasificarse según el
tipo celular, la edad de presentación y el comportamiento biológico benigno o
maligno (2). La frecuencia de este tipo de lesiones varía según sea el origen
de las series estudiadas (neuroquirúrgicas u oftalmológicas) y también según
el tipo de estudio realizado (histológico, radiológico, etc.).
MANIFESTACIONES CLÍNICAS
La sintomatología oftalmológica de los tumores orbitarios, evoluciona en
general de forma insidiosa o subaguda, excepto en casos de tumores de alta
malignidad (metastásicos), y tumores que se extienden desde los senos
paranasales y de otras estructuras paraorbitarias especialmente del cono
posterior y techo de la orbita (3).
La manifestación clínica clásica es la proptosis, producida por un
desplazamiento axial o anterior del globo ocular. Los pacientes la refieren como
prominencia de uno de sus globos oculares o como ampliación de la hendidura
palpebral. Otra manifestación frecuente es la quemosis, que indica un
importante aumento de la presión en las venas de la órbita, producida bien por
una obstrucción venosa o por una comunicación arterio-venosa orbitaria.
La alteración de la agudeza visual que suele acompañar a estos
procesos, puede estar producida por una compresión directa sobre el nervio
óptico o por una impronta sobre el globo ocular. Una forma peculiar de esta
alteración es la pérdida de visión monocular transitoria en relación con los
movimientos del globo ocular («gaze-evoked amaurosis») debida a la
compresión directa sobre el nervio óptico o la arteria central de la retina,
que desaparece al volver el globo ocular a su posición central. La pérdida
aguda de visión puede ser debida también a la presión provocada por un
hematoma intratumoral.
Con relativa frecuencia los pacientes refieren la aparición de visión
doble, bien de naturaleza mecánica (la masa interfiere la movilidad de uno
de los globos oculares) o por alteración de los pares craneales (III, IV o VI)
ya sea en la órbita o en el seno cavernoso.
DIAGNÓSTICO
La evaluación de los pacientes con tumores orbitarios requiere una
exploración oftálmica completa, que incluya un examen ocular externo y de la
órbita, una valoración campimétrica y de agudeza visual, y una valoración de
la musculatura ocular extrínseca e intrínseca.
Así mismo debe realizarse los estudios de imagen necesarios, los cuales
deben incluir ultrasonografía, Tomografía Computarizada (TC) y Resonancia
Magnética (RNM).
PATOLOGÍA OCUPANTE DE ESPACIO MÁS FRECUENTE
Glioma del nervio óptico
Este tipo de tumor tiene su origen en el nervio óptico (figura 1), quiasma o
radiaciones ópticas anteriores. La mayoría produce síntomas en la 1ª década
de la vida con pérdida progresiva de agudeza visual y proptosis (2). Presenta
una incidencia aumentada en los pacientes con Neurofibromatosis.
Histológicamente la mayoría son tumores de bajo grado con un patrón
histológico variable que oscila entre un patrón predominantemente fibrilar a
uno microquístico. Existe además una proliferación reactiva meníngea, que
contribuye al aumento de su tamaño.

Figura 1. Imagen axial de RM de un glioma del nervio óptico derecho
La evolución clínica puede seguir dos cursos diferentes: 1) evolución
indolente, con poca progresión sintomatológica (frecuente en pacientes con
Neurofibromatosis); y 2) crecimiento rápido del tumor, con ceguera, proptosis y
extensión intracraneal (poco frecuente en pacientes con Neurofibromatosis).
Alrededor de un 50% de los pacientes presentan un curso progresivo y precisan
por tanto un seguimiento estrecho, tanto desde el punto de vista clínico, como
radiológico (TC y RNM).
Si existe progresión de la sintomatología, se recomienda la intervención
quirúrgica, mediante un abordaje transcraneal (no lateral). Si existe
extensión intracraneal, sobre todo con afectación del quiasma óptico, se
recomienda la realización de una biopsia con aguja fina. El tratamiento con
radioterapia es controversial ya que son, en la mayoría, tumores de bajo grado
de malignidad histológica. Los gliomas malignos de la vía óptica se
desarrollan habitualmente en adultos y son uniformemente letales a pesar de
cualquier tipo de tratamiento.
Meningioma del nervio óptico
Se originan de las células meningoteliales, que ocupan la superficie interna
de la duramadre y que pueden encontrarse también en la aracnoides y la piamadre
(4). El primer síntoma es normalmente la pérdida de visión; posteriormente
puede aparecer proptosis, alteración de los movimientos oculares, papiledema o
atrofia óptica con un defecto pupilar aferente.
El curso clínico depende de las vías de desarrollo del tumor: 1)
crecimiento centrífugo: efecto de masa exofítico y proptosis anteriores a la
afectación visual; 2) tumor confinado al espacio subdural: la pérdida de
agudeza visual puede ser el único síntoma, apareciendo posteriormente
papiledema y atrofia óptica secundaria; y 3) tipo intradural-extradural:
componente exofítico y proptosis, coincidiendo con disminución de la agudeza
visual.
El diagnóstico radiológico (TC y RNM) permite además predecir el
comportamiento y localización anatómica de la lesión.
El tratamiento de este tipo de lesiones depende de la localización de las
mismas y del grado de afectación visual. Si está localizado en los segmentos
medio o anterior y se acompaña de una agudeza visual estable, se recomienda
seguimiento clínico y radiológico; si desarrolla pérdida de agudeza visual
progresiva, se recomienda abordaje microquirúrgico lateral. Si el tumor está
localizado en el ápex orbitario y la visión es normal se recomienda
seguimiento. Si existe pérdida de agudeza visual se recomienda craneotomía y
abordaje transcraneal o radioterapia. Si el tumor está localizado en el ápex
con extensión intracraneal y pérdida de visión progresiva, se recomienda un
abordaje transcraneal con resección de la porción intracraneal, incluyendo el
nervio óptico y la porción intraorbitaria.
Neurofibroma
Pueden ser formas solitarias y difusas o multicéntricas. El Neurofibroma
solitario aparece en personas de mayor edad y se caracteriza por una proptosis
indolora, lentamente progresiva. La pérdida de visión es normalmente mínima.
El tumor suele localizarse en la parte posterior y superior de la órbita,
produciendo una paresia de la mirada vertical.
El tipo difuso o multicéntrico representa un problema congénito con
afectación multisistémica, sobre todo en niños y adolescentes. El síntoma
inicial suele ser una proptosis progresiva desfigurante (figura 2). Es preciso
una exéresis completa del globo para la resección tumoral. La recurrencia es
la regla.
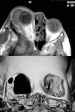
Figura 2. La imagen superior de RM, muestra en la parte externa de
la orbita derecha, una lesión neurofibromatosa. En la imagen inferior de la TC
en 3D se observa el defecto óseo de la pared orbitaria postero-externa en el
mismo paciente.
Quistes dermoides y epidermoides
Son los quistes de desarrollo más frecuentes de la órbita. De origen dermal
se encuentran normalmente en niños y constituyen un 4-6% de los tumores
orbitarios. Son los tumores orbitarios más frecuentes de la infancia, pero
pueden encontrarse en personas mayores de 50 años.
Los quistes epidermoides o colesteatomas afectan al grupo de mayor edad,
localizados profundos en la órbita y con crecimiento en el diploe óseo.
Tienden a localizarse en la porción superior de la órbita y pueden protruir a
través del arco supraciliar. Normalmente el quiste es indoloro, no adherido a
la piel y produce un desplazamiento escaso del globo ocular. En ocasiones puede
progresar intracranealmente o hacia el seno adyacente. El defecto óseo es
radiolucente con márgenes escleróticos o bien delimitados.
El abordaje quirúrgico depende de la localización. Los tumores localizados
en el ápex, cerca del agujero óptico o de la fisura orbitaria superior o los
que se extiendan intracranealmente, requieren un abordaje transcraneal. Sin
embargo, la mayoría de estas lesiones pueden abordarse a través de una
orbitotomía lateral. Independientemente del tipo de abordaje, es muy difícil,
poder extirpar el quiste intacto, siendo por lo tanto relativamente frecuente,
su recurrencia.
Metástasis
Las más frecuentes de la infancia son el neuroblastoma y el sarcoma de
Ewing. La mayoría de los neuroblastomas son retroperitoneales y aparecen antes
de los 7 años de edad. Se presentan típicamente con exoftalmos brusco y
quemosis, que puede ser bilateral. Existe destrucción ósea, sobre todo de la
pared lateral.
Displasia fibrosa
Es una lesión ósea no neoplásica de la infancia y adolescencia. Cuando
afecta a la órbita lo suele hacer también al maxilar, arco zigomático,
etmoides, frontal o esfenoides. Dependiendo del hueso afectado puede haber
pérdida de visión (esfenoides) o proptosis ligera y distensión orbitaria
(maxilar). En general el crecimiento es indoloro (figura 3). Radiológicamente
se caracteriza por la aparición de pequeñas zonas translúcidas en los huesos
craneales o amplias áreas de esclerosis difusa.
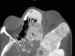
Figura 3. Imagen de TC , en proyección axial, que muestra la
compresión de los elementos del ápex orbitario en un paciente con displasia
fibrosa.
El tratamiento está condicionado por la severidad de la lesión, reflejado
en la pérdida de agudeza visual, debiendo realizarse una descompresión del
nervio óptico mediante un abordaje transcraneal (5,6). No se recomienda la
radioterapia, ya que puede inducir una transformación sarcomatosa.
ABORDAJES QUIRÚRGICOS A LA ÓRBITA
La primera cirugía para un tumor intracra neal que producía proptosis fue
realizada por Durante en 1889 (7) en Roma. Desde entonces se han desarrollado
numerosas técnicas para el abordaje quirúrgico a la órbita las cuales
requieren un conocimiento de la microanatomía orbitaria (1,8) de las técnicas
microquirúrgicas convencionales (2,9) y las guiadas con neuroimagen
(Navegación asistida con ordenador o con ultrasonidos).
La cirugía intraorbitaria presenta notables dificultades, debido
principalmente al pequeño tamaño de la órbita y a la forma geométrica de la
misma: pirámide rectangular irregular (figura 4).
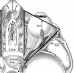
Figura 4. Dibujo de la pirámide orbitaria.
La órbita tiene 5 caras, que pueden utilizarse para alcanzar el contenido
intraorbitario: 1) orbitotomía anterior: a través de los párpados o
conjuntiva; 2) orbitotomía transetmoidal: ruta órbito-nasal; 3) orbitotomía
transmaxilar: a través de la pared orbitaria inferior; 4) orbitotomía lateral
o temporal: cara externa a través de la fosa temporal; y 5) orbitotomía
transfrontal: intracraneal.
La vía de acceso a utilizar depende de la localización de la patología y
de la experiencia del cirujano. En Neurocirugía se utilizan las orbitotomías
lateral y transfrontal.
Reglas generales
1) Tarsorrafía preventiva: evita el edema palpebral y conjuntival, la
quemosis y el hematoma subconjuntival. Se realiza preferentemente al principio o
al final de la cirugía y se mantiene 1-2 semanas. La técnica consiste en unir
los bordes de los párpados con 2-3 puntos en U.
2) Aislamiento pre-operatorio de los músculos oculares: sobre todo en
cirugía transfrontal. Se realiza mejor a través de una vía transconjuntival,
mediante ganchos.
3) Mantener la anatomía de la órbita (anillo) o reconstruirla al finalizar,
debido al gran componente estético de la órbita.
Orbitotomía lateral
Es el abordaje más antiguo, descrito por Krönlein en 1889 (10); desde
entonces se han descrito numerosas variaciones (2,11,12).
Es menos invasivo que el abordaje transcraneal y puede utilizarse no sólo
para la resección de tumores orbitarios, sino también para la descompresión
orbitaria en la orbitopatía tiroidea.
Técnica
Incisión cutánea en S, curvada hacia arriba hasta la región lateral de la
ceja y posteriormente a lo largo del arco zigomático hasta no más de 40 mm del
canto externo.
Exposición del periostio para liberar el hueso fronto-zigomático con
separación del músculo temporal, y separación de la periórbita de la pared
externa. Se realizan 2 incisiones horizontales con sierra oscilante posteriores
al reborde orbitario lateral. Se realiza la osteotomía superior por encima de
la sutura fronto-zigomática, y la osteotomía inferior a nivel del borde
superior del arco zigomático; posteriormente se fractura el hueso hacia fuera y
hacia atrás en la sutura esfeno-zigomática. Si se quiere exponer lesiones en
el interior del cono muscular se fresa parcialmente el esfenoides.
La orbitotomía puede ampliarse, si se precisa, hasta la fisura orbitaria
superior (FOS) con exposición de la duramadre temporal, teniendo mayor acceso a
la porción lateral profunda del cono muscular.
Abordajes intraorbitarios
1) Superior: entre el músculo recto superior y el músculo recto
lateral.
Las primeras estructuras que encontramos son la arteria y el nervio
lacrimales (ramas respectivamente de la arteria y el nervio oftálmicos).
Retrayendo hacia abajo el recto lateral se expone el compartimiento lateral del
cono muscular, pudiendo visualizarse la arteria ciliar postero-lateral y los
nervios ciliares cortos. La división superior del III par camina en la cara
inferior del músculo recto superior. La vena oftálmica superior pasa en el
interior del cono muscular, saliendo del mismo cerca del anillo de Zinn, y puede
ocasionalmente dificultar el acceso a la región cercana al ápex.
Se suele utilizar para lesiones situadas supero-laterales al nervio óptico o
cuando es necesario exponer el nervio óptico.
2) Inferior: entre el músculo recto lateral y el músculo recto
inferior.
Las estructuras neurales que podemos encontrar incluyen la división inferior
del III par, los nervios ciliares cortos y el ganglio ciliar. La división del
III par da 3 ramas para los músculos recto inferior, oblicuo inferior y recto
medial (pasa por debajo del nervio óptico). La rama para el músculo recto
inferior proporciona la rama parasimpática del ganglio ciliar. El ganglio
ciliar se encuentra lateral al nervio óptico. También puede exponerse la
arteria ciliar postero-lateral y la vena oftálmica inferior sobre el músculo
recto inferior; esta vena es de menor tamaño que la superior y no suele suponer
ninguna dificultad operatoria.
Se suele utilizar este acceso para lesiones localizadas infero-laterales al
nervio óptico. Se consigue peor exposición del nervio óptico, ya que
encontramos en nuestra trayectoria al ganglio ciliar y sus raíces; estas
estructuras están en general, confundidas con la grasa orbitaria y se lesionan
con bastante facilidad.
En ambos casos se realiza una apertura del anillo de Zinn entre el origen de
los músculos rectos superior y lateral.
Abordaje transcraneal
Se utiliza generalmente para tumores orbitarios con extensión intracraneal,
tumores localizados en ápex orbitario o canal óptico y tumores intracraneales
con extensión orbitaria.
Técnica
Se realiza una craneotomía fronto-orbitaria modificada con resección del
reborde supraorbitario junto con el colgajo frontal. La parte posterior de la
órbita se reseca con una pinza de Leksell.
Abordajes intraorbitarios
1) Medial: entre el espacio comprendido entre el músculo oblicuo
superior (que se retrae medialmente) y los músculos elevador del párpado y
recto superior (se retrae lateralmente). Se expone el nervio óptico desde el
globo hasta el canal óptico. En la parte lateral del nervio óptico encontramos
el IV par, la arteria oftálmica, el nervio nasocialiar y la vena oftálmica
superior, que cruzan por encima del nervio óptico hasta la región medial de la
órbita. El anillo de Zinn se abre entre los músculos rectos superior y medial,
permitiendo exponer la parte medial y superior del nervio óptico.
Se suele utilizar para lesiones localizadas supero-mediales al nervio óptico
o cuando se necesita exponer el nervio óptico desde el canal óptico hasta el
globo ocular. Se utiliza sobre todo en meningiomas y gliomas del nervio óptico.
2) Central: se retrae medialmente el músculo elevador del párpado y
lateralmente el recto superior. Existen 2 variantes, con retracción medial o
lateral del nervio frontal.
Se utiliza preferentemente para lesiones localizadas en la porción media del
segmento intraorbitario del nervio óptico o para realizar biopsias del nervio
óptico.
3) Lateral: se realiza entre el músculo recto lateral (se retrae
lateralmente) y los músculos recto superior y elevador del párpado (se retraen
medialmente). Existen 2 variantes, con retracción medial o lateral de la vena
oftálmica superior. Permite una buena exposición de la zona apical profunda
del nervio óptico. Dividiendo el anillo de Zinn entre los músculos recto
superior y recto lateral se puede exponer la unión de la zona apical con la
fisura orbitaria superior.
Se suele utilizar para lesiones que incluyen el área apical profunda, la
fisura orbitaria superior o el seno cavernoso.
Descompresión del canal óptico
La descompresión del canal óptico se realiza principalmente cuando el
nervio óptico está comprometido por un tumor o por fragmentos óseos (13,14).
Para ello se han utilizado varias técnicas. La vía a través de una
craneotomía frontal es la más antigua y permite una visión directa del nervio
óptico, una vez extirpado el techo. La vía esfenoetmoidal, variante lateral de
la ruta clásica transesfenoidal a la silla turca, proporciona acceso
microquirúrgico a la porción del canal óptico que entra en contacto con las
celdas etmoidales y el seno esfenoidal. Esta última técnica se puede realizar
con medios endoscópicos transnasales (15,16).
El abordaje transorbitario-etmoidal utiliza una vía a través de la pared
medial de la orbita la cual permite extirpar las celdas etmoidales posteriores
que forman parte de la cara infero medial del canal óptico.
PATOLOGÍA TRAUMÁTICA CRANEO-ORBITARIA: FRACTURAS
Las fracturas orbitarias se producen comúnmente después de un trauma
directo oculo-facial pero también pueden existir asociadas a politraumas con
lesiones graves craneoencefálicas, torácicas, o abdominales, etc. Muchas de
ellas, a pesar de tratamientos correctos, dejan secuelas permanentes como
diplopia, ceguera y alteraciones en las vías lagrimales. Cuando no se
diagnostican o no se tratan bien pueden dejar también deformidades estéticas.
Las causas más frecuentes que intervienen en la producción de las fracturas
orbitarias son los accidentes de vehículos con motor, las caídas, los traumas
deportivos y las agresiones, etc. En USA, el trauma fronto orbitario, es la
segunda causa de ceguera.
Clínica
Los síntomas asociados a las fracturas de la orbita pueden ser triviales o
devastadores incluyendo la pérdida completa de visión (17). Los pacientes
pueden presentar diplopia, alteraciones sensitivas en la piel, dolor mandibular
al abrir la boca, sangrado nasal, hinchazón de los párpados, rinolicuorraquia.
La exploración debe incluir un examen completo ocular. Pudiendo existir
disminución de la agudeza visual, ptosis, heridas en los párpados,
desplazamientos oculares, limitaciones de la movilidad ocular, movimientos
dolorosos, enoftalmus, proptosis, epixtasis, desplazamiento medial o lateral del
canto ocular, alteración en la sensibilidad en el dermatoma correspondiente y
enfisema subcutáneo entre otros hallazgos. Las fracturas del tercio medio
facial suele provocar edema importante de los tejidos blandos. El aplanamiento
de la eminencia malar indica fractura con desplazamiento del zigoma. La
palpación del contorno orbitario puede revelar deformidades indicando que
existen fracturas. La salida continua de líquido claro transparente que aumenta
al comprimir las venas yugulares o al flexionar el cuello es sugestivo de
fístula de líquido cefalorraquideo (LCR). Esto ocurre en las fracturas que
afectan al techo orbitario con desgarro de la duramadre y también se observa en
el 20% de las fracturas naso-etmoidales (figura 5). El diagnóstico de fístula
de LCR se confirma si el análisis del líquido tiene un contenido de glucosa
mayor de 30mg/ml. Una Tomografía Computarizada Cerebral después de la
inyección de Metrizamida en la teca puede detectar el punto de salida de LCR.
La anosmia es un síntoma típico de las fracturas del suelo de la fosa craneal
anterior las cuales pueden irradiarse al techo orbitario. La presencia de
heridas externas deben hacer pensar al clínico en la posibilidad de cuerpos
extraños o ser el inicio de trayectorias de proyectiles u otros objetos
penetrantes. A veces después de un trauma craneo-orbitario aparece un soplo
carotídeo acompañado de quemosis conjuntival y exoftalmus, hallazgos que
sugieren la producción de una fístula carótido-cavernosa.
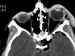
Figura 5. La imagen de TC muestra un neumoencéfalo en una fractura
del techo de la orbita izquierda.
Neuroimagen
La Tomografía Computarizada (TC) ha revolucionado la evaluación de las
fracturas orbitarias y sustituido a las técnicas de Rx simples, técnicas de Rx
tomográfico y las xeroradiografías. La introducción del TC helicoidal permite
una reducción significativa en el tiempo de análisis y es muy útil en la
población pediátrica. La TC tridimensional (18) sirve de ayuda para la
planificación y guía de las reparaciones quirúrgicas. Las imágenes de
resonancia magnética evitan la radiación, dan mejor definición de las partes
blandas, e informan de la composición de ciertas lesiones (hematomas,
inflamaciones, herniaciones cerebrales, etc.). Son muy útiles como complemento
en la evaluación de las fracturas del techo de las órbitas. Las técnicas de
ultrasonidos son rápidas y dan información de cuerpos extraños, quistes,
hematomas, desplazamientos, etc. (19). En ciertos casos de fracturas provocadas
por objetos penetrantes (cuchillos, antenas, arpones, lapiceros) la angiografía
informa de la relación de estos objetos con las estructuras vasculares
intracraneales) siendo muy útil para la planificación quirúrgica. Igualmente
la angiografía cerebral permite diagnosticar la presencia de una fístula
carótido-cavernosa de origen traumático.
Clasificación de las fracturas
El tipo de fractura ordinaria debe ser reconocido después de la valoración
clínica del paciente y de los estudios neuroimagen. Según la localización
anatómica las fracturas pueden ser: (del suelo, techo, paredes lateral y medial
orbitario), del tercio medio facial. Según la forma se clasifican en
«blow-out» y «blow-in». Pueden ser también simples o conminuta, desplazadas
y no desplazadas, estables o inestables. Cuando sale LCR son abiertas. Son
evolutivas si crecen en el tiempo herniándose a su través las leptomeninges y
a veces el tejido cerebral. En las fracturas tipo «blow-out» no se afecta el
reborde orbitario inferior, existe un desplazamiento óseo hacia fuera de la
órbita lo cual puede causar enoftalmus al aumentar el volumen orbitario. En
contraste, en las fracturas del tipo «blow-in», los fragmentos se desplazan al
interior de la órbita reduciendo su volumen y provocando proptosis. El techo de
la órbita suele verse afectado en este último tipo de fracturas.
Tratamiento
El tratamiento de fracturas que interesan el techo orbitario, canal óptico,
la fisura orbitaria superior, ápex orbitario, el etmoides, el esfenoides son de
interés neuroquirúrgico. En las medidas de tratamiento médico se recomienda
evitar en lo posible las maniobras de Valsalva las cuales pueden causar enfisema
orbitario, y sangrado con resultado de proptosis y a veces aumentar un
neumoencéfalo existente. Se aconseja por lo tanto el uso de descongestivos
nasales en spray. La proximidad de los senos paranasales a la órbita aumenta el
riesgo de infección de su contenido si se tiene sinusitis. En estos casos se
recomienda el uso de antibióticos profiláctico. Si existen cuerpos extraños
incluidos o heridas contaminadas o sucias se debe utilizar antibióticos. La
presencia de LCR obliga al uso de antibioterapia siempre.
El uso de corticoides cuando existe edema orbitario y hematomas reduce la
proptosis y mejora las condiciones quirúrgicas orbitarias. Cuando se
administran debe asociarse antibioterapia sistémica. Si se produce una pérdida
de visión completa o parcial secundaria a una compresión del nervio óptico en
el ápex orbitario o en canal óptico la administración de corticoides en
megadosis no ha demostrado un efecto sustancial por lo que su uso permanece en
controversia (20-24).
La presencia de neumoencéfalo o lesiones contusivas cerebrales hace
necesario el uso de anticomiciales profilácticos.
Las fracturas del techo orbitario son más frecuentes en los niños que en
los adultos. La disminución de la visión puede ser secundaria a una lesión
directa del ojo, a una hemorragia orbitaria, a una fractura que se extiende
hasta el canal óptico. Los daños directos del nervio óptico pueden ser
debidos a contusiones, estiramientos, torsiones, desgarros, secciones y
compresiones (figura 6). A veces se produce la lesión en los vasos que irrigan
al nervio. Cuando la perdida de visión es progresiva y existe un hematoma,
fractura extendida al canal óptico o fragmentos óseos que afectan al nervio
óptico se indica una intervención descompresiva de urgencia (20-24). Ante una
pérdida completa de visión, aunque existen controversias, se indica cada vez
más una cirugía descompresiva de urgencia. Se debe recordar que el nervio
óptico tolera muy poco el tiempo de isquemia por lo que el diagnóstico debe
realizarse de urgencia al igual que las descompresiones.

Figura 6. En la imagen de TC, se aprecia un fragmento óseo en la
pared interna de la órbita izquierda que comprime los elementos del cono
orbitario.
Las fracturas del techo orbitario y las naso órbito etmoidales requieren a
veces tratamiento neuroquirúrgico de urgencia por existir hemorragias
intracraneales, contusiones cerebrales, fracturas complejas abiertas
hundimientos del hueso frontal, heridas, penetrantes con cuerpos extraños
intracraneales (25-29). En estos casos el abordaje se realiza mediante incisión
cutánea bicoronal y requiere la colaboración estrecha de varios especialistas
(figura 7).

Figura 7. Fractura abierta hundida del techo orbitario derecho, con
desgarro dural y herniación cerebral.
En ausencia de las indicaciones de urgencias citadas anteriormente una espera
de una semana antes de la intervención quirúrgica es razonable. En este
período de observación el 80% de la fístulas de LCR se cierran
espontáneamente. Otros autores abogan por la cirugía precoz cuando existe
fístula de LCR con el argumento de evitar infecciones.
Las complicaciones mas frecuente después de la cirugía suelen ser las
fístulas de LCR, hidrocefalia, pérdida de visión, diplopia y enoftalmus. Los
pacientes que sufres desgarros de la duramadre desarrollan meningitis y/o
abscesos cerebrales en un 25% de los casos. Otras de las complicaciones que
pueden ocurrir cuando no se diagnostican bien estas fracturas o la reparación
dural es defectuosa es el desarrollo de fracturas evolutivas con herniaciones de
la leptomeninges solas o asociadas a encarceración de tejido cerebral en los
defectos óseos creados (figura 8).
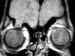
Figura 8. Imagen coronal de RM que muestra una herniación cerebral
a través de una fractura evolutiva en el techo de la orbita derecha.
HIPERTENSIÓN ENDOCRANEAL BENIGNA
Clásicamente el tratamiento neuroquirúrgico de elección para reducir la
hipertensión endocraneal benigna (figura 9) ha sido la implantación de
derivaciones de LCR. Sin embargo estas implantaciones no están exentas de
complicaciones y de morbilidad. Las derivaciones lumboperitoneales con
frecuencia se obstruyen y son fuente de dolores radiculares o de reacciones
inflamatorias.
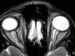
Figura 9. Acumulos de LCR dentro de las vainas del nervio óptico
vistos en una plano axial de RM. Paciente con hipertensión endocraneal benigna.
La técnica de fenestración de las vainas del nervio óptico ha resurgido
como método de tratamiento de la hipertensión endocraneal benigna en la
última década (30-32). En muchos de los casos se ha convertido en el
procedimiento de elección con una eficacia que alcanza el 90%. La mayoría de
paciente tratados con esta técnica presentaban hipertensión endocraneal
crónica con edema de papila y afectación del nervio óptico. La técnica se ha
mostrado eficiente también en otros tipos de hipertensión endocraneal
secundarios a hidrocefalia, tumores cerebrales y trombosis de senos venosos
intracraneales (33). La mayoría de autores creen que el mecanismo de reducción
de la presión intracraneal es el filtrado de LCR hacia la órbita desde las
fenestraciones de las vainas de nervio ópticos. El acceso al nervio para
realizar estas fenestraciones puede ser hecho por una vía medial o por una vía
lateral. En ambos casos se debe abrir bien tanto la duramadre como la aracnoides
del nervio óptico permitiendo la salida de LCR hacia la órbita.
BIBLIOGRAFÍA
- Natori Y, Rhoton ALJ. Transcranial approach to the orbit: microsurgical
anatomy. J Neurosurg 1994; 81: 78-86.
- Maroon JC, Kennerdell JS, Brillman J. Tumors of the orbit; in Ed.Wilkins
RHyR, SS (eds): Neurosurgery. Mcgraw-Hill, 1995, pp 1481-1493.
- Brihaye J. Neurosurgical approaches to orbital tumours. Adv Tech Stand
Neurosurg 1976; 3: 103-121.
- Sibony PA, Krauss HR, Kennerdell JS, et al. Optic nerve sheath
meningiomas. Clinical manifestations. Ophthalmology 1984; 91: 1313-1326.
- Michael CB, Lee AG, Patrinely JR, et al. Visual loss associated with
fibrous dysplasia of the anterior skull base. Case report and review of the
literature. J Neurosurg 2000; 92: 350-354.
- Yavuzer R, Khilnani R, Jackson IT, et al. A case of atypical
McCune-Albright syndrome requiring optic nerve decompression. Ann Plast Surg
1999; 43: 430-435.
- Durante F. Contribution to endocraneal surgery. Lancet 1887; 2: 654-655.
- Natori Y, Rhoton ALJ. Microsurgical anatomy of the superior orbital
fissure. Neurosurgery 1995; 36: 762-775.
- Maroon JC, Kennerdell JS. Surgical approaches to the orbit. Indications
and techniques. J Neurosurg 1984;60:1226-1235.
- Krönlein RU. Zur pathologie und operativen Behandlung der Dermoid-zysten
der orbita. Beitr Klin Chir 1889; 4: 149-163.
- Berke RN. A modified Krönlein operation. Trans Am Ophthalmol Soc 1953;
51: 193-231.
- Arai H, Sato K, Katsuta T, et al. Lateral approach to intraorbital
lesions: anatomic and surgical considerations. Neurosurgery 1996; 39: 1157-1162.
- Maurer J, Hinni M, Mann W, et al. Optic nerve decompression in trauma and
tumor patients. Eur Arch Otorhinolaryngol 1999; 256: 341-345.
- Knox BE, Gates GA, Berry SM. Optic nerve decompression via the lateral
facial approach. Laryngoscope 1990; 100: 458-462.
- Luxenberger W, Stammberger H, Jebeles JA, et al. Endoscopic optic nerve
decompression: the Graz experience. Laryngoscope 1998; 108: 873-882.
- Kountakis SE, Maillard AA, El-Harazi SM, et al. Endoscopic optic nerve
decompression for traumatic blindness. Otolaryngol Head Neck Surg 2000; 123:
34-37.
- Ashar A, Kovacs A, Khan S, et al. Blindness associated with midfacial
fractures. J Oral Maxillofac Surg 1998; 56: 1146-1150.
- Remmler D, Denny A, Gosain A, et al. Role of three-dimensional computed
tomography in the assessment of nasoorbitoethmoidal fractures. Ann Plast Surg
2000; 44: 553-562.
- Forrest CR, Lata AC, Marcuzzi DW, et al. The role of orbital ultrasound
in the diagnosis of orbital fractures. Plast Reconstr Surg 1993; 92: 28-34.
- Cook MW, Levin LA, Joseph MP, et al. Traumatic optic neuropathy. A
meta-analysis. Arch Otolaryngol Head Neck Surg 1996; 122: 389-392.
- Lee AG. Traumatic optic neuropathy [letter; comment]. Ophthalmology 2000;
107: 814.
- Levin LA, Beck RW, Joseph MP, et al. The treatment of traumatic optic
neuropathy: the International Optic Nerve Trauma Study [see comments].
Ophthalmology 1999; 106: 1268-1277.
- Li KK, Teknos TN, Lai A, et al. Traumatic optic neuropathy: result in 45
consecutive surgically treated patients. Otolaryngol Head Neck Surg 1999; 120:
5-11.
- Mine S, Yamakami I, Yamaura A, et al. Outcome of traumatic optic
neuropathy. Comparison between surgical and nonsurgical treatment. Acta
Neurochir (Wien) 1999; 141: 27-30.
- Denny AD, Rosenberg MW, Larson DL. Immediate reconstruction of complex
cranioorbital fractures in children. J Craniofac Surg 1993; 4: 8-20.
- Penfold CN, Lang D, Evans BT. The management of orbital roof fractures.
Br J Oral Maxillofac Surg 1992; 30: 97-103.
- Crockett DM, Funk GF. Management of complicated fractures involving the
orbits and nasoethmoid complex in young children. Otolaryngol Clin North Am
1991; 24: 119-137.
- Holt GR, Holt JE. Management of orbital trauma and foreign bodies.
Otolaryngol Clin North Am 1988; 21: 35-52.
- Gonul E, Akboru M, Izci Y, et al. Orbital foreign bodies after
penetrating gunshot wounds: retrospective analysis of 22 cases and clinical
review. Minim Invasive Neurosurg 1999; 42: 207-211.
- Mauriello JAJ, Shaderowfsky P, Gizzi M, et al. Management of visual loss
after optic nerve sheath decompression in patients with pseudotumor cerebri.
Ophthalmology 1995; 102: 441-445.
- Kelman SE, Heaps R, Wolf A, et al. Optic nerve decompression surgery
improves visual function in patients with pseudotumor cerebri. Neurosurgery
1992; 30: 391-395.
- Lee AG, Patrinely JR, Edmond JC. Optic nerve sheath decompression in
pediatric pseudotumor cerebri. Ophthalmic Surg Lasers 1998; 29: 514-517.
- Horton JC, Seiff SR, Pitts LH, et al. Decompression of the optic nerve
sheath for vision-threatening papilledema caused by dural sinus occlusion.
Neurosurgery 1992; 31: 203-211.
|