ACTUALIZACIONES TECNOLÓGICAS EN OFTALMOLOGÍA
GILI MANZANARO P1, MARTÍN RODRIGO JC2, MATILLA RODRÍGUEZ A2
(1) Doctor en
Medicina y Cirugía. Especialista en Oftalmología. Fundación Hospital Alcorcón.
(2) Licenciado en Medicina y Cirugía. Especialista en Oftalmología. Fundación
Hospital Alcorcón.
RESUMEN
Las técnicas de imagen se han incorporado a la oftalmología como herramientas de diagnóstico, con una clara proyección terapéutica en algunos casos, con aplicaciones en la clínica, la docencia y la investigación. El objetivo de esta revisión es describir las principales aplicaciones de las técnicas de imagen fotográfica en oftalmología, los equipos y las indicaciones de cada una de ellas: fotografía ocular externa, fotografía de polo anterior (lámpara de hendidura, microscopía especular), fotografía de fondo de ojo (color, filtros AFG e ICGA) y fotografía quirúrgica.
INTRODUCCIÓN
Fotografía oftalmológica
El ojo humano como objeto de la fotografía tiene unas características específicas propias que deben conocerse (1):
1. El ojo es sensible a la luz y se fatiga, por lo que un exceso de luz o sesiones muy prolongadas pueden llevar al cansancio y la falta de colaboración del paciente.
2. El ojo está formado por estructuras muy diferentes: transparentes (córnea, cristalino) y opacas (esclera, iris, retina...); claras (esclera, nervio óptico) y oscuras. Estos grandes contrastes obligan a utilizar técnicas de iluminación muy diferentes para cada estructura y situación.
3. La exploración oftalmológica requiere la utilización de instrumentos, iluminaciones y accesorios muy variados: lámpara de hendidura, microscopio especular, lentes accesorias, retinógrafos, fluoresceína... La realización de fotografías obliga a un perfecto conocimiento y utilización de los mismos.
4. La patologías oculares son de muy variable magnitud: desde grandes lesiones macroscópicas (tumores orbitarios y palpebrales), hasta patologías microscópicas (lesiones endoteliales, pequeñas lesiones retinianas). Es necesario utilizar magnificaciones muy diferentes en cada caso.
5. El fotógrafo oftalmológico debe estar familiarizado con la patología ocular, debiendo conocer la mejor técnica a utilizar en cada caso, así como las variaciones en la iluminación necesarias para destacar y documentar esa patología.
La fotografía oftalmológica nace apoyada en los grandes avances de los instrumentos de exploración y las mejoras de la técnica fotográfica (cámaras, objetivos, flashes, películas, filtros, etc.). La fotografía ocular externa, la fotografía con lámpara de hendidura, la microfotografía especular, la fotografía de fondo y la angiofluoresceingrafía son las principales ramas de una técnica en continuo avance y expansión. Este desarrollo propició profesionales específicamente dedicados a la fotografía oftalmológica. Muestras de interés en este campo son, entre otras muchas, la aparición en 1969 de la Ophthalmic Photographers´ Society (OPS) (2) y en 1977 The Journal of Ophthlamic Photography, y otras sociedades y publicaciones dedicadas a la imagen en oftalmología (fig. 1).Cada vez son más numerosos los textos dedicados a la fotografía oftalmológica y ya son auténticos clásicos los libros publicados por Justice (3), Saine (4), o Vetter (5), entre otros.
La incorporación de nuevas técnicas de imagen a la oftalmología, con la introducción de técnicas digitales, topográficas, ecográficas, láser, etc. ha hecho que se cambie el concepto de «fotografía oftalmológica» por el término más amplio de «imagen en oftalmología». Esto ha propiciado el cambiado de nombre de sociedades como la Ophthalmic Imaging Association (OIA) (6), previamente denominada British Ophthalmic Photographic Asociation (BOPA), y que se hable de «Técnicos en imagen oftalmológica», en vez de fotógrafos oftalmológicos.
Imagen digital y teleoftalmología
La «era digital» abre un nuevo campo en cuanto a sistemas de captación, almacenamiento y retoque de imágenes. La tecnología digital está ampliamente implantada en nuestro país. Y por extensión se ha extendido a la imagen en oftalmología. La fotografía tradicional en 35 mm sigue siendo de una mejor calidad, es decir, con mayor resolución. Sin embargo, estas diferencias cada vez son menores y la fotografía digital aporta grandes ventajas en la documentación médica: la obtención inmediata, el almacenamiento, la fácil manipulación y la facilidad de transmisión de las imágenes constituyen algunos de los pilares de su clara imposición en la imagen científica (tabla 1).

Apoyado en el progreso de las técnicas de imagen digital y las nuevas tecnologías de comunicación nace la telemedicina. «Telemedicina», que literalmente significa «medicina a distancia», es la utilización de las telecomunicaciones para prestar servicios sanitarios de diagnóstico, tratamiento o prevención, independientemente de la distancia a la que se encuentren (10-12). Y entre ellas aparece la teleoftalmología. Las principales aplicaciones de la teleoftalmología son (13):
Acceso a especialistas para pacientes residentes en lugares remotos.
Consultas médicas entre centros o interhospitalarias (14).
Screening de enfermedades: especialmente utilizada en glaucoma (15-17) retinopatía diabética (18-21).
Investigación y estudios clínicos multicéntricos.
Educación continuada a distancia.
El objetivo de este capítulo es describir las principales aplicaciones de las técnicas de imagen en oftalmología, los equipos y las indicaciones de cada una de ellas. Existen otras muchas técnicas basadas en la imagen que progresivamente se van desarrollando y perfeccionando (Topografía corneal, BMU, OCT, HRT, RTA, SLO etc). pero las limitaciones del texto nos obligan a centrarnos en las que podríamos llamar «imágenes fotográficas», es decir:
Fig. 1. Sociedades y publicaciones de fotografía oftalmológica.
1. Fotografía ocular externa.
2. Fotografía de polo anterior.
3. Fotografía de fondo de ojo: color, filtros y colorantes.
4. Fotografía quirúrgica.
1. IMAGEN OCULAR EXTERNA
La fotografía ocular externa es la más general y elemental forma de imagen oftalmológica, empleada para captar las capas externas del ojo y sus estructuras adyacentes (22). Este mismo equipo se emplea para tomar fotos de salas de exploración equipos médicos, técnicas de diagnóstico y tratamiento oftalmológico.
Equipo
Tradicional: Clásicamente se empleaban equipos de caros que proporcionaban una excelente calidad de imagen.
Cámaras reflex de 35 mm.
Objetivos especiales «macro» de 105 mm de focal.
Unidades de flashes externas (flash anular, puntual, doble) (fig. 2).
Digital:
Cámaras digitales compactas: este tipo de cámaras, en continuo desarrollo y mejoría, con resoluciones que actualmente llegan a lo 8 millones de píxels, con objetivos zoom que permiten fotografías a distancias muy cortas (macro), empleando el propio flash de la cámara, permiten realizar fotografías oculares externas con facilidad y a bajo coste (fig. 2).
Cámaras digitales reflex: hasta hace poco reservadas a profesionales por su alto coste, actualmente se encuentran modelos a precios asequibles (Canon D30, Nikon D70, entre otra). Estos equipos permiten utilizar objetivos intercambiables de alta calidad y proporcionan un mayor control de los parámetros fotográficos.

Fig. 2. Fotografía externa. Equipo tradicional y equipo digital.
Las cámaras digitales compactas añaden a las ventajas de propias de todas las imágenes digitales, el tratarse de cámaras muy pequeñas y fáciles de manejar, y la posibilidad de grabar videos (aunque de baja resolución). Como inconvenientes, el elevado consumo de baterías, el retardo en la captación de la imagen y los automatismos de estas cámaras, que a veces hacen difícil de controlar el enfoque y la magnificación empleada.
Al igual que en cualquier otra técnica de imagen pueden captarse imágenes estereoscópicas (3D); en el caso de la fotografía externa es preciso utilizar una técnica fotográfica simultanea empleando dos cámaras (23).
Aplicaciones
La fotografía ocular externa tiene aplicaciones en la patología ocular, tanto en la consulta como en el quirófano (24) (fig. 3).
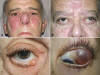
Fig. 3. Fotografía externa. Aplicaciones.
Fotografía de cara (magnificación 1:10) y ambos ojos (magnificación 1:4):
La fotografía ocular externa es la técnica de elección en patologías faciales con repercusión ocular, patología orbitaria y palpebral, estrabismos y parálisis oculares, y anomalías pupilares (anisocorias).
Fotografía de un ojo (baja magnificación 1:3, alta magnificación 1:1): patología orbitaria y palpebral, así como fotografía quirúrgica. También puede emplearse en patología de segmento anterior cuando no disponemos de imágenes de lámpara de hendidura (patología de borde libre, conjuntiva, esclera y otras).
2. IMAGEN DE POLO ANTERIOR
Fotografía con lampara de hendidura
La fotografía con lámpara de hendidura es una de las formas complejas y desafiantes de fotografía oftálmica. Ello deriva de la complejidad y flexibilidad del propio equipo, la posibilidad de emplear tinciones y lentes auxiliares, así como las variadas estructuras y patologías oculares a captar. Por este motivo, aunque se han tratado de introducir sistemas automáticos o semiautomáticos, éstos han tenido poco éxito. Constituye la técnica de elección en la patología del segmento anterior (25) y se ha empleado como sistema de clasificación objetiva en las cataratas (26). También se ha empleado como sistema de documentación de la patología vítrea (27,28).
Equipo
Tradicional:
Lámpara de hendidura fotográfica.
Cámara de 35 mm.
Unidad de flash electrónico.
Película: diapositivas 200ASA (400ASA).
Digital (fig. 4):
Lámpara de hendidura clínica /fotográfica.
Cámara digital compacta /reflex.
Flash electrónico: si /no.
Almacenamiento: ordenador, tarjetas de memoria (compact flash, memory stick).

Fig. 4. Fotografía con lámpara de hendidura. Equipo con cámara réflex, flash
electrónico y sistema de archivo.
Aunque la incorporación de las técnicas digitales a las lámparas de hendidura ha sido más lenta que a otros equipos oftalmológicos, en la actualidad hay gran variedad de equipos y múltiples posibilidades. Y entre ellas se han descrito adaptaciones a lámparas de hendidura (29 ).Las imágenes digitales con lámpara de hendidura permiten realizar mediciones (30) o manipulaciones para evitar reflejos (31). Sin embargo existen algunas controversias en este campo son:
Equipos compactos integrados (ej Topcon): ventaja: fácil manejo, estética agradable; inconvenientes: equipo cerrado, sin posibilidad de cambios por cámaras mejores.
Codos de adaptación de cámaras (ejemplo: Digicam, Zeiss) Ventajas: permiten adaptar muchas cámaras fotográficas y cámaras de video mediante sistemas de anillos; este mismo equipos se puede adaptar fácilmente a los microscopios quirúrgicos de la casa (fig. 14) inconvenientes: son más incómodas de manejar.
Cámaras digitales compactas: Ventajas: menor tamaño; inconvenientes: menores posibilidades de ajustes manuales.
Flash electrónico: El flash electrónico tiene la ventaja de permitir realizar fotografía con altos aumentos sin que salgan borrosas por leves movimientos del paciente; como inconvenientes, aumentan considerablemente el coste del equipo (fig. 4).
Sistemas de almacenamiento: El volumen de fotografías a realizar va a condicionar el sistema que más se ajuste a nuestras necesidades: para una utilización esporádica, puede ser suficiente con las tarjetas de almacenamiento de la cámara; para una utilización muy frecuente es interesante contar con programas informáticos de manejo y almacenamiento de imágenes (como Imagenet, Optilink, Visupac o Eyecap).
Aplicaciones y técnicas de iluminación
La fotografía con LH es la técnica de elección en la patología del segmento anterior, el ángulo camerular (goniofotografía), el vítreo y la periferia retiniana (1,25,26). La técnica de iluminación y los parámetros a emplear dependerá de la patología a estudiar.
Iluminación difusa: Ofrece una visión de conjunto del ojo. Es la primera foto a realizar en cualquier patología (fig. 5).
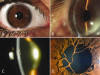
Fig. 5. Fotografía con lámpara de hendidura. Iluminación difusa y directa.
Parámetros:
Aumentos 10-16 x.
Luz: Hendidura abierta al máximo con difusor (con o sin luz de relleno).
Ángulo 45º.
Flash /luz (intensidad): media-alta.
Iluminación directa (fig. 5) incluye:
Hendidura: Realza detalles de polo anterior (córnea, cámara anterior, cristalino ).
Parámetros:
Aumentos 16-40x.
Luz: Hendidura estrecha (0,1 mm), luz de relleno apagada.
Ángulo: 45-60º.
Flash/luz: alta.
Hendidura + luz de relleno: Realza detalles de polo anterior con una iluminación de fondo. Es la técnica más característica en la fotografía con LH.
Parámetros:
Aumentos 16-25x.
Luz: Hendidura estrecha con luz de relleno.
Ángulo: 45-60º.
Flash/luz: alta.
Iluminación tangencial: Ofrece imágenes muy contrastadas del polo anterior creando un efecto «tridimensional», especialmente útil en valoración de lesiones de iris, pseudoexfoliación y ángulos estrechos.
Parámetros:
Aumentos 16-40x.
Luz: Hendidura amplia, luz de relleno apagada.
Ángulo: 70-90º.
Flash/luz: bajo.
Iluminación indirecta (fig. 6).
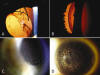
Fig. 6. Fotografía con lámpara de hendidura. Iluminación indirecta.
Retroiluminación de fondo: Resalta anomalías de iris, cristalino, lentes intraoculares, etc. por el reflejo rojo de fondo de ojo.
Parámetros:
Aumentos 10-25x.
Luz: Media, luz relleno habitualmente apagada.
Ángulo: 2-4º. Para patologías de iris habitualmente luz centrada en pupila sin dilatar. Para el resto de las patologías iluminación descentrada lateralmente , con midriasis farmacológica.
Flash/luz: alta.
Retroiluminación desde el iris: Destaca detalles de la córnea o cámara anterior por la luz rebotada en el iris.
Parámetros:
Aumentos 16-25x.
Luz: Hendidura media luz de relleno apagada
Ángulo: 45-60º.
Flash/luz: media-alta.
Dispersión escleral: Realza lesiones de la córnea por dispersión de la luz en la esclera.
Parámetros:
Aumentos 10-16x.
Luz: Hendidura media, luz de relleno apagada
Ángulo: 30º, desplazado lateralmente incidiendo en esclera.
Flash/luz: alta.
Aplicaciones especiales (fig. 7):

Fig. 7. Fotografía con lámpara de hendidura. Aplicaciones especiales.
Fluoresceína + luz azul cobalto: su objetivo es la visualización de erosiones corneales, conjuntivales, seidell, y el patrón de adaptación de lentillas.
Parámetros:
Aumentos 10-16x.
Luz: Luz con filtro azul y hendidura amplia. Se puede añadir un filtro amarillo verdoso (barrera) que realza más la tinción.
Ángulo: 45º.
Flash/luz: Media-alta.
Lente de no contacto (90dp, 78dp, Superfield )Indicado para fotografiar el vítreo y polo posterior.
Parámetros:
Aumentos 25x.
Luz: Hendidura media, luz de relleno apagada.
Ángulo: 4º, lateralizar la luz para evitar reflejo.
Flash/luz: baja.
Lente de contacto (tres espejos): Indicado para fotografía del ángulo (goniofotografía), polo posterior y periferia retiniana.
Parámetros:
Aumentos: 25x.
Luz: hendidura media, luz de relleno apagada.
Ángulo: 4º, ladear la lámpara de hendidura y evitar los reflejos de luz sobre la lente.
Flash/luz: baja.
Fotografía de endotelio: microscopia endotelial
La fotografía de endotelio nos permite valorar la forma, tamaño, densidad y alteraciones de las células endoteliales corneales. Esta técnica de imagen se basa en el principio del reflejo especular descrito por Vogt en 1920.Tiene aplicaciones en la patología corneal y la valoración de los efectos de la edad, drogas, enfermedades y cirugías en el endotelio corneal (32-35).
Equipo
La fotografía del endotelio corneal puede realizarse con varios equipos (fig. 8):

Fig. 8. Fotografía de endotelio corneal. Equipos e imágenes.
Lámpara de hendidura
Lámpara de hendidura fotográfica (convencional /digital).
Parámetros:
Aumentos altos 40x.
Hendidura estrecha, sin luz de relleno.
Ángulo. Reflejo especular 30º iluminación x 30º lámpara h.
Intensidad Flash/luz: Alta.
Valoración: esta técnica permite una valoración clínica (estimación de la densidad y patología), no un verdadero contaje. Es difícil de realizar, requiere experiencia.
Lámpara de hendidura + lente especular:
Lámpara de hendidura + lente especular. Fotografía tradicional o digital acoplada a ordenador.
Magnificación 50-520 (7,5-32,5x).
Valoración: Manejo difícil por el enfoque muy selectivo. Permite valorar la forma, el tamaño y la densidad de las células endoteliales.
Microscopio especular no contacto:
Equipo compacto semiautomático, de no contacto, en el que se visualiza la imagen del ojo y el endotelio en un pequeño monitor. Los resultados se imprimen.
Valoración: Equipo de fácil manejo que ofrece una valoración semiautomática de la forma tamaño y densidad celular seleccionando un mínimo de 10 células contiguas, aportando muchos parámetros: área celular mínima, máxima y media; coeficiente de variación (CV); densidad celular (CD). Dificultad en obtención de imágenes en casos de edemas corneales marcados.
Microscopio especular contacto:
Microscopio monocular de contacto mediante un cono de aplanación, con un equipo digital incorporado y un ordenador para una valoración semiautomática.
Valoración: Ofrece imágenes de gran calidad y de campo amplio. Especialmente indicados para estudios en banco de ojos (córneas donantes). Permite valoración semiautomática de la estructura, forma, tamaño y densidad celular, mediante un software muy completo.
Aplicaciones
Patología corneal. Distrofias posteriores.
Valoración prequirúrgica de córneas seniles y distrofias.
Transplantes de córnea: córnea donante, injerto corneal postquirúrgico.
Portadores de lentes de contacto.
Efectos en endotelio de la edad, drogas, enfermedades oculares, traumas o cirugías.
3. IMAGEN DE FONDO DE OJO
La imagen de fondo de ojo es uno de los campos en mayor expansión (36). La cámara de fondo de ojo, a pesar de la aparición de nuevas tecnologías de imagen (OCT, SLO, GDx, RTA, HRT, etc), continúa siendo el principal método de documentación de la patología del polo posterior. Desde la aparición de las primeras fotografías de fondo de ojo, realizadas en 1886 por Jackmman y Webster (37), hasta la actualidad, con la amplia difusión de los sistemas de imagen digital, se ha recorrido un largo camino.
La cámara de fondo actualmente nos permite estudiar el fondo de ojo con en color (retinografía), resaltar distintas estructuras con filtros (azul, verde y rojo), y emplear colorantes con filtros especiales para destacar la patología vascular retiniana y alteraciones maculares (AFG) y la vascularización coroidea (ICGA). La introducción de los sistemas digitales en las cámaras de fondo facilita enormemente la obtención, el almacenamiento, la manipulación y la transmisión de las imágenes. Además estos equipos nos permiten obtener y visualizar fotografías estereoscópicas secuenciales (3D) (38) medir de estructuras del fondo de ojo con una alta fiabilidad (39) y realizar montajes panorámicos, entre otras cosas.
Equipos
Desde la introducción de las cámaras de fondo con equipos digitales en 1987 (Topcon Imagenet), estos equipos han evolucionando con notables mejorías tanto en las cámaras como en los programas de manejo y almacenamiento (Imagenet, Visupac, EyeCap).
Cámaras no midriáticas: Cámaras de muy fácil manejo, utilizadas por personal no especializado, que se han empleado en programas de screening, especialmente en la retinopatía diabética.
Cámaras midriáticas: Cámaras de uso oftalmológico, con las que pueden realizarse todas las técnicas de imagen. La mayoría de estos equipos en la actualidad se comercializan con equipos exclusivamente digitales.
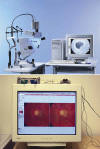
Fig. 9. Fotografía con cámara de fondo de ojo. Equipo y software para 3D.
Constan de:
Cámara de fondo (retinógrafo/angiógrafo).
Cámaras: Existen gran variedad de cámaras y combinaciones posibles.
Cámara de 35 mm: En la actualidad la mayoría de los equipos ya se comercializan sin cámara tradicional. Se empleaban para color, fotografía con filtros y AFG.
Color: videocámara 3CCD (Sony) 768x576 pixeles. Empleada para fotografía en color (retinografía).
BN: cámara Kodak Megaplus 1.4.i (1024x1024)1.6i (1280 x1024 pixels). Empleada para fotografía con filtros, AFG e ICGA.
Cámara BN para observación (monitorización).
Ordenador con sistema de captura y almacenamiento digital.
Unidades de almacenamiento de imágenes: CD-ROM, MO, DVD.
Cámaras especiales: Con un uso mucho más restringido en la práctica clínica:
Cámara estereoscópica 3D (Discam): Obtiene imágenes tridimensionales en blanco y negro, realizando 2 fotografías simultáneas.
Fotografía de campo amplio (Retcam): Indicado en el estudio de patología pediátrica, especialmente retinopatía del prematuro.
Cámaras portátiles: Equipo de fondo de ojo de bajo peso para fotografía en color y AFG. Indicado en pacientes encamados o para campañas de detección en lugares remotos.
Técnicas y aplicaciones
1. Fotografía en color
La imagen en color de fondo de ojo (retinografía) es la técnica básica para registrar las patologías del vítreo, retina, coroides y nervio óptico.
La selección del ángulo de visión depende de la patología a estudiar:
50º: visión global del fondo de ojo. Se emplea en patologías extensas: retinopatía diabética, retinopatía hipertensiva y oclusiones vasculares, desprendimiento de retina, grandes tumores coroideos.
30-35º: Visión de polo posterior, que incluye papila, mácula y arcadas vasculares grandes. Es la magnificación de elección en todas las patologías maculares.
20º: Visión de alta magnificación, especialmente indicada para el estudio papila y resaltar detalles maculares.
2. Fotografía con filtros
La fotografía de fondo de ojo con filtros destaca selectivamente distintos detalles del fondo de ojo y nos permite localizar las lesiones según la longitud de onda del filtro utilizado: el filtro azul la interfase vítreo-retiniana y la CFNR, el filtro verde la vascularización retiniana y las alteraciones retinianas, y el filtro rojo la coroides (1).
La fotografía monocromática es una herramienta diagnóstica complementaria a la retinografía, la angiografía fluoresceínica y la angiografía con verde indocianina en la patología de fondo de ojo (40).
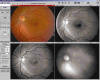
Fig. 10. Fotografía fondo ojo: retinografía y filtros.
Filtro azul
Filtro azul: longitud de onda 490 nm (filtro excitador de AFG).
Propiedades: Penetra escasamente en la retina. Resalta la capa de fibras nerviosas (CFNR) y la interfase vitreorretiniana. Requiere un enfoque muy selectivo (enfocar primero en los vasos de la retina y entonces moviendo ligeramente el enfoque hacia el vítreo (40).
Imágenes: En las imágenes con filtro azul se resalta la estriación de la CFNR, apareciendo la mácula oscura (por el pigmento xantófilo amarillo).
Aplicaciones
Membranas epirretinianas (41).
CFNR (glaucoma, patología de nervio óptico) (42,43).
Filtro verde
Filtro verde, luz aneritra o filtro «libre de rojo» (red free): 540 ó 575 nm.
Propiedades: Penetra la retina hasta EPR. Resalta la vascularización retiniana y sus alteraciones (hemorragias), aumentando el contraste entre la sangre de los vasos retinianos y el EPR (44). Se debe realizar el enfoque en los vasos retinianos.
Imágenes: Empleando el filtro verde con película en BN obtenemos la mejor representación de la visión oftalmoscópica, y es recomendable realizarse en todos los pacientes que queramos documentar. Son imágenes muy contrastadas en las que se resalta la vascularización retiniana y la retina, quedando «ocultas» las alteraciones coroideas pigmentadas.
Aplicaciones: Se emplean en todas las patologías de fondo de ojo, pero especialmente en:
Patología retiniana.
Vascularización retiniana normal y patológica. Hemorragias.
Membranas epirretinianas (45,46).
Estudio de CFNR, especialmente en presencia de opacidades de cristalino (47,48).
Filtro rojo
Filtro rojo: longitud de onda 630-640 nm.
Propiedades: Atraviesa la retina, EPR y coroides (excepto acúmulos pigmentados), siendo reflejada por la esclera. Resalta los detalles coroideos, especialmente lesiones pigmentadas, tumores y vascularización coroidea. Enfocar primero en los vasos retinianos y luego continuar bajando ligeramente hasta enfocar en la coroides (40).
Imágenes: Las imágenes captadas con luz monocromática roja son poco contrastadas, desdibujadas, en las que se visualiza la vascularización coroidea normal, apareciendo los vasos retinianos desdibujados. El filtro rojo resalta especialmente lesiones pigmentadas coroideas, que aparecen de color negro.
Aplicaciones:
Estudio de grandes vasos coroideos.
Patología coroidea: lesiones pigmentadas (nevus), tumores (melanomas, hemangioma) y lesiones inflamatorias coroideas (49,50).
1. -Fotografía con filtros y colorantes: AFG, ICGA
Angiografía fluoresceínica (AFG)
Novotny y Alvis en 1961 (51), 2 estudiantes de medicina, fueron los primeros en fotografiar el patrón de fluorescencia en la circulación retiniana humana. Estudios e investigaciones desarrollados en las siguientes tres décadas han hecho de la angiografía fluoresceínica una herramienta esencial para el conocimiento de las patologías coriorretinianas. La angiografía fluoresceínica (AGF) consiste en la realización de una serie de fotografías de fondo de ojo mientras se inyecta una solución de fluoresceína sódica rápidamente en la vena del brazo o mano. La cámara de fondo está equipada con unos filtros especiales que crean y realzan el patrón de fluorescencia, siendo registrado en una película en blanco y negro de alta sensibilidad (400 ASA) o en un sistema fotográfico digital. Durante los 30-45 primeros segundos el fotógrafo produce una rápida secuencia; la fotografía final de la serie debe hacerse 5 a 10 minutos más tarde.
Los equipos de angiografía digital, introducidos en la década de los 80 y con una clara implantación clínica en los 90, ofrecen imágenes con muy buena resolución, y aportan grandes ventajas a los sistemas tradicionales como son la disposición inmediata de las imágenes y la facilidad de almacenamiento, manipulación y transmisión de las imágenes. Por otro lado, la posibilidad de mostrar gráficamente al paciente unas alteraciones contribuye a una mejor relación medico-paciente.
Equipo
Cámara de fondo.
Filtros: Excitador (azul, 490nm) + barrera (amarillo verdoso 520 nm).
Cámaras:
Tradicionales: 35 mm. Película negativa blanco y negro 100-400 ASA.
Digital:
Baja resolución: 768x576 pixels.
Alta resolución. Cámara BN 1280x1024 pixels.
Fluoresceína sódica 20%, 5cc inyección intravenosa en antebrazo.
Equipo para inyección intravenosa.
Set de emergencia.
Consentimiento informado, especificando los riesgos de la prueba.
Aplicaciones
La AFG es probablemente la técnica de imagen con mayores implicaciones diagnósticas y terapéuticas. Es de gran valor en el estudio de la circulación retiniana y las enfermedades maculares. Las principales indicaciones son (fig. 11):
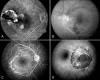
Fig. 11. Angiografía fluoresceínica (AFG). Aplicaciones.
Enfermedades maculares: DMAE, agujeros maculares, neovascularización coroidea, CCS, membranas epirretinianas, edemas maculares, distrofias retinianas, etc.
Enfermedades vasculares retinianas: obstrucciones arteriales y venosas, retinopatía diabética, malformaciones y tumores vasculares,etc
Enfermedades coroideas: neovascularización, inflamaciones, tumores coroideos, etc.
Enfermedades del nervio óptico: edema de papila, neuritis, neuropatías, tumores, drusas, fosetas, etc.
La aparición de nuevas tecnologías no invasivas y de alta resolución como la OCT probablemente limite las indicaciones de la AFG.
El conocimiento de los patrones angiográficos de normalidad y anormalidad es esencial en la interpretación de la prueba. Deben conocerse conceptos como:
Hiperfluorescencia: exceso de fluorescencia respecto al angiograma normal, que puede deberse a:
Autofluorescencia y pseudofluorescencia.
Transmisión (Defecto ventana): atrofia de EPR.
Escape o fuga: neovasos retinianos y coroideos.
Acumulación o estancamiento.
Tinción: cicatrices, tumores.
Hipofluorescencia: Reducción o ausencia de fluorescencia normal. Puede deberse a:
Bloqueo: por sangre, pigmento
Defecto de relleno vascular: isquemia.
La interpretación angiográfica queda fuera de las pretensiones de esta breve revisión.
Angiografía con verde indocianina (ICGA)
El verde indocianina es un colorante que inicialmente fue utilizado en la industria fotográfica. Fue empleado por primera vez en oftalmología por Flower y Hochheimer (52) a comienzos de los años 70 para visualizar la circulación coroidea. Aunque continuaron las investigaciones experimentales y clínicas, no fue hasta comienzos de los años 90 con la expansión de los sistemas de imagen digital cuando quedo bien establecido como método diagnóstico.
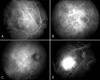
Fig. 12. Angiografía con verde indocianina (ICGA). Aplicaciones.
La angiografía con verde indocianina inicialmente y de forma predominante ha sido usada en el diagnóstico de la neovascularización subretiniana oculta asociada a la DMAE (53). Sin embargo, también ha contribuido al diagnóstico y conocimiento de otras patologías del segmento posterior y, menos frecuentemente, enfermedades del segmento anterior (54).
Equipo
Cámara de fondo.
Filtros: 805 y 835 nm.
Cámara de blanco y negro para infrarrojos de baja o alta resolución (1.280x1.024).
Verde de indocianina: 25 mgr de verde de indocianina (IC-Green o Cardio-Green) disuelto en 3-5 cc. Inyección intravenosa. Las reacciones adversas son muy poco frecuentes entre 0,22% y 0,34% (55,56) (inferiores a las descritas con AFG).
Equipo para inyección intravenosa.
Set de emergencia.
Consentimiento informado, especificando los riesgos de la prueba.
La prueba es poco molesta, bien tolerada, y dura aproximadamente 30 minutos. Puede realizarse conjuntamente con la AFG o inmediatamente después.
Fases:
Fase precoz (0-5 minutos): llenado de arterias coroideas, venas coroideas y vascularización retiniana.
Fase media (10-20 minutos): recirculación
Fase tardía (30 minutos): Vaciado de vasos coroideos (hipofluorescentes) contra un fondo teñido hiperfluorescente. La papila aparece hipofluorescente.
Aplicaciones
La angiografía con verde indocianina se emplea con mucha menor frecuencia que la angiografía fluoresceínica (relación aproximada de 1 a 10). La angiografía con verde indocianina es una técnica con indicaciones muy precisas que resulta de utilidad diagnóstica en (54):
DMAE con MNVS oculta, mal definida y asociada a DEP (57,58).
Vasculopatía polipoidea (59).
Maculopatías de otras causas (60,61).
Coroiditis (62).
Tumores coroideos: Hemangioma (63).
Otras patologías oculares en las que la AFG no llegaba a definir el diagnóstico.
4. IMAGEN QUIRÚRGICA
En el campo de la imagen quirúrgica en oftalmología la imagen en movimiento (video) ha ganado a la imagen estática. Sin embargo, en determinadas circunstancias puede ser de utilidad para ilustrar determinados pasos quirúrgicos.
Las imágenes quirúrgicas pueden ser captadas con dos equipos:
Cámaras externas.
Cámaras acopladas al microscopio quirúrgico.
Fotografía quirúrgica externa
Equipo
Se emplean los mismos equipos que los utilizados para fotografía ocular externa:
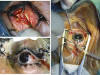
Fig. 13. Fotografía quirúrgica externa.
Tradicional: cámaras reflex de 35 mm con objetivos especiales «macro» de 105 mm de focal y unidades de flashes (flash para macrofotografía).
Digital: Cámaras compactas con objetivo equivalente a 35-105 mm o superior y flash incorporado. Su escaso volumen y fácil manejo lo hacen ideal para este tipo de imágenes.
Aplicaciones
Especialmente indicada en cirugía:
Oculoplástica y vías lagrimales.
Estrabismos.
Cirugías esclerales (DR).
Aspectos externos de cualquier cirugía ocular.
Fotografía con microscopio quirúrgico
Equipo
Microscopio quirúrgico con auxiliar coaxial.
Codo de acoplamiento para cámara.
Iluminación: luz del propio microscopio, no se emplea flash.
Cámara:
Tradicional: Reflex 35 mm. Películas diapositivas especiales para luz de tungsteno.
Digital: Cámaras compactas. Ajustar el balance de blancos (WB) para luz de interior (luz cálida). En condiciones de baja iluminación puede ajustarse la sensibilidad de la cámara (hasta 200 ó 400) para evitar imágenes borrosas.
Disparador: lo ideal es acoplar un dispositivo externo de disparo a la cámara (bien de mano o de pie) o dispositivos a distancia, para intentar interferir lo menos posible la labor del cirujano.
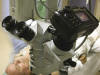
Fig. 14. Fotografía quirúrgica con microscopio. Equipo.
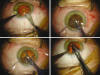
Fig. 15. Fotografías quirúrgicas con microscopio y cámara digital. Secuencia
quirúrgica de facoemulsificación.
Aplicaciones
Puede emplearse en cualquier tipo de cirugía ocular, pero resulta de especial interés en microcirugías:
Cirugías corneales.
Cirugía de catarata.
Cirugía de glaucoma.
Cirugías vitreorretinianas
CONCLUSIONES
Las técnicas de imagen se han incorporado a la oftalmología como herramientas de diagnóstico, con una clara proyección terapéutica en algunos casos, con aplicaciones en la clínica, la docencia y la investigación. A la imagen fotográfica (fotografía externa, fotografía de polo anterior, fotografía de fondo de ojo y fotografía quirúrgica), donde los equipos digital se imponen, se unen cada vez nuevas tecnologías de imagen con aplicación en la Oftalmología.
Probablemente el futuro nos depare imágenes con mejor resolución, equipos «integrales» que combinen varias técnica, y sistemas de captación y visualización en 3D más sencillos.
BIBLIOGRAFÍA
Gili P, Simón G, Yañez J. La Fotografía en Oftalmología. En: Publicación electronica en Oftalmología. Yañez J. Mesa redonda. 72 Congreso de la Sociedad Española de Oftalmología. 1996 Tecnimedia Editorial. Pg 161-203.
Justine J Jr. Ophthalmic Photography. Little, Brown and Company. 1982 Boston.
Saine PJ, Tyler ME. Ophthalmic photography: retinal photography, angiography, and electronic imaging. Patrick 2nd Ed. Butterworth-Heinemann. 2002 Woburn.
Vetter JP. Biomedical photography. Butterworth-Heinemann. 1992 Boston.
www7.ocn.ne.jp/~jops
Flowers CW jr, Baker RS, Khanna S, Ali B, March GA, Scott C, Murillo S. Teleophthalmology: rationale, current issues, future directions. Telemedicine Journal 1997; 3(1): 43-52.
Coma de Corral MJ, Pena HJ. Quo vadis telemedicina? Revista de Neurologia 1999; 29(5): 478-483.
Cuzzani O. teleoftalmología, presente y futuro. Arch Soc Esp Oftalmol 2000; 75(1): 1-2.
Li HK. Telemedicine and ophthalmology. Survey of ophthalmology 1999; 44 (1): 61-72.
Gonzalez F, Iglesias R, Suarez A, Gomez-Ulla F, Perez R. Teleophthalmology link between a primary health care centre and referente hospital. Medical Informatics and the Internet in Medicine 2001; 26(4): 251-263.
Tuulonen A, Ohinmaa T, Alanko HI, Hyytinen P, Juutinen A, Toppinen E. The application of teleophthalmology in examining patients with glaucoma: a pilot study. Journal of Glaucoma 1999; 8 (6): 367-373.
Li HK, Tang RA, Oschner K, Koplos C, Grady J, Crump WJ. Telemedicine screening of glaucoma. Telemedicine Journal 1999; 5 (3): 283-290.
Yogesan K, Constable IJ, Barry CJ, Eikelboom RH, Morgan W, Yay-Kearney ML, Jitskaia L. Evaluation of a portable fundus camera for use in the teleophthalmologic diagnosis of glaucoma. Journal of Glaucoma 1999; 8 (5): 297-301.
Tennant MT, Rudnisky CJ, Hinz BJ, Mac Donald IM, Greve MD.Tele-ophthalmology via stereoscopic digital imaging: a pilot project. Diabetes Technology and Therapeutics 2000; 2(4): 583-587.
Tennant MT, Greve MD, Rudnisky CJ, Hillson TR, Hinz BJ. Identification of diabetic retinopathy by stereoscopic digital imaging via teleophthalmology: a comparison to slide film. Canadian Journal of Ophthalmology 2001; 36(4): 187-196.
Gomez-Ulla F, Fernandez MI, Gonzalez F, Rey P, Rodriguez M, Rodriguez-Cid MJ, Casanueva FF, Tome MA, García-Tobio J, Gude F. Digital retinal images and teleophthalmology for detecting and grading diabetic retinopathy. Diabetes Care 2002; 25(8): 1348-1349.
Aoki N, DunnK, Fukui T, Beck JR, Schull WJ, Li HK. Cost-effectiveness analysis of telemedicine to evaluate diabetic retinopathy in a prison population. Diabetes Care 2004; 27(5): 1095-1101.
Christopherson KW. External Eye Photography: Equipment and Technique. In. Justine J Jr. Ophthalmisc Photography. Little, Brown and Company. 1982 Boston; 129-142.
Bartley GB, Younge BR. Stereoscopic external photography and the free-stereo viewing technique. Ophthalmic Plastic and Reconstructive Surgery 1991; 7(1): 67-68.
Mandell AI, Foster CW, Luther JD. External photography of the eye. International Ophthalmology Clinics 1976; 16(2): 133-143.
Allen L. Slit-lamp biomicrography. In. Justine J Jr. Ophthalmisc Photography. Little, Brown and Company. 1982 Boston. 143-172.
West SK, Rosenthal F, Newland HS, Taylor HR. Use of photographic techniques to grade nuclear cataracts. Invest Ohthalmol Vis Sci 1988; 29: 73-77.
Takahashi M, Trempe CL, Schepens CL. Biomicroscopic evaluation and photography of posterior vitreous detachment Arch Ophthalmol 1980; 98(4): 665-668.
Kakehashi A, Inoda S, Shimizu Y, Makino S, Shimizu H. Combined system of biomicroscopic vitreous videography and photography. Retina 1999; 19(1): 65-68.
Chalam KV, Shah VA. Slit lamp biomicroscopy adapter for simultaneous photodocumentation during clinical assessment. J Cataract Refract surg 2004; 30: 1808-1809.
Van den Berg TJ, Coppens JC. Conversion of lens slit lamp photographs into physical light-scattering units. Invest Ophthal Vis Scienece 1999; 40 (9): 2151-2157.
Findl O, Buehl W, Siegl H, Pinz A. Removal of reflections in the photographic assessment of PCO by fusion of digital retroillumination images. Invest Ophthalmol Vis Sci 2003; 44: 275-280.
Hirst LW, Yamauchi K, ENHER C, Vogelpohl W, Whittington V. Quantitative analysis of wide-field specular microscopy. II. Precision of sampling from the central corneal endothelium.Inves Ophthalmol Vis Science 1989; 30 (9): 1972-1979.
Anonymous. Corneal endotelial photography. American Academy of Ophthalmology. Ophthalmology 1991; 98 (9): 1464-1468.
Tsubota K, Yamada M, Naoi S. Specular microscopio observation of normal human corneal epithelium. Ophthalmology 1992. 99 (1): 89-94.
Anonymus. Corneal endotelial photography. Three-year revision. American Academy of Ophthalmology. Ophthalmology 1997; 104(8): 1360-1365.
Yannuzzi LA, Ober MD, Slakter JS, Spaide RF, Fisher YL, Flower RW, Rosen R. Ophthalmic fundus imaging: today and beyond. Am J Ophthalmol 2004; 137: 511-524.
Jackman WT, webster JD. On photographing the retina of the living human eye. Philadelphia Photographer 1886; 23: 275.
Rudnisky CJ, Linz BJ, Tennant MT, de Leon AR, Greve MD. High-resolution stereoscopic digital fundus photography versus contact lens biomicroscopy for detection of clinically significant macular edema. Ophtalmology 2002; 109: 267-274.
Gili Manzanaro P, Carrasco Font C, Martín Rodrigo JC, Yangüela Rodilla J, Arias Puente A. Análisis digital de la papila con cámara de fondo convencional: estudio de variabilidad. Arch Soc Esp Oftalmol 2004; 79: 125-130.
Saine PJ. Fundus Photography: Interpretation and technique. In: Ophthalmic photography: retinal photography, angiography, and electronic imaging. Patrick J. Saine, Marshall E.Tyler. 2nd Ed. Butterworth-Heinemann. 2002 Woburn. Capítulo 2. Páginas 13-96.
Ortiz RG. Lopez PF. Lambert HM. Sternberg P Jr. Aaberg TM.Examination of macular vitreoretinal interface disorders with monochromatic photography.American J Ophthalmology 1992; 113(3): 243-247.
Sommer A, Katz J, Quigley HA, Miller NR, Robin AL, Richter RC, et al. Clinically detectable nerve fiber atrophy precedes the onset of glaucomatous field loss. Arc Ophthalmol 1991; 109: 77-83.
Honrubia FM, Calonge B, Abecia E, Gomez ML. Correlación entre los defectos en la capa de las fibras nerviosas de la retina y el glaucoma. Arch Soc Esp Oftalmol 1992; 62: 107: 112.
Behrendt T, Slipakoff E. Spectral reflectance photography. In: Ophthalmic Photography. Justice J Jr. Little, Brown and company. Boston 1982; 95-99.
Ortiz RG. Lopez PF. Lambert HM. Sternberg P Jr. Aaberg TM.Examination of macular vitreoretinal interface disorders with monochromatic photography.American J Ophthalmology 1992; 113(3): 243-247.
Weinberger D, Stiebel-Kalish H, Priel E, Barash D, Axer-Siegel R, Yassur Y. Digital red-free photography for the evaluation of retinal blood vessel displacement in epiretinal membrane. Ophthalmology 1999; 106: 1380-1383.
Sommer A, Katz J, Quigley HA, Miller NR, Robin AL, Richter RC, et al. Clinically detectable nerve fiber atrophy precedes the onset of glaucomatous field loss. Arc Ophthalmol 1991; 109: 77-83.
Honrubia FM, Calonge B, Abecia E, Gomez ML. Correlación entre los defectos en la capa de las fibras nerviosas de la retina y el glaucoma. Arch Soc Esp Oftalmol 1992; 62: 107: 112.
Katsuhito Fukui, Akitoshi Yoshida, Yuji Kato, Hiromasa Igarashi. The usefulness of fundus photography with red light for the diagnosis of central serous chorioretinopathy. Journal of Ophthalmic Photography 2002; 24: 36-39.
Katsuhito Fukui, Yuji Kato, Hiromasa Igarashi. Screening of choroidal diseases using fundus photography with red rays. The Japanese Journal of Medical Photography 1999; 37: 2-11.
Novotni HR, Alvis DL. A method of photographing fluorescente in circulating blood in the human retina. Circulation 1961; 24: 82.
Flower RW, Hochheimer BF. Clinical infrared absorption angiography of the choroid. Am J Ophthalmol 1972; 73: 458.
Regillo CD. The present role of indocyanine grren angiography in ophthalmology. Curr Opin Ophthalmol 1999; 10: 189-196.
Stanga PE, Lim JI, Hamilton P. Indocyanine green angiography in chorioretinal diseases: indications and interpretation. An evidence-based update. Ophthalmology 2003; 110: 15-24.
Hope-Ross M, Yannuzzi LA, Gragoudas ES, et al. Adverse reactions due to indocyanine green . Ophthalmology 1994; 101: 529-533.
Obana A, Miki T, Hayashi K, et al. Survey of complications of indocyanine green angiography in Japan. Am J Ophthalmol 1994; 118: 749-753.
Reichel E, Duker JS, Puliafito CA. Indocyanine green angiography and choroidal neovascularization obscured by hemorrhage. Ophthalmology 1995; 102: 1871-1876.
Guyer DR, Yannuzzi LA, Slakter JS, et al. Digital indocyanine-green videoangiography of occult choroidal neovascularization. Ophthalmology 1994; 101: 1727-1737.
Yannuzzi LA, Ciardella A, Spaide RF et al . The expanding clinical expectrum of idiopathic polipoidal choroidal vasculopathy. Arch Ophthalmol 1997; 115: 478-485.
Brancato R, Trabucchi G, Introini U, et al. Indocyanine grren angiography (ICGA) in patological miopía. Eur J Ophthalmol 1996; 6: 39-43.
Spaide RF, may L, Hass A, et al. Indocyanine green angiography of older patients with central serous chorioretinopathy. Retina 1996; 16: 203-213.
García Saenz MC, Gili Manzanaro P, Bañuelos Bañuelos J, Villarejo Díaz-Maroto I, Arias Puente A. Valoración de enfermedades inflamatorias coriorretinianas con angiografía verde indocianina. Arch Soc Esp Oftalmol 2003; 78: 675-684.
Mashayekhi A, Shields CL. Circumscribed choroidal hemangioma. Curr Opin in Ohthalmol 2003; 14: 142-149.