COMUNICACIÓN SOLICITADA
Tratamiento del glaucoma neovascular. Papel de los fármacos antiangiogénicos
MARTÍN GIRAL E1, PERUCHO MARTÍNEZ S2, FERNÁNDEZ ESCÁMEZ CS1, TOLEDANO FERNÁNDEZ N2
Hospital
Universitario de Fuenlabrada. Servicio de Oftalmología. Madrid.
1
Licenciada en Medicina.
2
Doctor en Medicina.
RESUMEN
El glaucoma neovascular (GNV) designa a un tipo de glaucoma relativamente frecuente y con un efecto devastador sobre el potencial visual, que ocurre secundariamente a la proliferación de neovasos sobre el iris y en el ángulo camerular.
El estímulo principal que promueve el desarrollo del GNV es la hipoxia retiniana severa. Puede aparecer asociado a retinopatía diabética severa, oclusiones vasculares, síndrome de isquemia ocular, enfermedad de células falciformes o desprendimiento de retina de larga evolución.
La aparición de nuevos fármacos antiangiogénicos ha supuesto una pequeña revolución en el tratamiento de esta patología pero todavía hay muchas incógnitas por aclarar.
El objetivo de esta revisión es actualizar los conocimientos disponibles hasta ahora sobre el uso de los nuevos fármacos antiangiogénicos en el glaucoma neovascular.
Palabras claves: Antiangiogénicos, glaucoma neovascular.
GLAUCOMA NEOVASCULAR (GNV). DEFINICIÓN Y MECANISMO
El GNV es un tipo de glaucoma por cierre angular segundario sin bloqueo pupilar. Se trata de un cuadro clínico derivado de una situación de isquemia retiniana o de inflamación intraocular que pueden tener diferentes orígenes (tabla 1). Las causas más frecuentes son la diabetes mellitus, oclusión de la vena central de la retina y síndrome isquémico ocular.

La enfermedad se caracteriza por la proliferación de finos vasos sobre la superficie del iris y la malla trabecular que asientan sobre una membrana fibrosa transparente, cuando ésta se contrae es la responsable de la formación de sinequias que producen el cierre angular secundario. Aunque el cierre angular suele ser un cierre progresivo, el GNV clínicamente se suele presentar como un glaucoma agudo o subagudo con dolor, fotofobia, epífora y aumento de la presión intraocular (PIO) así como disminución de la agudeza visual (AV).
Clínicamente podemos encontrar las siguientes fases (1):
-
Fase de rubeosis (estadio preglaucomatoso). Se caracteriza por PIO normal. Se puede observar fina rubeosis. El ángulo puede estar neovascularizado o no pero siempre está abierto.
-
Fase de glaucoma de ángulo abierto. Encontramos una rubeosis más florida con reacción inflamatoria en cámara anterior. Encontramos neovasos en ángulo y un aumento progresivo de la PIO. En este estadio puede haber hipema con debut de un glaucoma agudo.
-
Fase de glaucoma de ángulo cerrado. Cierre sinequial parcial o completo del ángulo. Suele estar presente un ectropión uveal. En este estadio el glaucoma suele ser severo con importante elevación de la PIO. Suele ser necesario tratamiento quirúrgico.
Diagnóstico diferencial (1,2)
En la fase de ángulo abierto debemos diferenciarlo de otros glaucomas de comienzo agudo con neovasos en iris:
-
Glaucoma asociado a uveítis (uveítis heterocrómica de Fuchs).
-
Vasos fisiológicos en estroma de iris claros.
En la fase de ángulo cerrado debemos diferenciarlo de otros glaucomas por cierre angular de otra etilogía:
-
Traumatismos.
-
Síndromes irido-corneo-endoteliales.
-
Glaucomas facogénicos.
-
Tumores, …
ANGIOGÉNESIS Y FACTOR DE CRECIMIENTO ENDOTELIAL VASCULAR
La angiogénesis está regulada por diversos factores pro-angiogénicos y antiangiogénicos, cuyo desequilibrio conlleva a la formación de neovasos.
Se ha demostrado en numerosos trabajos que VEGF es un elemento clave en el proceso de angiogénesis. VEGF es un miembro de una familia de proteínas que incluyen VEGF-A, VEGF-B, VEGF-C, VEGF-D y PGF (placental growth factor). Su efecto está mediado por tres receptores con actividad tirosina-quinasa: VEGFR-1, VEGFR-2 y VEGF-3.
VEGF-A y sus isoformas son considerados los principales mediadores de la neovascularización patológica. Por ello, el término clásico de VEGF hace referencia a VEGF-A. Existen cinco isoformas de VEGF-A generadas a través del splicing alternativo de una misma molécula de RNA mensajero transcrito desde un único gen.
Las isoformas más estudiadas son VEGF121, VEGF165 y VEGF189. La nomenclatura utilizada hace referencia al número de aminoácidos que componen la molécula madura. Por ejemplo, VEGF165 contiene 165 aminoácidos y típicamente aparece como un homodímero.
VEGF induce la proliferación de células endoteliales, promueve la migración celular e inhíbe la apoptosis. In vivo, VEGF induce la angiogénesis e incrementa la permeabilidad vascular, jugando un papel central en la regulación de la vasculogénesis.
VEGF es un potente mitógeno específico para las células del endotelio vascular. De todas las moléculas liberadas por la retina isquémica, VEGF parece ser la única con actividad mitótica sobre las células endoteliales. La asociación entre los niveles de VEGF y la neovascularización de la córnea, iris, retina y coroides ha sido constatada en modelos experimentales. Cuando VEGF es inhibida de modo selectivo en estos modelos animales se aprecia una supresión en el crecimiento de neovasos en estos tejidos (3).
La correlación en humanos implicando a VEGF y sus receptores en la enfermedad neovascular ha sido verificada en diversos trabajos implicando a pacientes con retinopatía diabética, oclusión de vena retiniana, neovascularización de iris, retinopatía de la prematuridad y degeneración macular asociada a la edad de tipo exudativo. En todos ellos, los datos obtenidos implican a VEGF en el proceso de crecimiento vascular patológico (4).
TRATAMIENTO DEL GNV (fig. 1)
El tratamiento del glaucoma neovascular se fundamenta en tres pilares:
a) Tratamiento del factor
etiopatogénico.
b) Tratamiento inmediato de la elevación aguda de la PIO.
c) Tratamiento del glaucoma residual.
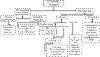
Fig. 1: Algoritmo manejo del GNV.
A) Tratamiento del factor etiopatogénico:
1. Retinopatia diabética: Está indicada la panfotocoagulación en casos de retinopatía diabética proliferativa o retinopatía diabética no proliferativa severa con factores de riesgo añadidos (neovascularización en el ojo adelfo, mal control metabólico, mal cumplimiento del tratamiento de la enfermedad de base o catarata en evolución que impedirá próximamente una correcta visualización del fondo de ojo (5). La regresión de los neovasos tras una PFC completa ocurre entre cuatro y seis semanas después. En casos con opacidad de medios (hemovitreo severo y persistente o catarata madura) que impida una correcta visualización y realización del procedimiento se indicará cirugía vitreorretiniana y endofotocoagulación.
2. Trombosis de la Vena Central de la Retina:
La PFC solo está indicada cuando ya existe neovascularización y no de forma profiláctica (6). La regresión de los neovasos se consigue en cuatro a ocho semanas.
3. Síndrome de Isquemia Ocular: La PFC es controvertida en este caso ya que el origen de la isquemia sería la úvea y no la retina propiamente dicha (7). Los hipotensores oculares pueden ayudar a mejorar la presión de perfusión intraocular.
4. Resto de patología: Tumores, Uveítis, vasculitis, traumatismos, etc. se realizará el tratamiento etiológico correspondiente.
B) Control de la HTO aguda: Las recomendaciones de la Sociedad Europea de Glaucoma (8) son:
1. Corticoides: Acetato de Prednisolona 1% cada 4/6 horas.
2. Ciclopléjicos: Atropina 1% cada 8/12 horas.
3. Hipotensores: betabloqueantes, alfa agonistas e inhibidores de la anhidrasa carbónica tópicos y sistémicos. Se desaconseja el uso de análogos de prostaglandinas por su posible efecto proinflamatorio y de la pilocarpina por su efecto miótico.
C) Tratamiento del glaucoma residual: El glaucoma neovascular se ha considerado hasta hoy una patología quirúrgica (9). Los procedimientos posibles incluyen:
1. Trabeculectomía convencional sin o con antimitóticos: en casos con actividad de la enfermedad de base controlada, sin cierre sinequial completo y proceso neovascular inactivo.
2. Dispositivos de drenaje: en casos con actividad neovascular sin controlar, cierre sinequial en evolución y alto riesgo de recurrencia. Se recomienda la colocación del tubo en sulcus y la facoemulsificacion asociada (10).
3. Procedimientos ciclodestructivos: se recomiendan como segunda línea de tratamiento para el control del dolor en ojos con glaucoma absoluto.
PAPEL DE LOS ANTIANGIOGÉNICOS
Los fármacos antiangiogénicos (Anti-VEGF) actúan uniéndose al factor de crecimiento endotelial (VEGF) e impidiendo su acción vasoproliferativa.
El Bevacizumab (Avastin R, Genetech Inc., San Francisco, CA, EEUU) y el Ranibizumab (Lucentis R, Genetech Inc., San Francisco, CA, EEUU) son anticuerpos monoclonales anti-VEGF. Se diferencias en el tamaño molecular, siendo Ranibizumab más pequeño al carecer de una parte de la molécula que actúa como transportador. Esto favorece su penetración en la retina pero también puede disminuir su vida media dentro de la cavidad vítrea.
El Pegaptanib (Macugen R, Eyetech Pharmacutticals Inc. NY, EEUU) es un aptámero que actúa únicamente contra la isoforma VEGF-165, responsable de la neovascularización ocular y por tanto más selectivo que los anteriores.
El más estudiado de todos ellos para el tratamiento del glaucoma neovascular, hoy por hoy, es el Bevacizumab.
Estos fármacos han supuesto una pequeña revolución en el tratamiento del glaucoma neovascular. Parece demostrado que los Antivegf: inducen la regresión de los neovasos en pocas horas, controlan el cierre sinequial y reducen la congestión e inflamación asociadas (fig. 2). Esto no excluye la necesidad de tratamiento ablativo de la retina isquémica ni la necesidad de cirugía filtrante en la gran mayoría de los casos, pero sí permite realizar estos tratamientos con menos urgencia, de forma reglada, con menos complicaciones y con mejores resultados finales.
Hasta nuestro conocimiento en la actualidad solo se ha publicado un ensayo clínico controlado randomizado y enmascarado de casos y controles (11). En él el autor demuesta que el bevacizumab intravítreo, administrado a dosis de 2.50 mg en tres inyecciones separadas por cuatro semanas en eficaz en el control de la neovascularizacion iridiana y la PIO en el tratamiento del GNV, el autor describe que el efecto se mantiene seis meses después y siempre realiza el tratamiento de forma adyuvante a la cirugía y el tratamiento láser cuando se requiere.
Parece claro que el efecto antiangiogénico de estas sustancias es temporal y solo logramos que permanezca en el tiempo cuando se realiza un tratamiento ablativo de la retina isquémica junto con la inyección de la sustancia. Se ha publicado la persistencia del efecto antiangiogénico tras tres inyecciones de Bevacizumab hasta 12 meses después (12). Cuando se produce el cierre angular completo el pronóstico de la enfermedad se ensombrece y la respuesta a los tratamientos es más impredecible. Algunos estudios (13) han puesto de manifiesto la importancia de realizar el tratamiento con antivegf de forma lo más precoz posible.
Con respecto a la cuestión de la dosificación, existen dos pautas: inyecciones de 1.25 mg/ml o 2.50 mg/ml. Un estudio (14) comparó el efecto de Bevacizumab intravítreo a dosis de 1.25 mg y de 2.50 mg en una sola inyección previa a Trabeculectomía sin encontrar diferencias estadísticamente significativas. La mayoría de las publicaciones existentes utilizan la pauta de 1.25 mg ya que parece que doblar la dosis no aportaría un mayor beneficio.
En cuanto al lugar de administración puede ser tanto en cámara anterior como en la cavidad vítrea, estudios publicados (15,16) han demostrado buenos resultados tanto en un sentido como en otro. La inyección en cavidad vítrea tendría la teórica ventaja de colocar el fármaco cerca de la retina que es su diana terapéutica. Sin embargo, la técnica de la inyección intracamerular es accesible para todos los oftalmólogos, dada su sencillez y seguridad. La rapidez con la que ocurre el efecto antiangiogénico parece ser la misma independientemente del lugar de administración, aún así no existen estudios controlados que demuestren la superioridad de una vía sobre otra.
Con respecto al número de inyecciones necesarias tampoco existe consenso. Sí parece claro que una sola dosis en muchos casos es insuficicente y el hecho de utilizar tres inyecciones separadas por cuatro semanas de aplicación puede proporcionar buenos resultados y el tiempo suficiente para realizar el tratamiento laser o quirúrgico que sea necesario (11).
CONCLUSIÓN
En definitiva, los antiangiogénicos , y en especial el Bevacizumab se han convertido hoy por hoy en una herramienta de innegable utilidad en el manejo de un tipo de glaucoma como es el glaucoma neovascular muy agresivo, difícil de manejar y con mal pronóstico en la mayoría de los casos. La sencillez de su administración, la rapidez del efecto antiangiogénico y las muy escasas complicaciones publicadas son argumentos a favor de su uso como tratamiento adyuvante en el manejo de esta patología. Sin embargo es necesaria la realización de ensayos clínicos debidamente controlados que respalden estos hallazgos con mayor evidencia cientifica.
BIBLIOGRAFÍA
-
Shields MB. Textbook of Glaucoma. 5th ed. Philadelphia: Lippincott Williams & Wilkins; 2005.
-
Stamper RL, Lieberman MF, Drake MV, eds. Becker – Shaffer´s Diagnosis and Therapy of the Glaucomas. 7th ed. St Louis: Mosby; 1999.
-
Adamis AP, Shima DT. The role of vascular endothelial growth factor in ocular health and disease. Retina 2005 Feb-Mar; 25(2): 111-118.
-
Ciulla TA, Rosenfeld PJ. Anti-vascular endothelial growth factor therapy for neovascular ocular diseases other than age-related macular degeneration. Curr. Opin. Ophthalmol. 2009 May; 20(3): 166-174.
-
Pareja-Rios et al., Guías de práctica clínica de la SERV: Manejo de las complicaciones oculares de la diabetes. Retinopatía diabética y edema macular. Arch Soc Esp Oftalmol [online]. 2009, vol. 84, n.9, pp. 429-450.
-
Gomez-Ulla et al. Manejo de las Oclusiones Venosas de la Retina. Guías de Práctica Clínica de la SERV.
-
Johnston ME, Gonder JR, Canny CL. Succesfull treatmente for the ocular ischemic síndrome with panretinal fotocoagulation and cerebrovascular surgery. Can J Ophthalmol. 1988; 23: 114-117.
-
Terminology and guidelines for glaucoma(3rd edition):Therapetic guides: secondary angle closure glaucoma.European Glaucoma Society 2009. Pp: 181.
-
Garcia Sanchez, Julian; Honrubia Lopez, Francisco. Actualizacion en el tratamiento del Glaucoma. Sociedad Española de Oftalmología. 2003.
-
Gutierrez Dia, Esperanza, Montero Rodriguez , Marta. Dispositivos de Drenaje para glaucoma. Ed Ergon 2002.
-
Yazdani S, Hendi K, Pakravan M, Mahdavi M, Yaseri M. Intravitreal bevacizumab for neovascular glaucoma: a randomized controlled trial. J Glaucoma Oct-nov 2009, vol18, nº 8: 632-637.
-
C. Costagliola et al. Intravitreal Bevacizumab injection for neovascular glaucoma: a survey of 23 cases throughout 12 months follow-up. Br J Clin Pharmacol/66: 5/667-673.
-
Intravitreal Bevacizumab to treat iris neovascularization and neovascular glaucoma secondary to Ischemic retinal dieases in 41 consecutive cases. Ophthalmology. 2008 Sep; 115(9): 1571-80.
-
Gupta V, Jha R, Rao A, Kong G, Sihota R The effect of different doses of intracameral bevacizumab on surgical outcomes of trabeculectomy for neovascular glaucoma. European Journal of Ophthalmology / Vol. 19 no. 3, 2009; pp. 435-441.
-
Susana Duch, MD, PhD, Oscar Buchacra, MD, Elena Milla, MD, PhD, David Andreu, MD, PhD, and Jesu´s Tellez, MD. Intracameral Bevacizumab (Avastin) for Neovascular Glaucoma.A Pilot Study in 6 Patients. J Glaucoma _ Volume 18, Number 2, February 2009; 140-143.
-
Intravitreal bevacizumab as an adjunct treatment for neovascular glaucoma. Hasanreisoglu M, Weinberger D, Mimouni K, Luski M, Bourla D, Kramer M, Robinson A, Axer-Siegel R. Eur J Ophthalmol. 2009 Jul-Aug; 19(4): 607-12.